您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-12-21 09:11
2020年12月17日,由微创神通医疗科技(上海)有限公司(以下简称“微创®神通”)自主研发的Bridge®椎动脉药物支架获得国家药品监督管理局(NMPA)颁发的上市注册证,该产品可应用于症状性椎动脉狭窄的治疗。
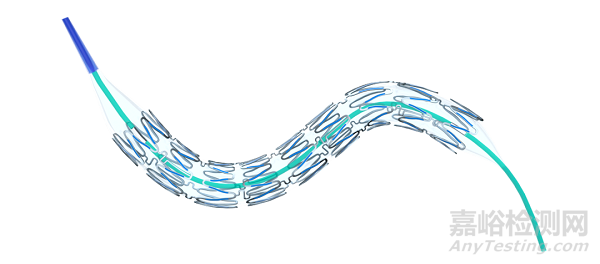
Bridge®椎动脉药物支架
《中国脑卒中防治报告2019》援引最新全球疾病负担研究(Global Burden of Disease Study, GBD)数据指出,我国缺血性卒中发病率不断上升,由2005年的1.12/1000升高至2017年1.56/1000。在缺血性卒中的人群中,后循环缺血性卒中占25%-40%,而9%-33%的后循环缺血性患者有椎动脉起始部狭窄或闭塞。临床上,支架置入术已成为治疗椎动脉狭窄的主要方法。支架置入可以即时有效地改善脑血流,起到预防卒中再次发作及降低后循环缺血性损伤的作用。但由于解剖结构等原因,置入金属裸支架血管再狭窄发生率高,而药物涂层支架在椎动脉狭窄治疗中的再狭窄率、症状复发率与再治疗率更低[1],但药物引起的副作用仍不可忽视。
微创®神通此次获批上市的Bridge®椎动脉药物支架采用了独特的载药设计方式,药物仅储存于支架贴血管壁表面的凹槽内能更早完成内皮化进程,减少血栓事件与再狭窄[2]。

Bridge®椎动脉药物支架采用了独特的载药设计方式
Bridge®支架上市前临床试验由北京天坛医院牵头、全国6家临床中心共同参与。研究数据显示,Bridge®支架植入成功率98%,术后6个月支架内再狭窄发生率3.7%。在长期随访的病例中,支架植入4年后DSA复查未发现支架内再狭窄,证明了Bridge®支架的长期有效性。
Bridge®椎动脉药物支架的获批上市,进一步完善了微创®神通的神经介入产品线。微创®神通总裁谢志永表示:“ Bridge®椎动脉药物支架通过NMPA创新医疗器械特别审批程序获准上市,将会为症状性椎动脉狭窄患者患者带来更完善的治疗方案。微创®神通会坚持创新研发,并努力把创新的治疗方案提供到离患者更近的地方,拯救大脑,继续生命之精彩。”
参考资料:
[1] J Neurointerv Surg. 2016 Aug;8(8):770-4
[2] Circulation. 2001 Jun 12;103(23):2816-21

来源:微创MicroPort


