您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-02-28 11:05
作者:刘春雨 , 于传飞 , 崔永霏 , 武刚 , 黄璟 , 王兰
中国食品药品检定研究院, 卫生部生物技术产品检定方法及标准化重点实验室, 北京 102629
摘要:
目的: 利用AlphaLISA方法建立抗白介素-17受体单抗的生物学活性测定方法。方法: 以人包皮成纤维细胞系作为靶细胞,通过AlphaLISA检测系统建立抗IL-17R单抗的生物学活性测定方法,根据四参数拟合分析计算抗IL-17R单抗的相对效价,并对该方法进行了验证。结果: 抗IL-17R单抗在该方法中存在量效关系,并且符合四参数方程:y=(A-D)/[1+(x/C)B]+D。6批抗IL-17R单抗经3次测定,相对效价平均值在(84.93±3.12)%~(107.51±1.66)%,相对标准偏差小于5%。2批回收率样品经3次测定,回收率分别为(100.66±13.65)%和(115.69±3.85)%。结论: 本研究利用AlphaLISA方法在国内首次成功建立重复性好、准确性高的抗IL-17R单抗的生物学活性测定方法。
关键词:抗IL-17R单抗 单克隆抗体 生物学活性 AlphaLISA法
白介素-17(Interleukin-17, IL-17)是由属于T细胞亚群的Th17细胞分泌产生的, 在啮齿类T细胞杂交筛选试验中首次被鉴别出来, 最早被命名为细胞毒T淋巴细胞相关抗原8(Cytotoxic T-lymphocyte-associated Antigen 8, CTLA-8)[1]。IL-17家族目前已有六种蛋白, 分别为IL-17A、IL-17B、IL-17C、IL-17D、IL-17E和IL-17F。而IL-17的受体为IL-17R(Interleukin-17 Receptor, IL-17R), 同样存在几种同源蛋白, 分别为IL-17RA、IL-17RB、IL-17RC、IL-17RD和IL17RE[2]。人源IL-17A以同源二聚体或与IL-17F形成异源二聚体的形式存在。IL-17A、IL-17F以及IL-17A/F的受体都是IL-17RA和IL-17RC形成的异源二聚体。IL-17与IL-17R特异性结合, 可以促进成纤维细胞及上皮细胞的转录因子NF-κB的激活以及IL-8的分泌, 共同促进T细胞的增殖并与炎症反应相关[3]。还能诱导肿瘤坏死因子-α(Tumor Necrosis Factor α, TNF-α)、IL-8、IL-1β、生长相关的癌基因-α(Growth Related Oncogene, GRO-α)等多种细胞因子的表达[4-6]。IL-17在宿主抵御各种微生物感染中起了重要作用, 如复发性葡萄球菌感染和粘膜皮肤念珠菌病等[7-8]。
IL-17A信号通路与各种自身免疫病包括银屑病(Psoriasis, Ps)、银屑病性关节炎(Psoriaticarthritis, PsA)、类风湿性关节炎(Rheumatoid Arthritis, RA)、多发性硬化症(Multiple Sclerosis, MS)、系统性红斑狼疮(Systemic Lupus Erythematosus, SLE)等均有一定的关联[9-13]。以IL-17及IL-17R为靶点的单抗, 可以靶向性特异结合于其配体, 达到阻断信号传导通路的作用, 从而抑制炎性细胞因子的产生, 主要用于银屑病等自身免疫疾病的治疗[14-15]。
Alpha技术, 即放大化学发光亲和均相检测(Amplified Luminescent Proximity Homogeneous Assay, Alpha), 是一种以微珠为基础的检测技术, 包括供体微珠(Donor Beads)和受体微珠(Acceptor Beads)。结合于供体微珠上的分子(分子A)与结合于受体微珠上的分子(分子B)发生相互作用, 当两个微珠达到足够接近的状态时, 能够检测出发光信号。供体微珠表面的光敏剂经激光照射而受到激发, 将周围的氧转变为激发态的单线态氧。单线态氧向供体微珠周围扩散, 到达附近的受体微珠后可在微珠内引发化学发光反应, 并最终发射出光。反之, 如果各微珠上的分子A与分子B不发生相互作用, 则供体微珠产生的单线态氧不会到达受体微珠, 则不会引发化学发光反应, 见图 1。
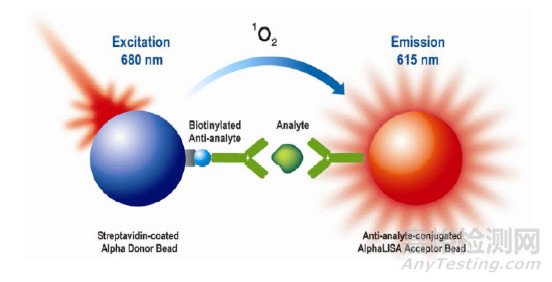
图 1 AlphaLISA技术检测原理
受体微珠根据不同染料, 其检测波长也不同, AlphaLISA受体微珠标记铕(Eu), 其发射波长为615~623 nm, 适用于缓冲液、细胞培养上清液和细胞裂解液样品[16-17]。具有亲和性强, 背景值低、灵敏度高的特点。
本文利用AlphaLISA技术, 以HFF-1细胞为靶细胞, 在国内首次建立了准确、快速的抗IL-17R抗体的生物学活性测定方法。
1 材料和方法
1.1 药品与试剂
HFF-1细胞系为本实验室留存(ATCC, SCRC-1041);抗IL-17R单抗参比品和供试品均为本实验室留样; IL-17A购自Amgen公司; 胎牛血清(FBS)、胰酶(Trypsin)、DMEM培养基、磷酸盐缓冲液(PBS)购自GIBCO公司; AlphaLISA IL-8试剂盒购自PE公司。
1.2 主要仪器
多功能酶标仪(Perkin Elmer公司); SoftMax分析软件(Molecular Devices公司)。
1.3 检测方法
1.3.1 生物学活性检测原理
HFF-1细胞系是人包皮成纤维细胞系(Human Foreskin Fibroblast, HFF-1), 可稳定表达IL17R, 位于细胞表面的IL-17R与IL-17A结合后, 激活细胞并将IL-8分泌至细胞培养上清中, 见图 2。IL-8则通过AlphaLISA技术进行检测[13, 17]。IL-8将AlphaLISA抗IL-8受体微珠与链亲和素-生物素化的抗IL-8供体微珠桥联起来形成供体受体复合物。该复合物接受激光照射后, 可激发能量释放出AlphaLISA信号, 信号强度剂量依赖性与IL-8剂量成正比, 与抗IL-17R单抗剂量成反比。
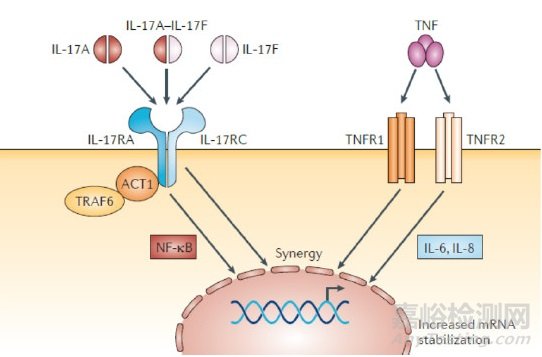
图 2 抗IL-17R单抗生物学活性检测原理
1.3.2 抗IL-17R单抗的生物学活性测定
HFF-1细胞培养至对数生长期, 加入0.25%EDTA的胰酶, 置于37 ℃、5%CO2培养箱中消化1~2 min, 加入5 mL含10% FBS的DMEM培养基(完全培养基)终止消化, 200 g离心5 min后以含0.1 % FBS的DMEM培养基(稀释液)重悬细胞, 调整细胞浓度至8×104个·mL-1, 以每孔100 μL接种于96孔白板中, 置于37 ℃、5% CO2培养箱中培养1~3 h; 以含有600 ng·mL-1 IL-17A的稀释液将抗IL-17R单抗及参比品稀释至起始浓度为3000 ng·mL-1, 再以稀释液按照1:2.5的比例往下稀释, 共10个稀释度, 每个稀释度设双复孔, 将稀释后的抗IL-17R单抗转入细胞培养板, 每孔50 μL, 细胞培养板置于37 ℃、5% CO2条件下培养过夜(16~20 h); 次日进行AlphaLISA检测:以AlphaLISA工作缓冲液稀释生物素化抗IL-8抗体和AlphaLISA抗IL-8受体微珠, 加入测定用96孔白色半孔板, 每孔20μL, 使半孔板中生物素化抗IL-8抗体的终浓度为2.5 nmol·L-1、AlphaLISA抗IL-8受体微珠的终浓度为25 μg·mL-1;将细胞培养板取出, 270 g离心10 min后细胞培养上清转入测定用96孔白色半孔板, 每孔20μL, 避光室温孵育50~75 min; 以AlphaLISA工作缓冲液稀释链亲和素标记的供体微珠, 加入测定用96孔白色半孔板, 每孔20μL, 使半孔板中链亲和素-生物素化的抗IL-8供体微珠终浓度为40μg·mL-1, 室温避光孵育25~40 min; 设置起始照射光波长为680 nm, 化学发光信号波长为615 nm, 读取AlphaLISA信号值(AlphaLISA Signal); 利用SoftMax软件分析数据, 以抗IL-17R单抗浓度对数为x轴, 对应的AlphaLISA信号值为y轴, 选用四参数方程回归模型, 拟合剂量效应曲线, 得到曲线的半数有效浓度(50 Percent of Effective Concentration, EC50), 按照下述公式计算供试品的相对效价。
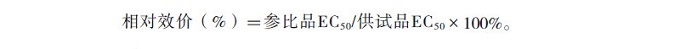
1.3.3 抗IL-17R单抗生物学活性的方法学验证
1.3.3.1 精密性试验
分别测定6批供试品的生物学活性, 每批重复测定3次, 计算RSD, 验证该方法的精密性。
1.3.3.2 准确性试验
将2批供试品与参比品等体积混合制备回收率样品, 测定其生物学活性, 每批重复测定3次, 按下述公式计算回收率, 验证该方法的准确性。

2 结果
2.1 抗IL-17R生物学活性剂量效应曲线
以抗IL-17R单抗浓度为x轴, 对应的AlphaLISA信号值为y轴, 选用四参数方程回归模型, 拟合抗IL-17R单抗的剂量效应曲线。所得数据经SoftMax软件分析, 符合四参数方程式:y=(A-D)/[1+(x/C)B]+D, 在半对数坐标轴上呈典型的反S型曲线, R2 >0.99, 见图 3。抗IL-17R单抗剂量效应曲线上参比品及供试品的EC50分别为3.78 ng·mL-1和3.69 ng·mL-1。
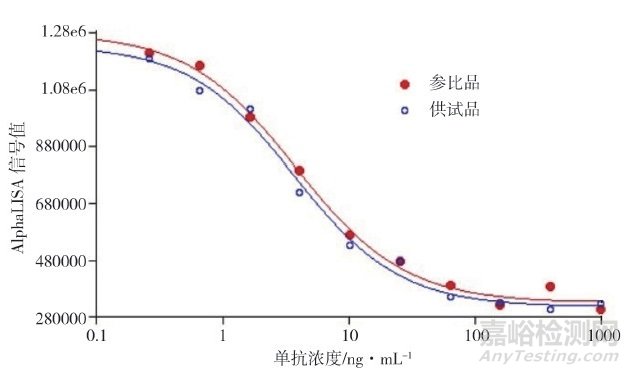
图 3 抗IL-17R单抗生物学活性的剂量效应曲线
2.2 方法学验证结果
2.2.1 精密性
同时检测6批抗IL-17R单抗与参比品, 每批进行3次重复测定, 计算相对效价, 结果显示6批抗IL-17R单抗的相对效价平均值在(84.93± 3.12)% ~(107.51±1.66)%, RSD均小于5 %, 结果见表 1。
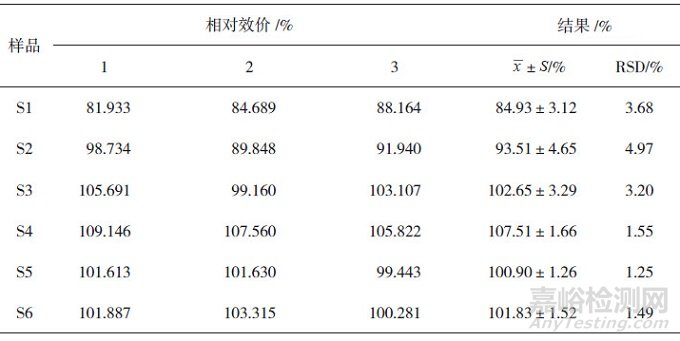
表 1 抗IL-17R单抗生物学活性精密性试验结果
2.2.2 准确性
将2批供试品与参比品等体积混合制备回收率样品, 测定其生物学活性, 分别重复测定3次, 2批回收率样品的回收率分别为(100.66 ± 13.65)%和(115.69 ± 3.85)%, RSD均小于15 %, 见表 2。
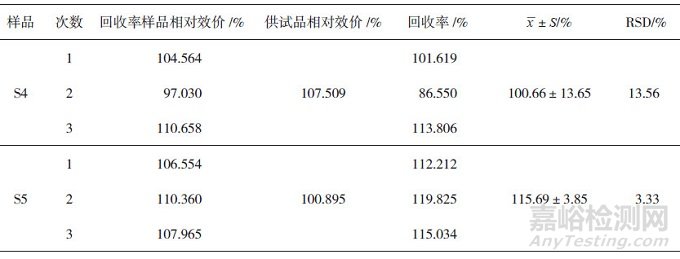
表 2 抗IL-17R单抗生物学活性准确性试验结果
3 讨论
治疗性单克隆抗体的生物学活性是其效应发挥的最关键条件, 也是评价其有效性的关键质量属性(Critical Quality Attribute, CQA)。以IL-17/IL17R为靶点的单抗药物, 因其在银屑病等自身免疫性疾病的疗效, 已成为近年来比较值得关注的新药之一。
目前, 抗IL-17/IL-17R单抗质量控制中的生物学活性测定方法有基于检测GROα、IL-6等细胞因子分泌的细胞酶免法、基于转基因细胞技术的活性检测方法以及基于AlphaLISA技术的活性检测方法。而AlphaLISA方法已经成为继放射免疫、酶标免疫、化学发光、电化学发光之后的一种新型检测方法, 它集合了酶标记技术、放射标记技术和同位素标记技术的优点, 越来越受到各领域科研工作者的关注。AlphaLISA无需分离和洗涤步骤, 操作简便, 不同于FRET检测, 单线态氧的扩散距离可达到200 nm, 最大程度减少了供体/受体之间的距离和方向限制。因此, 可用于全长蛋白检测和使用抗体的夹心免疫测定等应用。
本试验利用IL-8的AlphaLISA检测方法, 将系列稀释的抗IL-17R单抗与IL-17A结合后培养过夜, 通过AlphaLISA方法对细胞培养上清中释放的IL-8进行定量检测, 通过四参数方程拟合, 测得抗IL-17R单抗EC50, EC50值越低, 活性越高, 通过参比品与供试品EC50值的比较, 计算供试品的相对效价。抗IL-17R单抗经1:2.5倍系列稀释后可以得到较好的反S型曲线, 6批抗IL-17R单抗经三次测定相对效价的平均值在84.93%~107.51%, RSD均小于15%。该方法基于药物作用机制(Mechanism of Assay, MOA), 操作简便易行、结果准确客观、重复性好。为同类治疗性抗体或相关制品的生物学活性质量控制奠定了一定基础。
参考文献
[1] ROUVIER E, LUCIANI MF, MATTEI MG, et al. CTLA-8, Cloned from an Activated T Cell, Bearing AU-Rich Messenger RNA Instability Sequences, and Homologous to a Herpesvirus Saimiri Gene[J]. J Immunol, 1993, 150(12): 5445-5456.
[2] GAFFEN SL. Structure and Signalling in the IL-17 Receptor Family[J]. Nat Rev Immunol, 2009, 9(8): 556-567. DOI:10.1038/nri2586
[3] YAO Z, FANSLOW WC, SELDIN MF, et al. Herpesvirus Saimiri Encodes a New Cytokine, IL-17, Which Binds to a Novel Cytokine Receptor[J]. Immunity, 1995, 3(6): 811-821. DOI:10.1016/1074-7613(95)90070-5
[4] AGGARWAL S, GURNEY AL. IL-17:Prototype Member of an Emerging Cytokine Family[J]. J Leukoc Biol, 2002, 71(1): 1-8.
[5] KOLLS JK, LINDEN A. Interleukin-17 Family Members and Inflammation[J]. Immunity, 2004, 21(4): 467-476. DOI:10.1016/j.immuni.2004.08.018
[6] ZHU S, QIAN Y. IL-17/IL-17 Receptor System in Autoimmune Disease:Mechanisms and Therapeutic Potential[J]. Clin Sci (Lond), 2012, 122(11): 487-511. DOI:10.1042/CS20110496
[7] TEUNISSEN MB, KOOMEN CW, WAAL MALEFYT RD, et al. Interleukin17 and Interferon-Gamma Synergize in the Enhancement of Proinflammatory Cytokine Production by Human Keratinocytes[J]. J Invest Dermatol, 1998, 111(4): 645-649. DOI:10.1046/j.1523-1747.1998.00347.x
[8] PUEL A, CYPOWYJ S, BUSTAMANTE J, et al. Chronic Mucocutaneous Candidiasis in Humans with Inborn Errors of Interleukin-17 Immunity[J]. Science, 2011, 332(6025): 65-68. DOI:10.1126/science.1200439
[9] MITRA A, RAYCHAUDHURI SK, RAYCHAUDHURI SP. IL-17 and IL-17R:an Auspicious Therapeutic Target for Psoriatic Disease[J]. Actas Dermosifiliog, 2014, 105 Suppl 1: 21-33.
[10] BEJARANO JJR, VALDECANTOS WC. Psoriasis as Autoinflammatory Disease[J]. Dermatologic Clinics, 2013, 31(3): 445-460. DOI:10.1016/j.det.2013.04.009
[11] PARISI R, SYMMONS DP, GRIFFITHS CE, et al. Global Epidemiology of Psoriasis:A Systematic Review of Incidence and Prevalence[J]. J Invest Dermatol, 2013, 133(2): 377-385. DOI:10.1038/jid.2012.339
[12] KRUEGER JG, BOWCOCK A. Psoriasis Pathophysiology:Current Concepts of Pathogenesis[J]. Ann Rheum Dis, 2005, 64 Suppl 2: ii30-36.
[13] MIOSSEC P, KOLLS JK. Targeting IL-17 and TH17 Cells in Chronic Inflammation[J]. Nat Rev Drug Discov, 2012, 11(10): 763-176. DOI:10.1038/nrd3794
[14] LYNDE CW, POULIN Y, VENDER R, et al. Interleukin 17A:Toward a New Understanding of Psoriasis Pathogenesis[J]. J Am Acad Dermatol, 2014, 71(1): 141-150.
[15] MEASE PJ, GENOVESE MC, GREENWALD MW, et al. Brodalumab, an Anti-IL17RA Monoclonal Antibody, in Psoriatic Arthritis[J]. N Engl J Med, 2014, 370(24): 2295-2306. DOI:10.1056/NEJMoa1315231
[16] EGLEN RM, REISINE T, ROBY P, et al. the Use of AlphaScreen Technology in HTS:Current Status[J]. Current Chemical Genomics, 2008, 1(undefined): 2-10.
[17] PFLUGER M, KAPUSCIK A, LUCAS R, et al. A Combined Impedance and Alphalisa-Based Approach to Identify Anti-Inflammatory and Barrier-Protective Compounds in Human Endothelium[J]. J Biomol Screen, 2013, 18(1): 67-74.
[18] TAO L, RAO C, WANG L. Development of a Method for Quality Control of Humanized Monoclonal Antibody Against Epithelial Growth Factor Receptor[J]. Chin J Biologicals, 2013, 26(1): 72-75.

来源:xml-data


