今日,中国器审发布了一份左心耳封堵器系统的医疗器械产品注册技术审评报告,从这份资料我们看一下左心耳闭合系统研发需要做哪些实验?
点击下载报告全文
产品中文名称:左心耳封堵器系统
产品管理类别:第三类
申请人名称:上海普实医疗器械科技有限公司
一、左心耳闭合系统产品概述
(一)左心耳闭合系统产品结构及组成
该产品由非预装左心耳封堵器及介入输送装置组成。左心耳封堵器由盖片、填塞柱、不锈钢套、聚酯阻流膜等组成;盖片和填塞柱由两个独立的镍钛丝网分别成型而成,两者通过中间钢套连接,填塞柱上带有倒钩。介入输送装置由装载器、扩张器、传送鞘管、推送杆及冲洗接头组成。环氧乙烷灭菌,一次性使用。
(二)左心耳闭合系统产品适用范围
左心耳封堵器系统适用于CHADS2评分≥1,且不适合长期使用华法林抗凝药物治疗的非瓣膜性房颤患者。
(三)左心耳闭合系统作用机理
经房间隔中隔穿刺,通过介入输送装置将左心耳封堵器输送至左心耳,并逐步释放,左心耳封堵器通过填塞柱及倒钩固定在左心耳中,盖片关闭左心耳的入口,从而阻断进入左心耳的血流。
二、左心耳闭合系统临床前研究摘要
(一)左心耳闭合系统产品性能研究
1.产品技术要求研究
技术要求研究项目如表2所示。
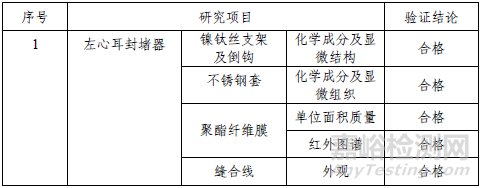
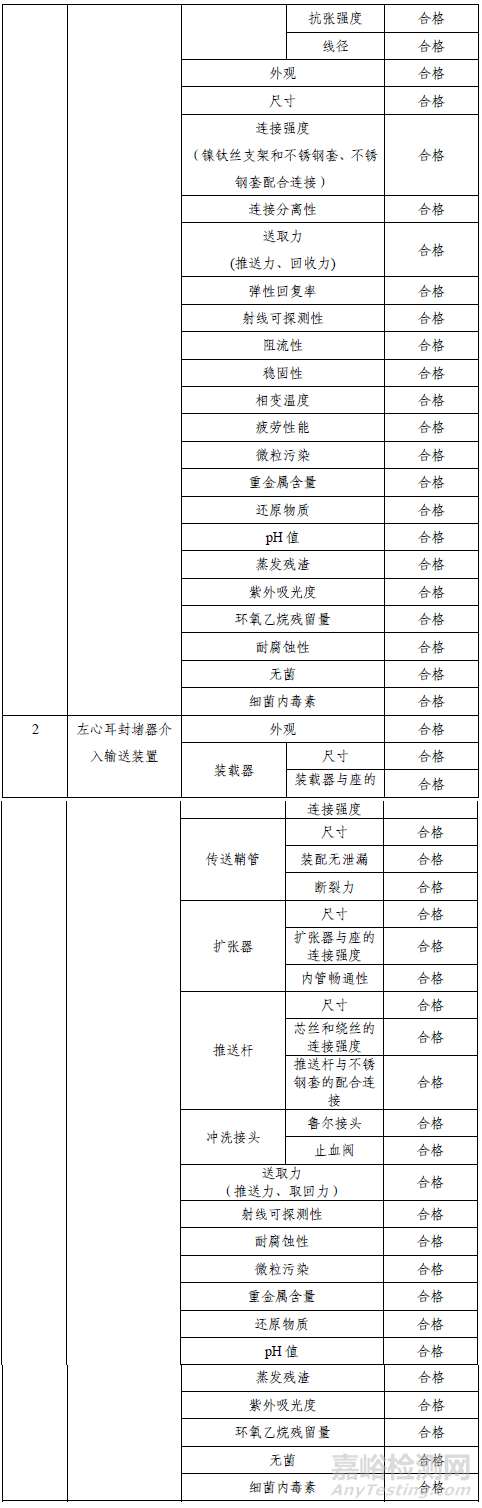
2.产品性能评价
产品性能评价包括左心耳封堵器的物理性能(外观、尺寸、连接强度、连接分离性、送取力、弹性回复率、射线可探测性)、化学性能(重金属含量、还原物质、PH值、蒸发残渣、紫外吸光度、环氧乙烷残留量、耐腐蚀性)、微生物性能(无菌、细菌内毒素)、左心耳封堵器MRI兼容性、左心耳封堵器疲劳性能、左心耳封堵器聚酯纤维膜缝合强度、左心耳封堵器径向支撑力及稳固性、倒钩的形变性能、左心耳封堵器微粒污染;左心耳封堵器介入输送装置传送鞘管头端与扩张器间隙、弯曲打折及扭转结合强度、止血性能、微粒污染、传送鞘管性能(尺寸、装配无泄漏、断裂力)、扩张器的性能(尺寸、扩张器与座连接强度、扩张器内管畅通性)、送取力(推送力、取回力)、推送杆和不锈钢套的配合连接、耐腐蚀性、外观化学性能(重金属含量、还原物质、PH值、蒸发残渣、紫外吸光度、环氧乙烷残留量、耐腐蚀性)、微生物性能(无菌、细菌内毒素);左心耳封堵器系统弯曲柔顺性、模拟使用性能。并对左心耳封堵器系统灭菌、成型热处理、钢套装配与焊接、传送鞘管和扩张器的弯曲成型等工艺进行了验证,结果表明产品符合设计输入的要求。
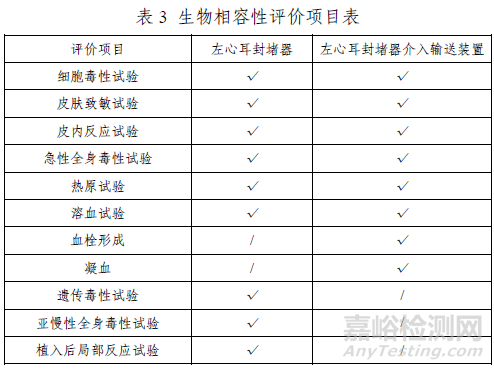
(二)生物相容性
左心耳封堵器系统包括左心耳封堵器和左心耳封堵器介入输送装置。其中,左心耳封堵器属于植入器械,与循环血液长期接触;左心耳封堵器介入输送装置属于外部接入器械,与循环血液短期接触。申请人按照GB/T 16886系列标准对植入器械及外部接入器械分别进行了生物学试验,产品的生物相容性风险可接受。具体评价项目详见表3。
(三)灭菌
该产品采用环氧乙烷灭菌,无菌状态提供。申请人提供了灭菌确认报告,证明无菌保证水平为10-6。环氧乙烷残留量不大于10氧乙烷残,2-氯乙醇残留水平不超过9mg/件。
(四)产品有效期和包装
该产品有效期为三年。申请人提供了货架有效期方案和报告。验证试验为加速老化和实时老化,包括产品外观、包装性能、产品使用性能、化学性能和微生物性能等。
(五)动物研究
申请人开展了犬模型的动物试验研究以验证产品可行性、安全性及有效性。封堵器植入后,通过封堵器稳定情况、残余分流情况、对周围器官的影响、推拉实验、封堵后观察等指标综合判断封堵器植入后效果。试验后存活犬随访时间分别为术后3天、1月、3月、6月。随访内容包括:一般状况、心电图检查及透视检查、经食道超声检查、大体标本观察(心脏标本大体观察和其他器官大体观察)、组织病理学检查和扫描电镜检查。动物实验结果表明,产品达到预期设计要求。