您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-04-30 08:08
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
康诺亚鼻炎单抗III期临床成功。康诺亚IL-4Rα抗体司普奇拜单抗(CM310)治疗季节性过敏性鼻炎(SAR)的III期临床达到主要终点。与安慰剂相比,司普奇拜单抗治疗患者2周后其rTNSS(每日回顾性鼻部症状总分)评分较基线变化的统计达到统计学显著改善,且安全性良好。去年年底,司普奇拜单抗治疗成人中重度特应性皮炎的上市申请已获CDE受理,并被纳入优先审评审批程序。
国内药讯
1.和黄结直肠癌新药上市获欧盟CHMP支持。和黄医药与武田联合开发的VEGFR抑制剂呋喹替尼(Fruzaqla)获欧洲药品管理局(EMA)人用药品委员会(CHMP)推荐批准上市,用于治疗转移性结直肠癌(mCRC)经治患者。在关键III期试验 (MRCT) FRESCO-2研究中,呋喹替尼治疗相比安慰剂使患者mOS延长2.6个月,mPFS延长1.9个月。此前,该新药已在中国和美国获批上市。
2.麓鹏淋巴瘤新药拟纳入突破性品种。麓鹏制药新一代BTK抑制剂LP-168片获CDE拟纳入突破性治疗品种,用于单药治疗既往接受过至少两线治疗的成人复发或难治性非生发中心B细胞型(non-GCB)弥漫性大B细胞淋巴瘤(DLBCL)。在治疗复发/难治性B细胞非霍奇金淋巴瘤患者的Ⅰ期研究中,LP-168的总体客观缓解率(ORR)为65.0%,其中在non-GCB DLBCL患者中的ORR达到70.0%。
3.恒瑞长效降糖复方启动III期临床。恒瑞长效胰岛素/GLP-1类似物固定比例复方制剂HR17031注射液登记启动一项III期临床(CTR20241529),拟在接受二甲双胍联合或不联合另一种口服降糖药治疗血糖控制不佳的2型糖尿病患者中,比较HR17031注射液与甘精胰岛素的有效性和安全性。该项研究由北京大学人民医院纪立农主任医师牵头开展。恒瑞目前正在中美同步HR17031的临床开发。
4.启德实体瘤ADC获批IND。启德医药靶向TROP2的下一代ADC新药GQ1010注射液获国家药监局临床试验许可,拟开发用于治疗晚期实体瘤患者。GQ1010是启德医药自主开发、采用其独特的酶促定点偶联技术iLDC,通过稳定的“开环”连接子将下一代喜树碱类似物和抗TROP2单克隆抗体偶联而成。去年4月,启德医药已将该新药除大中华区以外全球范围内开发和商业化权益授予Pyramid公司。
5.石药“合成致死”新药美国获批临床。石药集团宣布其小分子MAT2A抑制剂1类新药SYH2039已获得FDA临床许可,即将在美国针对晚期恶性肿瘤开展新药研究。临床前研究显示,SYH2039可有效抑制非小细胞肺癌、胶质瘤、胃食管癌、胰腺癌和膀胱癌等多种MTAP缺失型肿瘤细胞的生长,并具有良好的安全性。今年3月,该产品已在中国获批临床。
6.波睿达实体瘤CAR-T获批临床。波睿达生物自主研发的抗CD99 CAR-T细胞产品BRD-03获国家药监局临床试验默示许可,拟开发用于≥18周岁的复发/难治性CD99+骨或软组织肉瘤。临床前研究显示,BRD-03对横纹肌肉瘤肿瘤细胞系等小鼠模型均有显著的抑瘤效果及较好的耐受性。该产品在研究者发起的临床试验(IIT)中也取得积极的安全性与有效性的结果。
国际药讯
1.诺华PI3Kα抑制剂获批新剂型。诺华PI3Kα抑制剂Vijoice(alpelisib)口服颗粒剂型获FDA批准上市,用于治疗需要接受系统治疗的PIK3CA相关过度生长病谱(PROS)成人和2岁及以上儿童患者。2022年4月,FDA已批准Vijoice片剂用于上述适应症。值得一提的是,Alpelisib是FDA批准的首款用于针对PIK3CA突变的HR+/HER2-晚期乳腺癌的PI3K抑制剂,最早于2019年5月获得FDA批准,商品名为Piqray。
2.艾伯维皮炎新药头对头临床成功。艾伯维JAK1抑制剂Rinvoq(乌帕替尼)治疗中重度特应性皮炎(AD)患者的头对头IIIb/IIII期LEVEL UP研究达到主要终点和次要终点。与度普利尤单抗相比,乌帕替尼治疗第16周患者达到严重程度指数评分较基线至少改善90%(EASI 90)和最严重瘙痒数字评定量表(WP-NRS)评分0/1(完全或几乎完全瘙痒消退)的患者比例显著更多(19.9%vs8.9%,p<0.0001);研究中未观察到新的安全信号。
3.AZ/第一三共ADC乳腺癌III期临床积极。第一三共与阿斯利康开发的HER2靶向抗体偶联药物(ADC)Enhertu(德曲妥珠单抗)在治疗HR+、HER2低表达(IHC 1+或2+/ISH-)的转移性乳腺癌患者的III期DESTINY-Breast06研究达到主要终点。与研究者选择的化疗相比,Enhertu治疗显著改善患者的无进展生存期(PFS),总生存期(OS)数据也显示改善趋势。详细数据将在医学会议上公布。
4.AriBio公司AD新药获批III期临床。AriBio公司PDE5抑制剂AR1001获欧洲药品管理局(EMA)批准开展针对早期阿尔茨海默病(AD)的III期临床(POLARIS-AD)。AR1001旨在通过抑制神经元凋亡和恢复突触可塑性,以保护神经和缓解AD病程。在Ⅱ期研究中,接受AR1001(10mg和30mg)治疗的轻度AD患者52周后其ADCS-CGIC(AD临床总体印象变化量表)评分较基线分别下降了2.4分(15.1%)和8.7分(46.3%,P=0.001)。
5.精神运动障碍鼻喷剂Ⅱ期临床积极。Vistagen公司基于鼻-脑作用机制开发的pherine鼻喷剂PH15在治疗因精神疲劳引起的精神运动障碍的Ⅱa期临床中获积极结果。Pherine旨在激活鼻部化学感受器,将信号通过神经回路传送到特定的大脑区域。在所有测试时间节点,接受PH15治疗患者的平均反应时间均快于安慰剂鼻喷剂(p<0.001)和口服咖啡因(p<0.001),而且药物耐受性良好。
6.度普利尤单抗Q1大卖31亿美元。赛诺菲发布2024年Q1财报报表,公司营收104.64亿欧元(约113.99亿美元),同比增长6.7%;其中制药业务收入77.62亿欧元(约84.56亿美元,+6.4%),疫苗业务收入11.77亿欧元(约12.82亿美元,+5.6%);研发支出约17.19亿欧元(约18.73亿美元,+11.8%)。2024年一季度,赛诺菲自免管线中的度普利尤单抗(Dupixent)销售额达28.35亿欧元(约30.88亿美元),同比增长25%。
医药热点
1.上海拟建立“儿童孤独症诊断中心”。为进一步推进0~6岁儿童孤独症筛查、诊断和干预工作,完善0~6岁儿童孤独症筛查、诊断和干预康复服务体系,对筛查异常儿童及时进行诊断评估和干预指导,改善儿童症状和预后,上海市卫健委经公开遴选和组织专家评审,决定在复旦大学附属儿科医院、上海交通大学医学院附属上海儿童医学中心、上海交通大学医学院附属新华医院、上海市儿童医院、上海市精神卫生中心和上海市妇幼保健中心建立“上海市儿童孤独症诊断中心”。
2.亚洲首个15T转化医学影像平台落地华西医院。4月26日,15T转化医学影像中心宣布成立,标志着亚洲首个15T转化医学影像平台落地四川大学华西医院。15T转化医学影像平台包括7T超高场磁共振、5T超极化仪以及3T高场磁共振,作为转化医学国家重大科技基础设施(四川)精准成像核心功能平台,将主要用于基础研究和临床研究,以此探究疾病的结构、功能及代谢等多方位信息,为转化医学提供更多疾病探索的可能,助力精准治疗。
3.韩国医协新任会长要求政府取消扩招计划。据韩联社报道,大韩医师协会会长当选人林贤泽28日在医协定期代议员大会上表示,韩国政府应当从头讨论2000人扩招计划和必需医疗改革政策,韩国政府若不取消医学院扩招计划,医疗界将不会出面进行任何协商。据报道,虽然韩国政府日前允许32所扩招对象院校在原定新增名额的50%至100%范围内,自主调整扩招规模,但医疗界表示反对。
评审动态
1. CDE新药受理情况(04月29日)
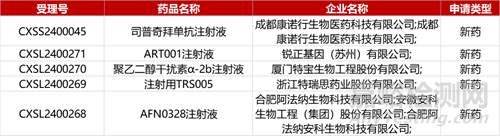
2. FDA新药获批情况(北美04月26日)
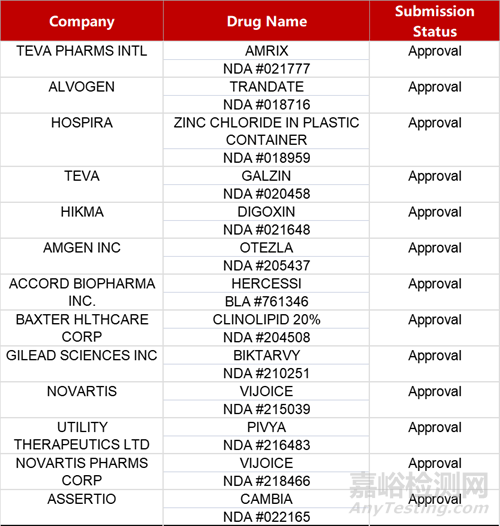

来源:药研发


