液相色谱柱的性能主要取决于填料的性质和类型。填料的大小、形状、键合相、含碳量等均能影响液相色谱柱的性能,这对我们使用及选择色谱柱都是非常有帮助的。今天我们一起看看填料是如何影响HILIC色谱柱的性能的呢?
水色谱HILIC(Hydrophilic Interaction Liquid Chromatography) 是一种用来改善在反相色谱中保留较差的强极性物质保留行为的色谱技术。它通过采用强极性固定性,并且结合高比例有机相/低比例水相组成的流动相来实现这一目的,但本质上是可以使用反相流动相的正相色谱。
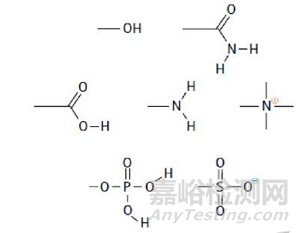
HILIC模式色谱柱综合了液液分配、离子交换和氢键作用:极性分子首先在主体流动相与色谱填料表面的半固定的高极性水膜之间发生液液分配;次级保留作用包括色谱填料表面硅醇基和/或极性官能团与带电分析物发生的离子交换作用;氢键作用发生在带正电的分析物与带负电的表面硅醇基之间。因此, HILIC模式色谱柱适用于含如下图所示官能团的物质。
目前HILIC技术已经越来越多的被用做HPLC方法开发策略的一部分, 作为传统反相色谱技术的补充,不仅可以保留高极性化合物,还能够提供巨大的选择性差异,获得与反相分离时完全相反的洗脱顺序。因此,HILIC模式色谱柱广泛应用在有机酸 、多巴胺、组胺、嘧啶及水溶性维生素等极性物质的分离中。液相液相色谱柱的性能主要取决于填料的性质和类型。填料的大小、形状、键合相、含碳量等均能影响液相色谱柱的性能,这对我们使用及选择色谱柱都是非常有帮助的。
色谱柱填料类型
常见的液相色谱柱填料有 C1、C3、C4、C8、C18、C30、氨基、氰基、硅胶色谱柱等。常见色谱柱中的填料分类:
1、反相(与离子对)方法
C18(十八烷基或ODS):普适性好;保留性强,用途广
C8(辛基):与C18相似,但保留值稍小
C3,C4:保留值小;大多用于肽类与蛋白质
C1【三甲基硅烷(TMS)】:保留值最小;最不稳定
苯基,苯乙基:保留值适中;选择性有所不同
CN(氰基):保留值适中;正相和反相均可使用
NH2(氨基):保留性弱;用于烃类;欠稳定
聚苯乙烯基b:在1<PH<13的流动相中稳定;对某些分 离峰形好,柱子寿命长
2、正相方法
CN(氰基):普适性好;极性适中;用途广
OH(二醇基):极性大于CN
NH2(氨基):极性大,欠稳定
硅胶b:普适性好;价廉;操作欠方便;用于制备LC
3、空间排阻方法
硅胶b:普适性极好;作吸附剂用
硅烷化硅胶:吸附性弱,溶剂兼容性好;适用于有机溶剂
OH(二醇基):欠稳定;在水SEC中使用(凝胶过滤)
聚苯乙烯基b:广泛用于有机SEC(凝胶渗透);一般与水和极性大的有机溶剂不相容
4、离子交换方法
键合相:稳定性与重现性均不好
聚苯乙烯基b:柱效不高;稳定;重现性好
填料对液相色谱柱性能的影响
1、粒径的影响
液相色谱柱填料的平均粒径越小,涡流扩散越小,传质越好,柱效越高,然而,填料粒径小,导致渗透性能变差,柱压较高。同时,填料粒径分布越宽,渗透性能越差,色谱柱柱效越低。常见的填料粒径有 3μm、3.5μm、5μm、10μm 等。
2、形状的影响
液相色谱柱的填料分为无定型和球型。无定型填料制备的液相色谱柱柱床结构不均匀,流动相线性速度不均匀,色谱图的峰形较宽;球型填料制备的液相色谱柱柱床结构均匀,因此色谱柱柱效高、重现性好。球型填料是目前最为常见的液相色谱柱填料,这种填料具有更好的性能和重现性。
3、键合相的影响
以硅胶为基质,通过化学键合的方式把 C18、C8、氨基、氰基等基团键合在基质上, 作为液相色谱柱中的填料。通过键合不同的化学基团,得到不同性能的液相色谱柱。由于不同键合基团的分离机理不同,从而影响化合物的保留与分离。
填料的键合使得液相色谱柱的固定相相对较为稳定,不易流失,同时很大程度上消除了硅羟基的不良影响,可适用于多种流动相中,应用广泛。然而,键合后的填料耐酸性较差,pH 值不能小于 2,当流动相 pH 超出酸性范围时,键合相易流失,耐用性和稳定性会变差。
4、端基封口的影响
硅胶因具有特殊的表面化学特性,被广泛用作液相色谱柱填料基质材料。硅胶表面具有硅羟基,硅羟基的密度、分布、及其化学特性对各种类型的色谱行为都会产生不同程度的影响。
在使用以硅胶为基质的高效液相色谱柱特别是在反相色谱柱时,经常会遇到因游离的硅羟基(或称为硅醇基)而导致的非特异性吸附。对一些极性较强的溶质,如碱性物质, 色谱峰会严重拖尾,甚至会因强吸附而不能洗脱。通常采用封尾的方式减少硅羟基的影响, 具体做法是将填料与小硅烷(如三甲基氯硅烷)进行后续反应,反应掉部分残余硅羟基, 以增加表面覆盖率。采用该方式不仅可以减少不可逆吸附或拖尾,还能增加碳含量。但是, 该方式并不能完全反应掉残余的硅羟基,仍有 50%的硅羟基未被反应。
5、含碳量的影响
液相色谱柱填料,特别是反相填料的含碳量,常被用于表征表面化学修饰程度。通常通过键合作用将碳链引入到填料中,填料含碳量越高,说明碳链密度越高,碳链越长,容量因子越大,疏水性越强。在反相条件中,碳链增长,意味着填料具有更大的比表面积, 缔合作用增强,待测物质保留增加。因此,高含碳量填料的液相色谱柱稳定性好,重复性好,有利于保留效果差的化合物的分离,可以改善极性化合物的拖尾;低碳量填料的液相色谱柱有利于分析中性及碱性化合物,可以降低溶剂损耗。
6、其他因素的影响
除上述情况外,硅胶填料的活性、杂质含量、pH 稳定性、热稳定性等也会影响液相色谱柱性能。
生产硅胶时,处理温度不同,硅胶活性也不同。硅胶的活性是选择性差异的主要来源, 主要影响碱性化合物的保留行为;硅胶的杂质含量是色谱柱质量好坏的重要标志,重金属含量低,硅羟基活性小,拖尾减小。
HILIC色谱柱的使用注意事项
1、HILIC色谱柱的平衡
使用50倍柱体积的50/50的乙腈/水相缓冲溶液(缓冲液的最终浓度为10mM)平衡新色谱柱。
在开始进样前,用20倍柱体积的起始流动相平衡色谱柱。
进行梯度分析时,进样间隔需要用10倍柱体积起始流动相平衡色谱柱,色谱柱平衡不充分将导致保留时间漂移。
2、HILIC流动相需要注意的问题
流动相中总是至少保持5%的极性溶剂(如5%水相缓冲液,5%甲醇或3%甲醇+2%水相缓冲液等),保证HILIC硅胶填料始终被水浸润。
在流动相或梯度中至少保持有机溶剂(如乙腈)的比例不低于40%。
不要使用磷酸盐缓冲溶液体系,因为磷酸盐缓冲液在HILIC色谱模式下会析出;使用磷酸则没有问题。
甲酸铵或乙酸铵水溶液缓冲系统比甲酸或乙酸的水溶液重现性更好。如果不能使用缓冲液而一定要使用流动相添加剂如甲酸,最好使用0.2%的浓度而非0.1%。
为得到最好的峰形,在流动相或梯度中总是保持缓冲系统的浓度为10mM。
3、HILIC稀释剂需要注意的问题
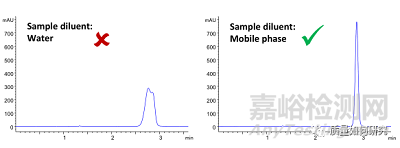
如果可能,尽量用100%乙腈溶解样品进样。避免使用水配制样品溶液,请选择较弱的HILIC溶剂,如乙腈、甲醇、异丙醇等配制样品溶液。
最常用的稀释剂为75/25乙腈/甲醇,这个体系充分平衡了样品的溶解度和峰形两个因素。
不要用水或DMSO做稀释剂,它们将导致峰形变得很差。
使用反相SPE技术将水或DMSO置换成乙腈再进样。如果不能这样操作,用有机溶剂稀释水或 DMSO。
4、其它有关使用HILIC的建议
开始时可以运行一个95%乙腈至50%乙腈的梯度,如果样品不保留,使用95/3/2的乙腈/甲醇/水相缓冲溶液的流动相进行等度分析。
将流动相中的水换成甲醇、丙酮或异丙醇也可以增加极性化合物的保留。
请确保洗针溶剂/冲洗溶剂包含和流动相一样的高比例有机相,否则峰形会受到影响。
5、色谱柱清洗、再生和保存
(1)清洗和再生。压力骤然升高,保留时间或分离度发生波动往往表明色谱柱被污染了。可根据如下操作清洗色谱柱。
用50/50的乙腈/水清洗以去除极性污染物。如果清洗无效,可用5:95的乙腈/水清洗色谱柱。
如果系统压力上升至超过设定的压力限或者突然出现色谱峰分叉,通常是需要更换保护柱的信号。
(2)色谱柱的保存。如果较长时间内不使用色谱柱,请将柱子保存在95%乙腈中;不要将色谱柱保存在缓冲盐流动相中,如果流动相中含有缓冲盐,先用10倍柱体积的HPLC级水清洗色谱柱然后换上95%乙腈保存。如果中间不用水“过渡”清洗有可能在使用95%乙腈时造成盐析出。