您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2025-08-29 21:50
摘 要: 建立了高效液相色谱法同时检测化妆品中迪高替尼、托法替尼、乌帕替尼、鲁索替尼4种组分。样品用体积分数为80%的甲醇溶液提取,C18色谱柱分离,二极管阵列检测器检测,检测波长为225 nm。4种组分在各自质量浓度范围内与对应的色谱峰面积线性关系良好,相关系数均为0.999 9;4种组分的检出限为2.48~2.83 μg/g;霜类、乳液类、水剂类3种化妆品基质下,方法回收率为92.6%~100.6%,测定结果相对标准偏差为0.2%~4.1%(n=6)。该方法操作简便、准确快速,适用于化妆品中迪高替尼等4种组分的含量测定。
关键词: 高效液相色谱法; 化妆品; 迪高替尼; 托法替尼; 乌帕替尼; 鲁索替尼
特应性皮炎(AD)是皮肤科常见疾病之一,是一种慢性炎症性皮肤病,临床上以皮肤瘙痒、复发性湿疹样皮疹为特点,儿童患病率大,严重影响患者及其家庭的生活质量[1‒2]。目前,AD的病因尚不完全明确,但有文献报道Janus激酶抑制剂(JAKi)通过阻断Janus激酶的信号通路,抑制Ⅱ型细胞因子而对AD的治疗有一定效果[3‒5]。近年来,多种JAKi获批用于治疗AD,其中乌帕替尼、迪高替尼、鲁索替尼和托法替尼是目前临床最为常用或是最具潜力的Janus激酶抑制剂[6‒14]。《化妆品监督管理条例》第五十九条第三项规定,不得使用禁止用于化妆品生产的原料生产化妆品,不得在化妆品中添加可能危害人体健康的物质。上述几种JAKi类药物,由于其良好的治疗AD效果,有被不法化妆品生产企业违规加入儿童类化妆品或是宣称具有舒缓、修护功效化妆品中的风险。但查阅相关文献,目前尚未有可以检测化妆中迪高替尼等4种组分的方法,使此类风险的监管尚处于空白,给消费者用妆安全带来隐患。笔者建立了可快速、高效地在化妆品中同时检测迪高替尼、托法替尼、乌帕替尼、鲁索替尼4种组分的高效液相色谱检测法。
1 实验部分
1.1 主要仪器与试剂
高效液相色谱仪:岛津LC-20AD型,配有SIL-20AC自动进样器、DGU-20 A在线真空脱气机、CTO-20A柱温箱、SPD-M40二极管阵列检测器,日本岛津仪器公司。
电子分析天平:METTLER TOLEDO XS205DU型,感量为0.01 mg,瑞士梅特勒-托利多公司。
涡旋震荡器:IKA MS3型,德国爱卡公司。
超声波清洗仪:PRIMA PM5-2000TD型,英国普律玛仪器公司。
离心机:赛默飞X1R型,美国赛默飞世尔科技公司。
超纯水发生器:Millipore Milli Q Reference型,美国密理博公司。
迪高替尼、托法替尼、鲁索替尼标准品:纯度(质量分数)分别为99.9%、98.3%、99.9%,上海安谱实验科技股份有限公司。
乌帕替尼标准品:纯度(质量分数)为99%,上海麦克林生化科技股份有限公司。
甲醇:色谱纯,德国默克公司。
1.2 溶液配制
标准储备溶液:分别精密称取迪高替尼、托法替尼、乌帕替尼、鲁索替尼4种标准品约0.01 g (精确至0.000 1 g)于4只10 mL容量瓶中,用甲醇溶解并定容至标线,摇匀,于-4 ℃下保存。
混合标准溶液:分别精密移取4种标准储备溶液各1 mL于同一10 mL容量瓶中,用80%(体积分数,下同)甲醇溶液稀释至标线,得4种标准品质量浓度均为100 μg/mL的混合标准溶液。
系列混合标准工作溶液:精密移取一定量的4种组分的混合标准溶液,用80%甲醇溶液逐级稀释,得到4种组分质量浓度均分别为0.5、1、2、5、10、25、50 μg/mL的系列混合标准工作溶液。
1.3 液相色谱条件
色谱柱:CAPCELL PAK TYPE MG柱 (250 mm×4.6 mm,5 μm,厂家);柱温:40 ℃;进样体积:10 μL;检测波长:225 nm;流动相:A相为水,B相为甲醇;流量:1.0 mL/min;洗脱方式:梯度洗脱,洗脱条件见表1。
表1 梯度洗脱条件
Tab. 1 Gradient elution program
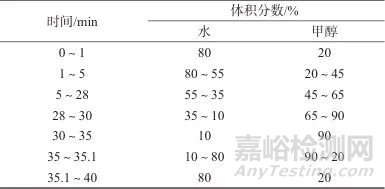
1.4 样品处理
精密称取0.5 g样品(精确至0.000 1 g)于10 mL具塞比色管中,加入80%甲醇溶液8 mL,用涡旋震荡器混匀,超声提取20 min,后用80%甲醇溶液定容至10 mL,必要时于10 000 r/min转速下离心10 min,取上清液经0.45 μm滤膜过滤,滤液作为样品溶液。
1.5 样品测定
在1.3液相色谱条件下,取系列混合标准工作溶液分别进样,进行色谱分析,以系列混合标准工作溶液质量浓度为横坐标,对应的色谱峰面积为纵坐标,绘制标准曲线。取样品溶液进样,测得色谱峰面积,根据标准工作曲线得到样品溶液中迪高替尼等4种组分的质量浓度。
2 结果与讨论
2.1 液相色谱条件的选择
比较了水-乙腈和水-甲醇为流动相[15]时4种组分的分离效果,结果表明,两种流动相体系下4种组分均能有效分离且色谱峰形较好,但水-乙腈体系下保留时间较短,不利于后期样品检测,水-甲醇体系下保留时间合适且分离度好,故选择水-甲醇作为流动相体系。甲醇作为有机相时,分别试验了10、20 mmol/L乙酸铵缓冲盐溶液对4种组分分离效果的影响。结果发现,水-甲醇体系下各组分峰形已经较好,添加缓冲盐并未使峰形更好。综上所述,选择水-甲醇作为流动相。
2.2 色谱柱温度的选择
比较柱温分别为25、30、35、40 ℃时4种组分的分离效果。结果显示,4种柱温条件下4种组分均能得到有效分离,但随着柱温降低保留时间有所延长,综合考虑,选择柱温为40 ℃。
2.3 检测波长的选择
采用二极管阵列检测器对4种组分进行全波长扫描,扫描范围为190~400 nm,结果如图1所示。由图1可见,迪高替尼在284 nm波长处有最大吸收,托法替尼在286 nm波长处有最大吸收,乌帕替尼在232 nm、340 nm处有最大吸收,鲁索替尼在252 nm、310 nm处有最大吸收,4种组分在短波长区域都有较大的紫外吸收,为了方便试验操作,统筹考虑,选择225 nm作为迪高替尼、托法替尼、乌帕替尼、鲁索替尼等4种组分的检测波长。
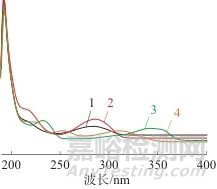
1—迪高替尼;2—托法替尼; 3—乌帕替尼; 4—鲁索替尼图1
4种组分的紫外吸收光谱图
Fig. 1 UV absorption spectrum of 4 components
2.4 提取溶剂的选择
根据前述流动相的种类以及4种组分均较易溶于甲醇的特性,考察了不同体积分数(100%、80%、60%、40%)甲醇溶液作为提取溶剂时样品的提取效果。结果发现,当甲醇体积分数为40%时,4种组分的提取回收率较低,为65%~80%;随着甲醇体积分数的增加,4种组分的提取回收率均有不同程度的增加,当甲醇体积分数为80%和100%时,4种组分的提取回收率无明显差异。综合考虑,采用体积分数为80%的甲醇溶液作为提取溶剂。
2.5 专属性试验
按1.3条件分别测定迪高替尼等4种组分混合标准溶液、空白样品溶液、加标样品溶液,色谱图分别见图2~图4。由图可见,4种组分峰形和分离度均表现良好,样品溶液基质对4种组分的测定无干扰,加标样品溶液与混合标准溶液中4种组分的保留时间一致,表明该方法具有良好的专属性。
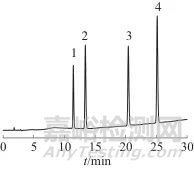
1—迪高替尼;2—托法替尼; 3—乌帕替尼; 4—鲁索替尼
图2 混合标准溶液色谱图
Fig. 2 Chromatograms of mixed standard solution
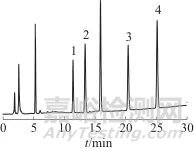
1—迪高替尼;2—托法替尼; 3—乌帕替尼; 4—鲁索替尼
图4 加标样品溶液色谱图
Fig. 4 Chromatograms of spiked sample solution
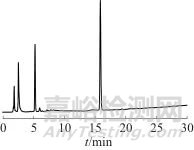
图3 空白样品溶液色谱图
Fig. 3 Chromatograms of blank sample solution
2.6 线性回归方程
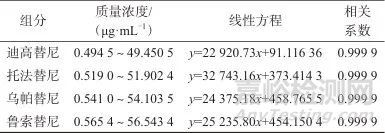
取系列混合标准工作溶液在1.3液相色谱条件下进行测定,以各组分的质量浓度为横坐标,对应色谱峰面积为纵坐标进行线性回归,得到回归方程。4种组分在对应的质量浓度范围内与色谱峰面积线性关系良好,相关系数均为0.999 9,结果如表2所示。
表2 4种组分的线性范围、线性回归方程和相关系数
Tab. 2 Linear range,linear equation and correlation coefficient of 4 components
2.7 检出限和定量限
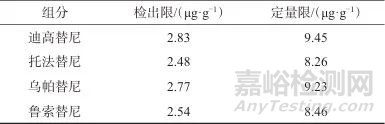
取较低质量浓度的混合标准工作溶液,稀释进样,记录信噪比(S/N),按S/N为3和10的标准,计算检出限和定量限,结果如表3所示。
表3 4种组分的检出限、定量限
Tab. 3 Detection limit and quantification limit of 4 components
2.8 样品加标回收试验
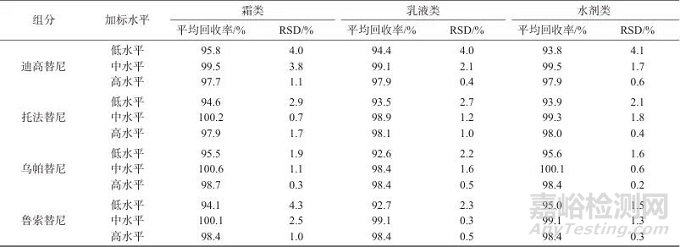
选取霜类、乳液类、水剂类3类化妆品常见剂型进行加标回收试验。称取3类空白样品各0.5 g,分别加入50、100、500 μL混合标准溶液,制得低、中、高3个浓度水平的加标样品,每个浓度水平平行制备6份,按1.4样品处理进行操作,得到样品溶液并测得其中的迪高替尼等4种组分的质量浓度,计算各组分回收率和测定结果的相对标准偏差(RSD),结果见表4。4种组分在3类基质下的平均回收率为92.6%~100.6%,RSD为0.2%~4.1%(n=6)。结果表明,该方法在霜类、乳液类、水剂类3类基质中的准确度和精密度均良好。
表4 样品加标回收试验结果
Tab. 4 Results of recovery test of spiked samples
3 结语
建立了同时测定迪高替尼等4种治疗特应性皮炎组分的高效液相色谱法,该方法操作简单,标准曲线线性关系、准确度和精密度良好,为检测化妆品中迪高替尼、托法替尼、乌帕替尼、鲁索替尼等治疗特应性皮炎药物提供了新的方法。该方法的建立有效补充了化妆品非法添加的检测范围,为监管部门的科学监管监测提供技术支撑。
参考文献
1 中华医学会皮肤性病学分会免疫学组,特应性皮炎协作研究中心.中国特应性皮炎诊疗指南(2020版)[J].中华皮肤科杂志,2020,53(2): 81.
Atopic Dermatitis Working Group,Immunology Group,Chinese Society of Dermatology. Chinese guideline for diagnosis and treatment of atopic dermatitis (2020)[J]. Chinese Journal of Dermatology,2020,53(2): 81.
2 王建琴.中国特应性皮炎诊疗指南(2020版)解读[J].皮肤性病诊疗学杂志,2020,27(5): 359.
WANG Jianqin. Interpretation of Chinese guidelines for the diagnosis and treatment of atopic dermatitis(2020)[J]. Journal of Diagnosis and Therapy on Dermato-Venereology,2020,27(5): 359.
3 SCHULER C F 4th,BILLI A C,MAVERAKIS E,et al. Novel insights into atopic dermatitis[J]. The Journal of Allergy and Clinical Immunology,2023,151(5): 1 145.
4 NAKASHIMA C,YANAGIHARA S,OTSUKA A. Innovation in the treatment of atopic dermatitis:Emerging topical and oral Janus kinase inhibitors[J]. Allergology International,2022,71(1): 40.
5 李妍,李明.系统Janus激酶抑制剂治疗特应性皮炎专家共识[J].实用皮肤病学杂志,2022,15(3): 129.
LI Yan,LI Ming. Expert consensus on the treatment of atopic dermatitis with systemic Janus kinase inhibitors[J]. Journal of Practical Dermatology,2022,15(3): 129.
6 LEVY L L,URBAN J,KING B A. Treatment of recalcitrant atopic dermatitis with the oral Janus kinase inhibitor tofacitinib citrate[J]. Journal of the American Academy of Dermatology,2015,73(3): 395.
7 BLAUVELT A,TEIXEIRA H D,SIMPSON E L,et al. Efficacy and safety of upadacitinib vs dupilumab in adults with moderate-to-severe atopic dermatitis:A randomized clinical trial[J]. JAMA Dermatology,2021,157(9): 1 047.
8 刘艳,田晶,梁源,等.儿童特应性皮炎的新药治疗进展[J].中国新药杂志,2023,32(19): 1 959.
LIU Yan,TIAN Jing,LIANG Yuan,et al. New advancement on the therapy of pediatric atopic dermatitis[J]. Chinese Journal of New Drugs,2023,32(19): 1 959.
9 殷科蕊,吴紫阳,汪皖青,等. 3种口服Janus激酶抑制剂治疗特应性皮炎的临床综合评价[J].中国药房,2024,35(12): 1 419.
YIN Kerui,WU Ziyang,WANG Wanqing,et al. Clinical comprehensive evaluation of three oral Janus kinase inhibitors for atopic dermatitis[J]. China Pharmacy,2024,35(12): 1 419.
10 庄昊俊,郭美亮,刘婉雯,等. Janus激酶抑制剂在特应性皮炎治疗中的临床应用研究进展[J].上海交通大学学报(医学版),2021,41(7): 963.
ZHUANG Haojun,GUO Meiliang,LIU Wanwen,et al. Clinical research progress of Janus kinase inhibitors in the treatment of atopic dermatitis[J]. Journal of Shanghai Jiao Tong University (Medical Science),2021,41(7): 963.
11 韩京宏,刘红. Janus激酶抑制剂治疗儿童难治性特应性皮炎二例[J].中国麻风皮肤病杂志,2024,40(3): 190.
HAN Jinghong,LIU Hong. Two children with refractory atopic dermatitis successfully treated with Janus kinase inhibitors[J]. China Journal of Leprosy and Skin Diseases,2024,40(3): 190.
12 李娜,衡明莉,王骏.治疗特应性皮炎新药及其临床药理学研究有关问题探讨[J].药物评价研究,2022,45(9): 1 894.
LI Na,HENG Mingli,WANG Jun. Discussion on new drugs and clinical pharmacology studies for atopic dermatitis[J]. Drug Evaluation Research,2022,45(9): 1 894.
13 何石焕,刘京平.乌帕替尼治疗特应性皮炎的研究进展[J].现代医药卫生,2022,38(20): 3 508.
HE Shihuan,LIU Jingping. Research progress on the treatment of atopic dermatitis with upadacitinib[J]. Journal of Modern Medicine and Health,2022,38(20): 3 508.
14 KATOH N,IKEDA M,OHYA Y,et al. Safety and efficacy of upadacitinib for atopic dermatitis in Japan:Analysis of the 3-year phase 3 rising up study[J]. Dermatology and Therapy,2024,14(1): 213.
15 沈红梅,秦明明. HPLC法测定原料药磷酸芦可替尼的含量和有关物质[J].广州化工,2021,49(2): 66.
SHEN Hongmei,QIN Mingming. Determination of related substances in ruxolitinib phosphate by HPLC[J]. Guangzhou Chemical Industry,2021,49(2): 66.

来源:化学分析计量


