近日,MDCG对MDCG 2024-14 关于实施隐形眼镜主UDI-DI解决方案的指南进行了更新,更新内容如下:
1.引言及范围
MDR Art.27中提到UDI系统的引入旨在确保医疗器械具有足够水平的识别和可追溯性。制造商在将除定制器械外的所有器械投放市场前须为其分配基本UDI-DI、UDI-DI以及UDI-PI,并在Eudamed中注册基本UDI-DI和UDI-DI。对于呈现高度个性化水平的隐形眼镜(高度个性化器械),MDR Annex VI C部分第6.6.1节规定了主UDI-DI的分配(分别由EU 2023/2197、EU2025/788进行了两轮修订)。
本指南就隐形眼镜主UDI-DI规则的结构、分配、标签和在Eudamed中的注册实施提供指导。
2术语
标准隐形眼镜(包括标准软性隐形眼镜和硬性透气性(RGP)隐形眼镜):即批量生产的隐形眼镜,通常由制造商/分销商/眼科护理专业人员持有库存,且参数范围有限。例如:标准软性日抛型隐形眼镜。
定制式隐形眼镜(软性或硬性):根据特定个人订单进行生产,镜片具有广泛的参数范围。例如:车床切割的按订单生产的季抛镜片。
隐形眼镜设计参数:用于向使用者、眼科护理专业人员以及其他利益相关者标识临床尺寸的隐形眼镜参数。例如:基弧、直径、加光度、轴位……
基本UDI-DI:用于连接具有相同预期用途、风险等级、基本设计和制造特性的器械的标识符。对于隐形眼镜,触发基本UDI-DI分配的参数可包括如材料、滤光片、着色、镜片类型等。
主UDI-DI:用于针对某些高度个性化器械进行分组的唯一标识符。此类高度个性化器械在预定义的临床相关参数方面具有特定的相似性,例如:应为具有相同隐形眼镜设计参数组合(至少包括基弧和直径)的隐形眼镜分配的单一的主UDI-DI。主UDI-DI应与一个基本UDI-DI相关联。
UDI-PI:包括序列号、批号、软件标识以及生产日期或有效期或两种日期,适用于隐形眼镜。
3主UDI-DI
由于隐形眼镜具有众多临床参数特征,存在多种变体。若根据MDR要求,为每种隐形眼镜变体都分配独立的UDI-DI,则会导致在UDI-DI层面的个体化分配导致相似隐形眼镜的UDI-DI数量激增,不仅使Eudamed超负荷运行,也与隐形眼镜相关的安全风险程度不成比例。因此,欧盟医疗器械主管机构根据当前技术表明:将具有相同临床和设计参数组合的隐形眼镜归组到同一UDI-DI(主UDI-DI)下。以下为示例图:
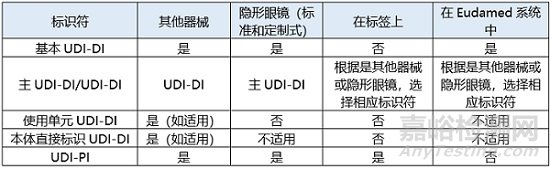
同时,对向隐形眼镜和其他器械分配UDI-DI所提供的不同器械标识符和标识级别进行比较:
标准隐形眼镜主UDI-DI分配
标准隐形眼镜的主UDI-DI将分配给制造商定义的特定隐形眼镜设计参数组合,至少包括基弧和直径,并辅以标签上向最终用户、眼科护理专业人员等指明的其他相关参数。示例:当一种镜片以一种材料提供,并有球面、复曲面、多焦点设计变体时,它将由三个基本UDI-DI(一种材料+设计类型)和相应数量的主UDI-DI覆盖,如下图:
UDI-PI:不需要为标准隐形眼镜分配特定的PI,MDR Annex VI Part C关于PI的规定适用。
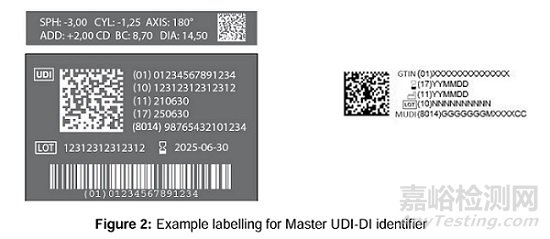
标签:MDR Annex VI Part C section 4中关于UDI载体的规则适用于主UDI-DI。以下标识是基于GS1发行机构的主UDI-DI标准的一个标签示例,反映了自动识别和数据采集(AIDC)和人工可读信息(HRI)载体可与其他信息和条码结合,以满足MDR中规定的要求。
UDI载体(包括主UDI-DI)在隐形眼镜包装上的放置取决于MDR中的规定和要求,尤其要满足空间限制和销售单位的要求。隐形眼镜泡罩包装的标签要求取决于空间限制以及根据MDR要求被视为最终用户使用的最低包装层级。如果根据MDR,隐形眼镜泡罩包装被视为最终用户使用的最低包装层级,则主UDI-DI可以为一条5片的隐形眼镜泡罩带标注一次,前提是制造商已进行了相关的风险管理。
定制式隐形眼镜主UDI-DI分配
主UDI-DI将根据制造商定义的隐形眼镜设计参数组合并结合其他相关参数分配给按订单生产的隐形眼镜,应考虑其高度个性化和定制化的特点,示例如下:
UDI-PI:应使用唯一的批号/序列号作为按订单生产隐形眼镜的UDI-PI。
标签:MDR Annex VI Part C section 4中关于UDI载体的规则同样适用于定制式隐形眼镜的主UDI-DI。以下是基于GS1和HIBCC发行机构的主UDI-DI标准的示例:
4不同包装层级的主UDI-DI分配
主UDI-DI可以与具有相同隐形眼镜设计参数组合的分组相关联,无论包装尺寸如何,该分组将包括识别该分组中的所有使用单位、包装尺寸和更高层级的包装。包装尺寸本身不影响关键设计参数。参照UDI-DI的分配,若存在更高层级的包装,则更高层级的包装应被分配主UDI-DI,运输包装不分配主UDI-DI。
5警戒报告
对于符合MDR的隐形眼镜进行警戒报告时,制造商应提供完整的UDI(主UDI-DI+UDI-PI),以便在发生不良事件时可准确追溯器械。对于遗留隐形眼镜进行警戒报告时,可通过Eudamed ID或UDI-DI(如GTIN)结合UDI-PI来识别,以便在Eudamed中进行警戒报告。
6主UDI-DI实施时间表
EU 2023/2197关于隐形眼镜的主UDI-DI于2023年10月20日发布,从2023年11月9日生效;EU 2025/788关于适用日期修订为2026年11月9日,提供了三年的过渡期,过渡期结束后才对隐形眼镜强制分配主UDI-DI。但在过渡期间,制造商可以自愿进行主UDI-DI分配。
7Eudamed中的器械注册
对于隐形眼镜,当选择特殊器械类型“标准软性隐形眼镜”或“硬性透气性隐形眼镜”或“定制式软性隐形眼镜”或“定制式硬性透气性隐形眼镜”时,主UDI-DI将在Eudamed中注册并代替UDI-DI使用。遗留隐形眼镜不应在Eudamed中注册,除非需要采取警戒行动。
参考资料:MDCG 2024-14 Rev.1 Guidance on Master UDI-DI for contact lenses