您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-08-09 10:35
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.华北制药狂犬病单抗即将上市。华北制药1类新药奥木替韦单抗已进入「在审批」阶段,预计即将获批上市,用于狂犬病毒暴露患者的被动免疫。奥木替韦单抗是华北制药自主研发的一款重组人源狂犬病单抗(rhRIG),曾被列为国家「重大新药创制」科技重大专项品种。目前,国内尚无rhRIG药物上市销售,国内可用于狂犬病毒暴露后预防的被动免疫制剂仅有抗狂犬病血清和狂犬病人免疫球蛋白。
2.腾盛博药新冠鸡尾酒上国际III期临床。腾盛博药新冠中和抗体组合疗法(BRII-196/BRII-198)用于COVID-19感染的早期(首发症状后5天内)和晚期(首发症状后5-10天)门诊患者的III期ACTIV-2研究已在美国、巴西、南非、墨西哥和阿根廷的研究中心完成846例受试者的入组工作。该项研究由美国国立卫生研究院(NIH)下属的国家过敏和传染病研究所(NIAID)资助,目前正在评估比较抗体组与安慰剂组的受试者在接受治疗后28天内住院和死亡的主要复合终点。
3.乐普生物TF-ADC获批临床。乐普生物旗下美雅珂申报的TF靶向ADC药物MRG004A获国家药监局临床试验默示许可,拟临床用于治疗晚期或转移性实体瘤。TF的异常表达通常与肿瘤生长、血管生成、肿瘤转移和临床治疗预后差相关,是一个有吸引力的癌症治疗靶点。全球目前尚无任何靶向TF的药物获批,开发进度最快的是Genmab和Seagen公司联合开发的tisotumab vedotin,同样也是一款抗体偶联药物。
4.微芯JAK抑制剂在美报IND。微芯生物JAK抑制剂CS12192的新药临床试验申请获FDA受理,拟用于治疗移植物抗宿主病。CS12192是该公司自主研发并拥有全球化合物发明专利授权的高选择性JAK3抑制剂,同时部分抑制JAK1和TBK1激酶。在临床前研究中,CS12192已在类风湿性关节炎、多发性硬化病、系统性红斑狼疮、银屑病等自身免疫性疾病模型及移植物抗宿主疾病(GVHD)模型上显示出明显的药效活性。在中国,CS12192正在I期临床中评估治疗类风湿性关节炎的潜力。目前尚无同类药物获批上市。
5.箕星药业引进两款干眼症新药。箕星药业宣布与Oyster Point Pharma达成独家许可协议,将获得Oyster Point Pharma两款拟用于治疗干眼症(DED)症状和体征的OC-01(varenicline)和OC-02(simpinicline)鼻喷雾剂在大中华区开发和商业化权益。根据协议,Oyster Point Pharma将获得1750万美元的首付款以及最高0.75%的箕星药业股份,并有资格获得最高2.048亿美元的里程碑付款,和产品的销售分成。OC-01已向FDA递交新药上市申请,有望今年获批。
国际药讯
1.庞贝病酶替代疗法获FDA批准上市。FDA批准赛诺菲公司(Sanofi)开发的酶替代疗法(ERT)Nexviazyme(avalglucosidaseα-ngpt)上市,用于治疗1岁及以上的晚发性庞贝病(LOPD)患者。在一项关键性Ⅲ期临床COMET中 ,Nexviazyme可以为患者提供步行距离和呼吸功能指标的改善;与对照组相比,Nexviazyme组第49周时与基线相比的用力肺活量预测值百分比(FVC )改善(2.9分vs2.4分)达到非劣效性标准(p=0.0074;95% CI,-0.13,4.99),但未达到统计学优效性(p=0.06)。
2.创新纳米疗法达Ⅱ期临床主要终点。Clene公司及其子公司Clene Nanomedicine宣布,其候选纳米药物CNM-Au8在治疗帕金森病(PD)和多发性硬化(MS)患者的Ⅱ期临床REPAIR中获积极顶线结果。13例PD患者和11例MS患者治疗12周后,患者大脑NAD+/NADH比值平均增加0.589个单位(10.4%),具统计学意义的显著改善(p=0.037);关键次要终点较基线的平均变化也与主要终点一致;而且CNM-Au8具有良好的耐受性,不良事件均为轻度,且与药物无关。
3.卡博替尼获FDA优先审评资格。FDA授予Exelixis制药公司多激酶抑制剂卡博替尼(Cabometyx)补充新药申请优先审评资格,用于治疗经治、放射性碘疗法难治性分化型甲状腺癌(DTC)患者。在一项关键性Ⅲ期临床COSMIC-311中,与安慰剂相比,卡博替尼将疾病进展或死亡风险降低78%(HR=0.22,96% CI,0.13-0.36,p<0.0001)。详细结果已在ASCO2021年会上公布。该申请的PDUFA目标日期为2021年12月4日。
4.默沙东K药在美sBLA获优先审评。FDA授予默沙东PD-1抗体Keytruda补充生物制品许可申请(sBLA)优先审评资格,用于接受完全切除手术后黑色素瘤患者的辅助治疗。PDUFA日期为2021年12月4日。在一项Ⅲ期临床KEYNOTE-716中,与安慰剂相比,Keytruda用于这类患者术后辅助治疗显示出具有统计学意义的无复发生存期(RFS)改善;而且未观察到新的安全性信号。详细结果将在医学会议上公布。
5.渤健/卫材Aβ抗体寻求FDA加速批准。卫材在最新季报中透露,该公司和渤健正与FDA进行沟通,积极推进两家公司联合开发的第二款阿尔茨海默病(AD)药物lecanemab(BAN2401)以获得FDA的批准。lecanemab是一款抗Aβ原纤维抗体,于今年6月获得FDA授予突破性疗法认定。在一项IIb期临床Study 201中,最高剂量(10mg/kg)的lecanemab能显著降低患者大脑中的淀粉样蛋白水平;多个临床和生物标志物终点均表现出了持续的临床缓解。
6.Kite合作开发创新CAR-iNKT疗法。吉利德旗下Kite公司与Appia Bio公司将利用Appia Bio名为“ACUA”的同种异体细胞技术平台,联合开发表达嵌合抗原受体的不变自然杀伤T细胞(CAR-iNKT)疗法,用于治疗血液相关恶性肿瘤。根据协议,Appia Bio将为Kite的嵌合抗原受体(CAR)改造两个源于造血干细胞(HSC)的CAR-iNKT候选疗法,并负责临床前和早期临床研究;Appia Bio将获得预付款与股权投资,以及可能总额达8.75亿美元的额外里程碑付款;而Kite将负责候选产品的后续开发和商业化。
7.拜耳拟收购“不可成药”精准疗法公司。拜耳宣布将以15亿美元首付款和5亿美元里程碑付款的数额,收购Vividion公司。Vividion公司独有的化学蛋白组学(chemoproteomics)技术平台能够靶向“不可成药”靶点,在多个治疗模式领域进行药物开发,包括别构激活剂和抑制剂,蛋白稳定剂和降解剂,以及蛋白互作抑制剂。目前,该公司的主打候选品种包括拟用于治疗携带NRF2突变的癌症的NRF2拮抗剂,以及用于治疗肠易激综合征等炎症性疾病的NRF2激活剂。
医药热点
1.全国「院感」排查整顿即将启动。国务院联防联控机制在8月5日的新闻发布会上宣布,郑州六院疫情是一起医院感染事件,该确诊病例与定点医院收治的一位境外输入的感染德尔塔毒株的患者的基因测序高度同源,这起感染与南京的感染没有关联。国务院副总理孙春兰强调,要汲取院感的教训,对院感实行零容忍;并将在全国组织开展院感防控专项排查行动。
2.预计江苏疫情在8月20日前后获控制。兰州大学《新冠肺炎疫情全球预测系统》发布对全国、湖北、湖南、江苏本轮突发新冠疫情的预测。该预测结果表明,在当前二级响应措施下,如果全国各地能第一时间发现潜在感染者并采取严格的管控措施,全国本轮疫情预计将于8月23日左右得到控制,累计感染人数预计约1087-1598人;若采取三级响应措施,本轮疫情预计在8月26日左右得到控制,累计感染人数或将达到2462人左右。
3.北京开展老年痴呆风险筛查。北京市卫健委印发《2021年脑健康体检(痴呆风险筛查)及老年痴呆防治行动实施方案》提出,要将老年人脑健康工作作为老年健康服务的重要内容之一,建立老年人脑健康体检、管理指导等专业人员队伍。根据《方案》,北京市将为65岁及以上常住人口老年人,以及有糖尿病、高血压、脑卒中病史或近一年主诉记忆力下降的50岁及以上人群,开展老年人脑健康体检(痴呆风险筛查)。
审评动向
申请临床:
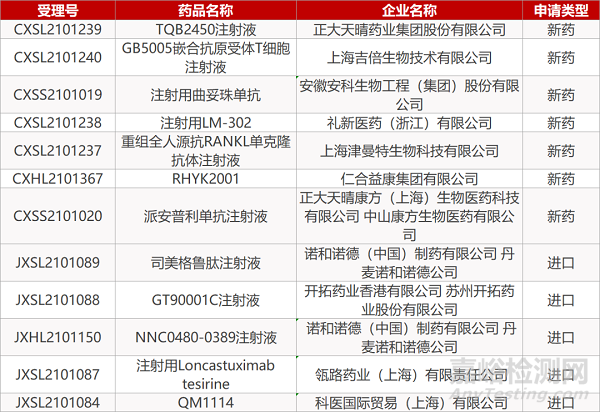
正大天晴的TQB2450注射液、上海吉倍生物的GB5005嵌合抗原受体T细胞注射液、礼新医药的注射用LM-302、上海津曼特生物的重组全人源抗RANKL单克隆抗体注射液、仁合益康集团的RHYK2001、诺和诺德的司美格鲁肽注射液和NNC0480-0389注射液、开拓药业的GT90001C注射液、瓴路药业的注射用Loncastuximab tesirine、科医国际的QM1114。
申请生产:
安徽安科生物的注射用曲妥珠单抗、正大天晴康方(上海)/中山康方的派安普利单抗注射液。
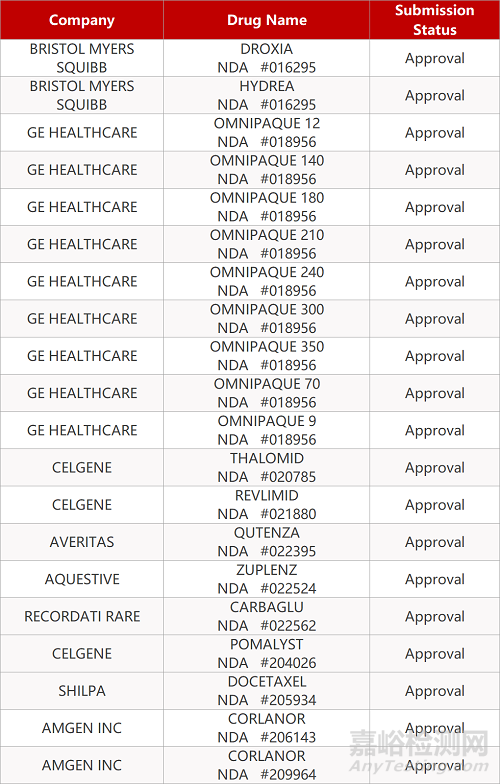

来源:药研发


