您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-01-02 17:06
全瓷义齿用氧化锆瓷块为定制式固定义齿常用的原材料。目前,国内约有40家(来源于国家药品监督管理局数据查询——国产医疗器械产品)企业生产该产品。根据《医疗器械分类目录》[1],全瓷义齿用氧化锆瓷块的分类编码为 17-06-02,管理类别为Ⅱ类,预期用途为供采用计算机辅助设计/计算机辅助制造(computer aided design/computer aided manufacturing,CAD/CAM)方法切削制作牙科固定义齿,如冠、桥、嵌体、贴面。为保证全瓷义齿用氧化锆瓷块的安全、有效,在我国境内上市销售,生产企业需取得国家药品监督管理局批准的医疗器械产品注册证。本研究主要分析全瓷义齿用氧化锆瓷块的安全、有效性,旨在为进一步加快产品注册、审评及生产企业研发提供参考。
1、原材料控制
全瓷义齿用氧化锆瓷块分为白色及彩色两种,白色氧化锆瓷块在义齿加工厂加工时需染色并烧结后才可呈现出定制式义齿的颜色,而彩色氧化锆瓷块无需染色,经雕铣机加工后,通过烧结即可呈现出定制式义齿的颜色。白色及彩色氧化锆瓷块的原材料均为氧化锆粉,只是存在白色与彩色之分。氧化锆粉是影响全瓷义齿用氧化锆瓷块性能的重要因素,每个生产企业都必须严格把控其质量及性能指标,建议生产企业在进行来料检验时,对氧化锆粉的化学成分、粒径、密度进行检测,也可于检测后按照企业内部的要求进行试产以确定氧化锆粉性能指标的符合性。
2、产品技术要求
根据 ISO 6872-2015《Dentistry—Ceramic materials》标准,全瓷义齿用氧化锆瓷块(Ⅱ型)的主要性能指标包括均匀性、无外来异物、放射性、弯曲强度、断裂韧性、线胀系数、化学溶解性、收缩率。其中,弯曲强度的大小决定了全瓷义齿用氧化锆瓷块的临床预期用途,若弯曲强度≥800 MPa,则可制作四单位及四单位以上的修复体。收缩率是CAD/CAM系统的设计参数,可表示全瓷义齿用氧化锆瓷块烧结前后的收缩程度,计算公式为:
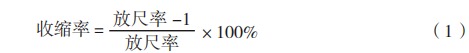
其中,放尺率=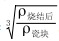 ,由公式(1 )可知,收缩率是通过瓷块密度和烧结后密度计算得到的。生产全瓷义齿用氧化锆瓷块的关键工序是粉体成型和瓷坯预烧结。目前,国内主要采取的是干法成型的方式,包括等静压成型和干压成型,主要控制产品的尺寸及密度,因此,密度应作为考量全瓷义齿用氧化锆瓷块性能的指标之一。瓷坯预烧结主要控制产品的硬度,若硬度超过企业制定的标准,将会对义齿加工厂加工产品时使用的雕铣机及车针造成一定的损坏,甚至会造成车针断裂;若硬度指标偏低,当应用于咀嚼硬物时,将会造成牙齿断裂,因此,在研究产品性能指标时还必须考虑硬度。临床上常出现患者口腔黏膜、牙龈受刺激破溃充血出现红肿的现象,其原因之一为配方不正确,因此,化学成分也是考量全瓷义齿用氧化锆瓷块性能的重要指标。对彩色氧化锆瓷块而言,因在加工厂加工时无需染色,所以,除以上性能指标外,还须检验颜色与比色板是否接近,且需于产品技术要求中明确其配方。
,由公式(1 )可知,收缩率是通过瓷块密度和烧结后密度计算得到的。生产全瓷义齿用氧化锆瓷块的关键工序是粉体成型和瓷坯预烧结。目前,国内主要采取的是干法成型的方式,包括等静压成型和干压成型,主要控制产品的尺寸及密度,因此,密度应作为考量全瓷义齿用氧化锆瓷块性能的指标之一。瓷坯预烧结主要控制产品的硬度,若硬度超过企业制定的标准,将会对义齿加工厂加工产品时使用的雕铣机及车针造成一定的损坏,甚至会造成车针断裂;若硬度指标偏低,当应用于咀嚼硬物时,将会造成牙齿断裂,因此,在研究产品性能指标时还必须考虑硬度。临床上常出现患者口腔黏膜、牙龈受刺激破溃充血出现红肿的现象,其原因之一为配方不正确,因此,化学成分也是考量全瓷义齿用氧化锆瓷块性能的重要指标。对彩色氧化锆瓷块而言,因在加工厂加工时无需染色,所以,除以上性能指标外,还须检验颜色与比色板是否接近,且需于产品技术要求中明确其配方。
3、生物相容性评价
生物安全性是指医疗器械与人体之间相互作用时,必须对人体无致敏性、无刺激性、无遗传毒性等,是生物相容性评价的最基本内容。企业应评价医疗器械全生命周期内的生物安全性。
目前,化学表征及毒理学分析手段难以为全瓷义齿用氧化锆瓷块的生物安全性提供足够的证据,所以,一般采取生物学试验的手段。因全瓷义齿用氧化锆瓷块与人体的接触性质属表面持久接触,根据GB 16886.1-2011《医疗器械生物学评价 第1部分:风险管理过程中的评价与试验》及YY/T 0268-2008 《牙科学 口腔医疗器械生物学评价 第1单元:评价与试验》,建议在进行生物学试验时,应考虑细胞毒性试验、迟发超敏反应试验、皮内反应或口腔黏膜刺激试验、亚慢性全身毒性试验及遗传毒性试验。结合ISO 10993-1 :2018《Biological evaluation of medical devices—Part 1 :Evaluation and testing within a risk management process》,还需增加急性全身毒性试验及植入试验(如全瓷义齿用氧化锆瓷块预期用于植入牙颌骨、牙槽骨部位)。由于全瓷义齿用氧化锆瓷块制成定制式义齿后,为患者安装时,可能发生牙龈出血,因此,还需考虑血液相容性试验。
企业在准备向国家药品监督管理局申请注册的过程中,选择生物学实验室时需注意以下几点:对于国内的实验室,需核查实验室是否具有医疗器械检验资质认定、中国计量认证(China Inspection Body and Laboratory Mandatory Approval,CMA)及中国合格评定国家认可委员会(China National Accreditation Service for Conformity Assessment,CNAS)证书是否覆盖检验标准;对于国外实验室,应要求其提供符合GLP实验室要求的质量保证文件[2];若企业产品还需进行510K注册、医 疗器械法规(Medical Device Regulation,MDR)认证,建议直接选择ISO 10993系列标准进行生物学试验;此外,选择的国内实验室在具备以上资质的情况下,还需符合ISO 17025 :2017《General requirements for the competence of testing and calibration laboratories》的要求,并能提供符合GLP实验室要求的质量保证文件。
4、灭菌消毒工艺
作为定制式义齿的原材料,全瓷义齿用氧化锆瓷块无需进行消毒灭菌,但在制成义齿成品戴入患者口腔之前,须进行消毒。因为在加工过程中会产生粉尘,且所接触的器皿及操作人员均会造成对义齿的污染,建议义齿加工厂在对义齿进行消毒时,选择合适的消毒方法,如微波消毒法、戊二醛溶液浸泡消毒等。
5、产品有效期和包装
5.1 有效期
全瓷义齿用氧化锆瓷块包括圆饼形、马蹄形、方块形、圆柱形,部分产品包含产品坯体、套环、尾柄,在进行有效期验证时,需选择带套环、尾柄的产品,见图 1~2。

图 1 圆饼形套环

注:图2来源于《全瓷义齿用氧化锆瓷块注册技术审查指导原则》(2018 年修订)[3]
图 2 方块形尾柄
验证有效期的方法包括实时老化和加速老化,目前,大多数企业采用的是加速老化试验。加速老化试验是通过改变试验环境,以缩短获得信息所需的时间。
根据 YY/T 0681.1-2018《无菌医疗器械包装试验方法 第1部分:加速老化试验指南》,实施加速老化试验需确定加速老化的温度、环境温度及产品寿命,因此,还需考虑在运输、储存和使用环境条件(温度、湿度等)下给产品性能及包装带来的老化。由于密度、弯曲强度、断裂韧性受温度影响较大,因此,建议老化后检测以上3个指标的性能。
5.2 包装
市面上全瓷义齿用氧化锆瓷块的包装盒材质基本为铜裱纸板,内置EVA材质的珍珠棉,并将其装于瓦楞纸箱内进行运输;考虑到运输过程中可能会出现挤压、跌落、振动等情况,建议企业根据包装箱的重量,选择GB/T 4857系列标准进行包装试验。
6、客户端烧结曲线
全瓷义齿用氧化锆瓷块经雕铣机加工、制作为定制式义齿后,需对其进行烧结。烧结需经历3个阶段,即从室温至最高烧结温度的升温阶段、在最高温度的保温阶段、从最高温度降至室温的降温阶段。定制式义齿常见的质量问题为易发生断裂,烧结温度正是其原因之一。在不同的烧结温度下,氧化锆会发生相变,即单斜氧化锆(m-ZrO2)、四方氧化锆(t-ZrO2)和立方氧化锆(c-ZrO2)之间的转变,转变过程中定制式义齿的体积会发生膨胀或收缩;若未控制好最高烧结温度,会导致单斜相含量增加,四方相含量降低,从而引起定制式义齿断裂。在烧结修复体时,必须控制升温速率,从而确保定制式义齿受热均匀并控制其晶粒生长速度,且可达到消除气孔的目的;若升温速率过快,定制式义齿内部气孔过多,则会导致孔隙度增加。对于保温时间,可根据定制式义齿的晶粒尺寸和有无气孔适当的缩短或延长。降温过程中也会出现相变,若降温速率太快,可能会引起微裂纹(注:可使用X线衍射法分析烧结各阶段的相含量,采用热重分析方法分析烧结温度)。
7、透光率
在定制式义齿的修复中,一致的透光率可使定制式义齿再现天然牙的特性,因此,掌握天然牙的透光率是全瓷义齿修复成功的关键[4]。影响定制式义齿透光率的主要因素包括原材料性能指标、产品烧结温度及制作方法。原材料性能指标包括原材料的化学成分、粒径、烧结温度等,因此,在选择供应商时,需依据设计输入考虑前述原材料的性能。产品烧结温度需根据全瓷义齿用氧化锆瓷块的性能控制升温速率、最高温度、保温时间及降温速率。在制作定制式义齿时,需控制好打磨(打磨转速控制为10000 r/min)和抛光工序,若义齿表面粗糙,将导致透光率降低。另外,全瓷义齿用氧化锆瓷块在进行染色时,需控制好浸泡染色液的时间,若浸泡时间过长,将会造成颜色加深,从而导致透光率降低。
综上所述,本研究简要分析了全瓷义齿用氧化锆瓷块的安全、有效性,旨在分享全瓷义齿用氧化锆瓷块的相关知识,从而推动行业的发展与进步。
【参考文献】
[1]国家食品药品监督管理总局.总局关于发布医疗器械分类目录的公告(2017年第104号)[EB/OL].(2017-09-04)[2018-08-01].
https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20170904150301406.html.
[2]国家药品监督管理局医疗器械技术审评中心.国外实验室出具的生物相容性试验报告在中国注册时是否认可[EB/OL].(2018-06-29)[2018-06-29].
https://www.cmde.org.cn/CL0113/7783.html.
[3]辽宁省药械审评与监测中心.全瓷义齿用氧化锆瓷块注册技术审查指导原则(2018 年修订)2018年第116号[EB/OL].(2018-11-13)[2018-12-31].
http://www.fredamd.com/law/11524.html.
[4]苏亚丽,王少海.天然牙与全瓷修复体光物理学特性及透光率[J].口腔颔面修复学杂志,2014,15(4):236-239.

来源:医疗装备杂志


