您当前的位置:检测资讯 > 监管召回
嘉峪检测网 2024-05-25 09:30
经常有医疗器械企业收到不良事件监测预警信号,那么,对于这些预警信号会引发药监局飞检吗?
1.什么是医疗器械不良事件监测预警信号?
根据《医疗器械不良事件监测和再评价管理办法》(国家市场监督管理总局令第1号)有如下定义:
第四十八条 持有人通过医疗器械不良事件监测,发现存在可能危及人体健康和生命安全的不合理风险的医疗器械,应当根据情况采取以下风险控制措施,并报告所在地省、自治区、直辖市药品监督管理部门:
(一)停止生产、销售相关产品;
(二)通知医疗器械经营企业、使用单位暂停销售和使用;
(三)实施产品召回;
(四)发布风险信息;
(五)对生产质量管理体系进行自查,并对相关问题进行整改;
(六)修改说明书、标签、操作手册等;
(七)改进生产工艺、设计、产品技术要求等;
(八)开展医疗器械再评价;
(九)按规定进行变更注册或者备案;
(十)其他需要采取的风险控制措施。
与用械安全相关的风险及处置情况,持有人应当及时向社会公布。
第四十九条 药品监督管理部门认为持有人采取的控制措施不足以有效防范风险的,可以采取发布警示信息、暂停生产销售和使用、责令召回、要求其修改说明书和标签、组织开展再评价等措施,并组织对持有人开展监督检查。
由此可见,开展医疗器械预警和风险控制,是法规要求。通过有效的方式收集医疗器械的风险信号非常重要,随着医疗器械不良事件监测信息系统中预警模块的上线,有效地实现了在监测系统中满足风险信号预警和风险控制的功能。
2.怎么收到医疗器械不良事件监测预警信号?
在医疗器械不良事件监测信息系统中设置了预警模块的功能,通过在系统设置一定的预警规则,自动生成或者触发预警信号,发送给系统相关用户,包括注册人和监测机构,达到实时有效监控的目的。
根据国家不良反应中心发布的相关预警指南文件可知,预警规则可以新增、修改、查看、启动、禁用等等,预警规则可以由国家中心管理员设置预警监测时间和监测时限,从而生成的预警信号,向注册人、事发地市级监测机构、事发地省级监测机构、注册人所在地省级监测机构、国家级监测机构推送预警信号。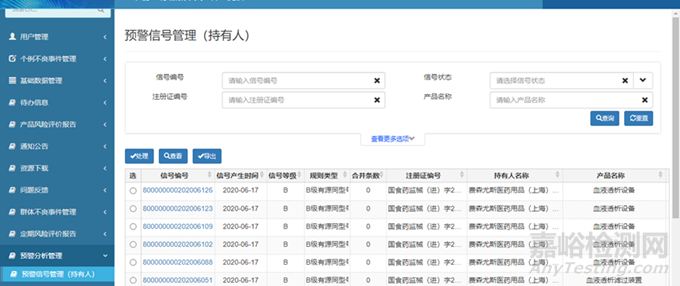
3.如何处置医疗器械不良事件监测预警信号?
当注册人收到预警信号后,需要填写的处理信息,提交给注册人所在地省级监测机构进行审核,注册人、事发地市级监测机构、事发地省级监测机构、注册人所在地省级监测机构、国家级监测机构对信号填写处置和处置意见。
通过预警信号模块,各地不良反应监测中心会就风险信号进行讨论和处置。
2024年4月18日,国家中心就在山西省太原市组织召开了2024年第一季度医疗器械不良事件监测季度风险信号讨论会。
此外,还有各地方的不良反应监测中心,也会对预警信号进行研讨分析,有效处置相关内容。同时,各地也会就不同类型产品的预警规则进行分析,从而细化完善风险信号预警规则。
4.医疗器械不良事件监测预警信号与监管检查?
由以上内容可知,风险预警信号是在不良事件监测系统中管理产品风险的一个功能,通过系统化运用风险预警信号的方式,提高了发现医疗器械不良事件风险的能力,从而可以降低产品风险监测难度。对于严重的预警信号可能会引发相关合规性的检查,如不良事件监测专项检查等。
通过对预警信号多方的评价、处置与管理,降低产品风险,为提升产品质量打下基础。
因此,当企业遇到不良事件监测信号时,不要过分担忧,需要积极正确有效地处置,配合监管部门的调查,也需要从源头管控医疗器械产品质量,避免伤害事件发生,从而有效控制产品风险。

来源:器械QMS


