7月26日,上海市药监局官网发布《上海市医疗器械不良事件监测年度报告(2022年度公众版)》。详细内容摘录如下:
上海市可疑医疗器械不良事件报告总体情况
2022年,上海市通过“国家医疗器械不良事件监测信息系统”上报可疑医疗器械不良事件报告12097份(图1)。
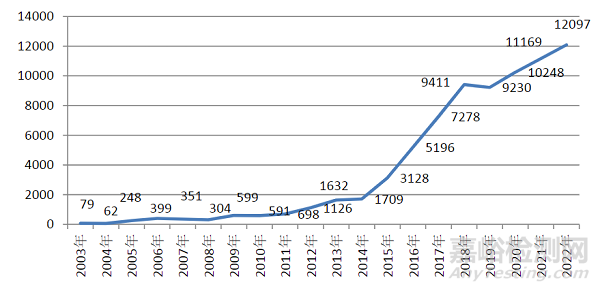
图 1. 上海市历年可疑医疗器械不良事件报告数量
1. 每百万人口平均报告数量
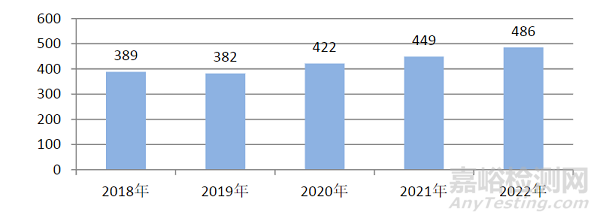
2022年,本市每百万人口平均可疑医疗器械不良事件报告数为486份,较2021年增加37份(图2)。
图 2. 近五年上海市每百万人口可疑医疗器械不良事件报告数量比较
2. 基层注册用户数量
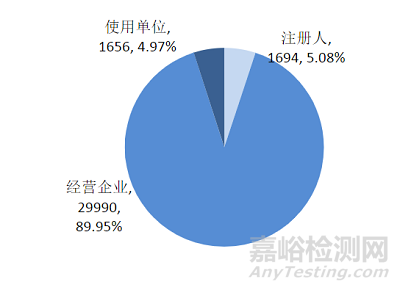
截至2022年12月31日,上海市已有33340家用户在国家医疗器械不良事件监测信息系统中注册,较2021年增加2300家,增长了7.41%。其中,注册人1694家,经营企业29990家,使用单位1656家(图3,图4)。
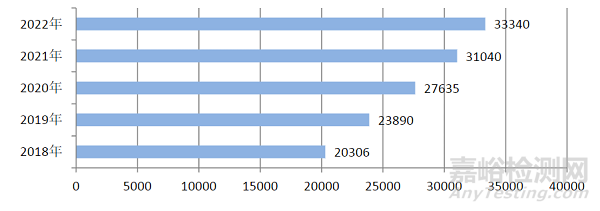
图3近五年基层用户注册情况
图4监测网络基层用户注册构成情况
2022年可疑医疗器械不良事件报告统计分析情况
一、上海地区可疑医疗器械不良事件报告统计分析情况
1.按报告来源分析
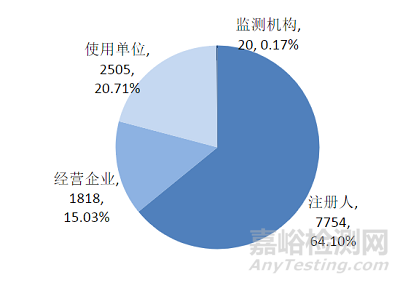
2022年上海市上报的12097份可疑医疗器械不良事件报告中,注册人上报7754份,占64.10%,经营企业上报1818份,占15.03%;使用单位上报2505份,占20.71%;监测机构代报的20份,占0.17%。(图5、图6)。
图5. 2022年度上海市可疑医疗器械不良事件报告按来源构成分析
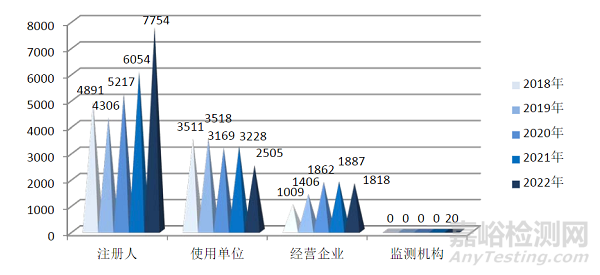
图6 近五年上海市可疑医疗器械不良事件报告来源数量分析
2.按医疗器械产品管理类别分析
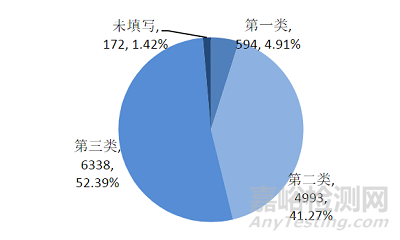
2022年上海市上报的可疑医疗器械不良事件报告中,第三类医疗器械不良事件报告6338份,占52.39%;第二类医疗器械不良事件报告4993份,占41.28%;第一类医疗器械不良事件报告594份,占4.91%,未填写产品管理类别的报告172份,占1.42%。不良事件报告主要涉及第三类和第二类医疗器械,与医疗器械风险程度高低相吻合(图7)。
图 7 可疑医疗器械不良事件报告涉及的产品按管理类别分析
3.按医疗器械产品分类分析
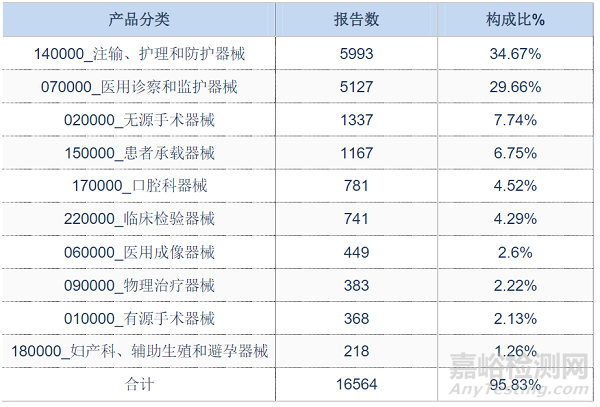
2022年上海市上报的可疑医疗器械不良事件报告中排名前十位的产品分类目录见表1。排名前十位的分类目录涉及的不良事件报告数占上海市上报报告数的81.95%。
表1 2022年上海市上报的可疑医疗器械不良事件报告数前十位的产品分类目录
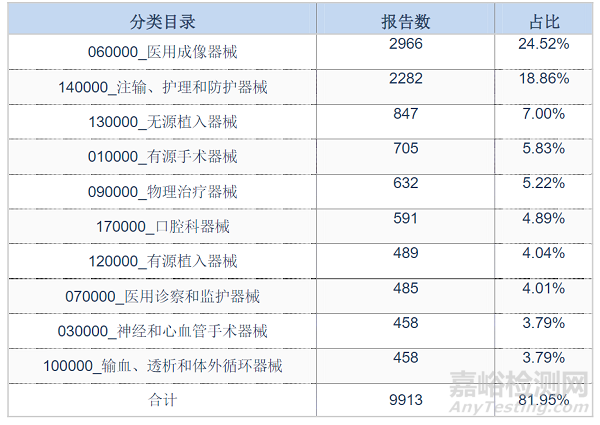
注:剔除未填写产品注册证号的报告
4.按医疗器械使用场所分析
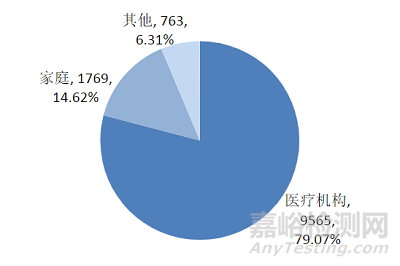
2022年,上海市上报的可疑医疗器械不良事件报告按产品使用场所分析,在医疗机构中使用的有9565份,占报告总数的79.07%;在家庭中使用的有1769份,占报告总数的14.62%;其他情况有763份,占报告总数的6.31%(图8)。
图8 2022年度上海市可疑医疗器械不良事件报告涉及产品按使用场所分析
二、涉及上海注册人产品的可疑医疗器械不良事件报告统计
1.按报告来源分析
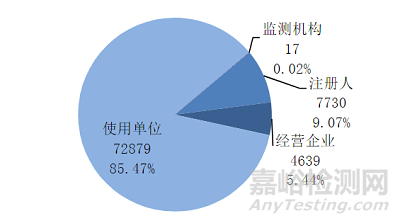
2022年,中心通过国家医疗器械不良事件监测信息系统共收到与上海注册人相关的医疗器械不良事件报告85265份,其中注册人主动上报7730份,占9.07%,经营企业上报4639份,占5.44%;使用单位上报72879份,占85.47%;监测机构代报17份,占0.02%(图9)。
图9 2022年度涉及上海注册人产品的可疑医疗器械不良事件报告按来源构成分析
2.按医疗器械产品管理类别分析
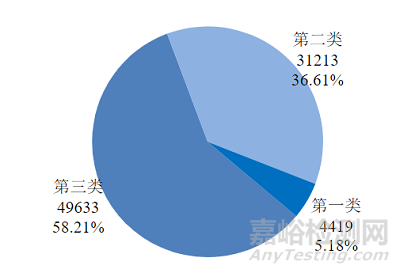
2022年涉及上海注册人的可疑医疗器械不良事件报告中,第三类医疗器械不良事件报告49633份,占58.21%;第二类医疗器械不良事件报告31213份,占36.61%;第一类医疗器械不良事件报告4419份,占5.18%。不良事件报告主要涉及第三类和第二类医疗器械,与医疗器械风险程度高低相吻合(图10)。
图 10 涉及上海注册人产品的可疑医疗器械不良事件报告按产品管理类别分析
3.按医疗器械产品分类分析
根据新的《医疗器械分类目录》,2022年收到涉及本市注册人产品的可疑医疗器械不良事件报告中,位列前十位的产品类别情况见表2。排名前十位的产品涉及的报告数占总报告数量的88.89%。
表2 涉及上海注册人的可疑医疗器械不良事件报告数前十位的产品分类目录
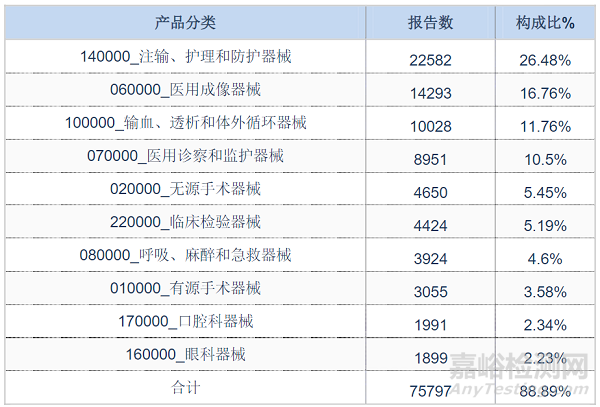
在85265份报告中,涉及由上海审批的第二类产品的报告共17284份,占全部报告的20.27%,排名前十位的产品分类情况见表3。
表3 2022年上海批准的第二类医疗器械不良事件报告数前十位的产品分类目录
该年度报告数据来源于2022年1月1日至12月31日期间,国家医疗器械不良事件监测信息系统中上海市报告的不良事件和全国各地经营、使用上海注册人产品后发生的不良事件,按“可疑即报”原则收集汇总,相关报告并不代表所涉及的医疗器械必然存在质量问题或不合理风险。
医疗器械不良事件监测小贴士
1、医疗器械:是指直接或者间接用于人体的仪器、设备、器具、体外诊断试剂及校准物、材料以及其他类似或者相关的物品,包括所需要的计算机软件;其效用主要通过物理等方式获得,不是通过药理学、免疫学或者代谢的方式获得,或者虽然有这些方式参与但是只起辅助作用;其目的是:
(1)疾病的诊断、预防、监护、治疗或者缓解;(2)损伤的诊断、监护、治疗、缓解或者功能补偿;(3)生理结构或者生理过程的检验、替代、调节或者支持;(4)生命的支持或者维持;(5)妊娠控制;(6)通过对来自人体的样本进行检查,为医疗或者诊断目的提供信息。
2、医疗器械不良事件:是指已上市的医疗器械,在正常使用情况下发生的,导致或者可能导致人体伤害的各种有害事件。
3、严重伤害,是指有下列情况之一者:
(1)危及生命;
(2)导致机体功能的永久性伤害或者机体结构的永久性损伤;
(3)必须采取医疗措施才能避免上述永久性伤害或者损伤。
4、群体医疗器械不良事件:是指同一医疗器械在使用过程中,在相对集中的时间、区域内发生,对一定数量人群的身体健康或者生命安全造成损害或者威胁的事件。
5、医疗器械不良事件监测:是指对医疗器械不良事件的收集、报告、调查、分析、评价和控制的过程。我国医疗器械不良事件监测按照“可疑即报”原则收集报告,即为可疑医疗器械不良事件报告。
6、家庭中常用的医疗器械:主要有血压计、体温计、血糖仪、隐形眼镜、胰岛素注射笔等。
血压计主要分为水银柱式血压计和电子(无液)血压计两大类。血压计在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为测量结果不准确、间断性黑屏、不显示血压值等。
体温计主要分为玻璃体温计、电子体温计和红外体温计。其在使用中可能出现的不良事件主要表现为测量结果不准确、水银柱不上升/下降、不能计数等。
血糖仪在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为血糖测量值不准确、血糖值显示不清晰、屏幕不显示等。
隐形眼镜可能导致人体伤害的主要可疑不良事件为眼睛干涩、红肿、疼痛、流泪、畏光、视物不清、充血、刺激感等。
胰岛素注射笔在使用中可能会出现的不良事件主要为注射部位疼痛、注射针头漏液、推动困难、笔芯密封不严、笔芯变色等。
7、个人发现导致或者可能导致严重伤害或死亡的医疗器械不良事件该如何上报?
个人发现导致或者可能导致严重伤害或死亡的医疗器械不良事件,可以将医疗器械不良事件情况告诉医生,请医生为您填写《可疑医疗器械不良事件报告表》;也可以向事发地所在区市场监督管理局报告。
8、国家医疗器械不良事件监测信息系统注册要求:注册人、经营企业和二级以上医疗机构应当注册为国家医疗器械不良事件监测信息系统用户,主动维护其用户信息,报告医疗器械不良事件。注册人应当持续跟踪和处理监测信息;产品注册信息发生变化的,应当在系统中立即更新。鼓励其他使用单位注册为国家医疗器械不良事件监测信息系统用户,报告医疗器械不良事件相关信息。