目的:建立某高风险注射剂生产企业制药用水系统微生物数据库,为企业制药用水系统污染微生物的有效控制和溯源调查提供指导。
方法:连续4个季度对某大容量注射剂生产企业的纯化水系统和注射用水系统监控收集微生物,采用基于16S rRNA 和ITS rDNA 序列比对等方法鉴定污染微生物,结合微生物种属和来源信息进行分析,建立企业制药用水系统的微生物菌库。
结果:共分离鉴定1499 株细菌和20株真菌,注射用水系统和纯化水系统的微生物分别占比9.0%和91.0%。纯化水系统中鞘氨醇单胞菌和甲基杆菌最多,分别占全部分离菌的28.9%和25.2%。注射用水系统中葡萄球菌和微球菌较多,分别占全部收集菌的24.9%和18.2%。纯化水系统中污染的微生物主要为革兰氏阴性菌,占污染微生物总数的67.0%。注射用水系统中污染的微生物主要为革兰氏阳性菌,占污染微生物总数的60.3%。制药用水系统中较为常见的真菌为杂色曲霉菌和产黄青霉。此外,经分析发现,纯化水系统的微生物在第二季度和第三季度数量占比较多,占全年微生物总量67.8%,第一季度和第四季度微生物数量则下降;注射用水系统微生物数量则在第二季度较多,其余3个季节数量差不多。
结论:建立制药用水系统微生物菌库可指导制药用水系统的运行维护及消毒灭菌,同时也为高风险药品生产企业的微生物污染事件提供溯源调查基础。
制药用水是药品生产过程中使用量最大最广的一种原料,尤其是注射剂生产企业使用的注射用水,会通过注射直接进入人体,直接影响患者的安全[1]。制药用水的制备、储存和分配系统是药品生产的关键系统,《药品生产质量管理规范》(GMP)规定药品生产企业应根据监控计划对制药用水的微生物负载等指标进行监测,并通过年度质量回顾工作分析制药用水是否持续处于稳定、受控状态。随着新版GMP 的实施,各制药企业开始关注制药用水系统的风险控制,尤其是水中微生物的控制。因为水系统中的微生物可浮游或黏附于管道和储罐的内壁等部位,并能大量繁殖形成生物膜,可以持续释放微生物从而形成持久的污染源,同时生物膜也是形成内毒素的主要原因[2]。
微生物检测是评价制药用水是否合格的重要指标,微生物指标的检测与控制是一项必要而复杂的工作[3-4]。尤其针对高风险无菌药品生产企业,通过对制药用水系统的微生物进行系统科学的收集和分析,采用合适的鉴定手段对制药用水正常状态下微生物进行调研,可以帮助生产企业更好地对日常制药用水系统运行及消杀情况进行评价,也可以进一步指导制药用水系统的灭菌、消毒和清洁[5-6]。建立的制药用水系统微生物菌库也可为基于微生物和药品特性分析风险等级收集的药品生产环境菌库奠定数据基础,帮助药品中污染微生物进行溯源调查。
1、材料
1.1仪器
ME2002E 电子天平(瑞士梅特勒-托利多公司);MLS-3781-PC 高压蒸汽灭菌器(日本三洋公司);生物安全柜(力康生物医疗科技控股有限公司);SF450灭菌箱、IF450 恒温培养箱、ICP55 低温培养箱均来自德国Memmert;HTY-2000B 型集菌仪、FC502 一次性使用集菌培养器均来自杭州泰林生物技术设备有限公司;ABI3730-XL 测序仪(美国ABI 公司)。
1.2培养基
胰酪大豆胨琼脂培养基(TSA , 批号:1064583)、R2A 琼脂培养基(批号:1061327)均由广东环凯微生物科技有限公司提供;以上培养基适用性检查均符合中国药典2015 年版规定[7]。
2、方法与结果
2.1制药用水系统微生物的收集
本研究连续4 个季度对某大容量注射剂无菌药品生产企业纯化水的各分配系统总供水点、回水点、使用点和注射用水系统供水点、各车间回水点及使用点进行取样,按照中国药典2015 年版纯化水标准进行微生物限度检查。纯化水的各分配系统总供水点、回水点每天取样检测,各使用点每月取样检测;注射用水系统供水点、各车间回水点每天取样检测,各使用点每月取样检测。
2.2制药用水系统微生物的分离和保存
一共收集获得1 499 株细菌和20 株真菌,对收集的微生物进行复苏分离纯化,复苏培养基采用TSA 和R2A 琼脂培养基,采用磁珠保存管置−70 ℃冰箱保存。部分无法复苏的菌株采用直接单个纯菌落鉴定。
2.3细菌16S rDNA 全长测序及真菌ITS rDNA 测序鉴定
对制药用水系统收集获得的1 499 株细菌及20 株真菌分别采用测序仪进行细菌16S rDNA 和真菌ITS rDNA 测序鉴定。本研究比对的数据库包含NCBI-Fungi 和NCBI-Bacteria(同源性>98.65%判定为同一种微生物[8])。
2.4制药用水系统微生物污染分析
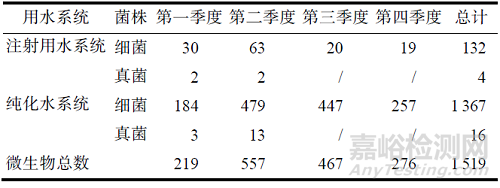
本次通过4 个季度连续收集到制药用水系统微生物菌株共计1 519 株,包括1 499 株细菌和20株真菌。其中132 株细菌来源于注射用水系统,1 367 株细菌来源于纯化水系统;4 株真菌来源于注射用水系统,16 株真菌来源于纯化水系统。来源于注射用水系统的微生物占比9.0%,来源于纯化水系统的微生物占比91.0%。整个制药用水系统细菌占比98.7%,真菌占比1.3%。结果见表1。
表1 菌株数统计
2.5随季节微生物污染变化
纯化水系统的微生物在第二季度和第三季度数量占比较多,占全年微生物总量67.8%,第一季度和第四季度微生物数量则下降;注射用水系统微生物数量则在第二季度较多,其余三个季节数量都差不多。结果见表1。这可能和温度、湿度等季节性因素存在关联。也有报道显示,在丰水期制药用水系统管路内检出革兰氏阴性菌比例上升,提示在这些时期需注意水系统管路等清洁消毒是否到位。
2.6制药用水系统微生物菌库的建立和分析
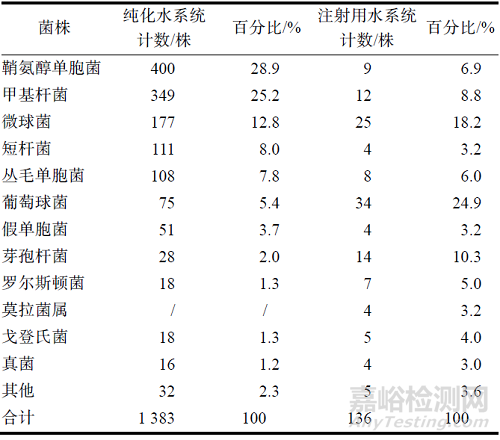
从制药用水系统收集的1 519 株微生物的测序鉴定结果统计见表2。纯化水系统中鞘氨醇单胞菌和甲基杆菌最多,分别占全部分离菌的28.9%和25.2%;其次为微球菌、短杆菌和丛毛单胞菌,分别占全部收集菌的12.8%,8.0%和7.8%。注射用水系统中葡萄球菌和微球菌较多,分别占全部收集菌的24.9%和18.2%;其次为芽孢杆菌和甲基杆菌,分别占全部分离菌的10.3%和8.8%。本研究通过对4 个季度收集的制药用水微生物的测序鉴定结果进行整理和分析,初步建立了制药用水微生物菌库。
表2 制药用水系统微生物鉴定结果
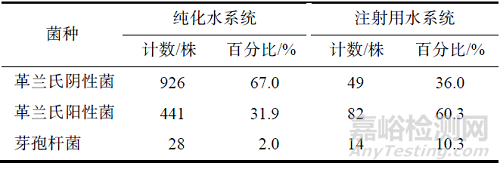
对微生物鉴定结果分析总结见表3,纯化水系统中污染的微生物主要为革兰氏阴性菌,占污染微生物总数的67.0%,其中也有芽孢杆菌污染(占比2.0%)。注射用水系统中污染的微生物主要为革兰氏阳性菌,占污染微生物总数的60.3%,其中芽孢杆菌污染占比10.3%。
表3 制药用水系统微生物污染结果
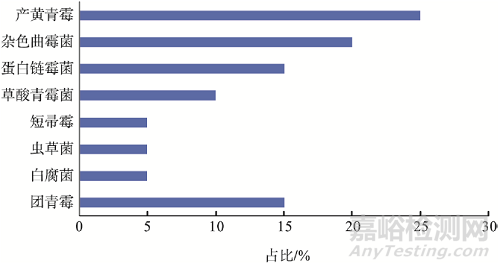
本研究从制药用水系统中一共收集到20 株真菌,污染真菌种群的多样性分析见图1。青霉菌是制药用水系统中主要污染真菌,占比50%,其中最常见的为产黄青霉。其次为杂色曲霉菌,占比20%。注射用水系统中污染的真菌为团青霉和白腐菌。
图1 制药用水系统污染真菌种群多样性分析
3、讨论
从建立的制药用水微生物菌库各方面的对比情况分析可知,制药用水系统中微生物占比绝大多数为革兰氏阴性菌,占比64.2%。其中收集到假单胞菌55 株,假单胞菌属的微生物容易形成生物膜,易造成水系统的微生物负载超标,对产品和患者安全带来影响,因此需要在水系统中严格控制,可采用热消毒方式(通常80 ℃)对这类热敏感微生物进行杀灭。芽孢类微生物占比3%,目前国际上也将芽孢类微生物列为产品中不可接受微生物,因此制药用水系统中如果出现这类较难消杀的微生物[9],也需要引起重视。在制药用水系统中较为常见的真菌为杂色曲霉菌和产黄青霉。从FDA 的Bad Bud Book 致病菌参考手册可知,曲霉菌属和青霉菌属均属于不可接受微生物范畴,FDA 也曾经因为产品中出现这两大类微生物把产品进行召回,因此针对水系统出现的这2 类霉菌,需要制定有效的消毒杀菌手段,防止这类微生物形成生物膜,造成更大的危害。
本次研究收集的注射用水系统污染的微生物主要为革兰氏阳性菌,可能革兰氏阳性菌细胞壁较厚耐热性好,比革兰氏阴性菌更能耐受注射用水系统温度(70~80 ℃)。而纯化水系统污染的微生物主要为革兰氏阴性菌,因此可根据纯化水系统和注射用水系统微生物种类的不同,采取有针对性的控制微生物手段。注射用水系统出现的革兰氏阳性菌主要考虑少量来源于纯化水系统,更多可能是外部环境带来的污染,因此企业需要重点考察外部环境对注射用水系统的影响,确保注射用水系统的清洁干净(包括各个取样点、使用点),同时应对注射用水系统进行系统检查,重点检查维护是否到位、是否存在可能与外部相通的位置。
本研究通过4个季度的持续采样收集制药用水微生物,初步建立了高风险药品生产企业制药用水系统的微生物菌库,但是环境微生物库的建立是个持续动态的过程,因此需要在日常监测中不断完善[9]。制药用水系统微生物菌库的建立,可帮助生产企业更好地评价日常水系统运行情况及消杀效果,并根据菌群建立不同的消杀方案,同时也为高风险药品生产企业的微生物污染事件提供溯源调查基础。
参考文献
[1] 丁玉莲, 杜文革, 罗艳娥. 注射用水系统微生物控制的风险管理[J]. 今日药学, 2013, 23(1): 14-18.
[2] 李志龙, 赵虹, 孙俊峰, 等. 制药用水系统微生物控制分析[J]. 中国卫生工程学, 2014, 13(4): 324-326.
[3] GU M, XU D, GU B R. A tentative exploration on fluorescence staining counting method as the alternative method of microbial limit test for the pharmaceutical water[J].Drug Stand China(中国药品标准), 2017, 18(4): 298-303.
[4] GAO C Y, WU G P, MA W D, et al. Validation of fast testing of microorganism with a Milliflex Quantum method[J]. Chin J New Drugs(中国新药杂志), 2015, 24(1): 85-89.
[5] MEISI L S. Microbial detection and control analysis of pharmaceutical water[J]. Chem Intermediate(当代化工研究) ,2018(7): 159-160.
[6] SONG M H, LI Q Q, QIN F. Establishment and data analysis of a contaminated microorganisms library for sterile pharmaceutical production processes[J]. Chin J Pharm Anal(药物分析杂志), 2019, 39(11), 1954-1960.
[7] 中国药典. 四部[S]. 2015: 140-141.
[8] KIM M, OH H S, PARK S C, et al. Towards a taxonomic coherence between average nucleotide identity and 16S rRNA gene sequence similarity for species demarcation of prokaryotes[J]. Int J Syst Evol Microbiol, 2014(64): 346-351.
[9] ZHENG X L, WANG Z N, WANG Z J, et al. Establishment of the environmentally microbial library in the drug sterility testing laboratory[J]. Chin J Mod Appl Pharm(中国现代应用药学), 2015, 32(7): 847-850.