您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-10-18 08:47
本文主要介绍了北京艾克伦医疗科技有限公司研发的医疗器械“Septin9/SDC2/BCAT1 基因甲基化检测试剂盒(PCR- 荧光探针法)”的临床前研发实验。
一、Septin9/SDC2/BCAT1 基因甲基化检测试剂盒(PCR- 荧光探针法)的产品主要组成成分
产品主要组成成分见下表:
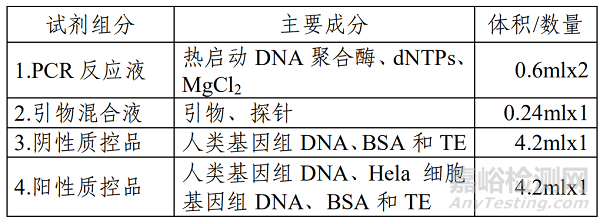
二、Septin9/SDC2/BCAT1 基因甲基化检测试剂盒(PCR- 荧光探针法)的产品预期用途
本试剂盒用于体外定性检测人外周血血浆中 Septin9、SDC2、BCAT1 基因的甲基化。
病人外周血中甲基化的 Septin9、SDC2、BCAT1 基因可以通过 DNA 的特异扩增而被检测到。本试剂盒适用于临床医师建议做肠镜检测,但因病人依从性差或其它医学原因无法做肠镜检测患者的辅助诊断,不能作为肿瘤早期诊断或确诊的依据,不能用于普通人群的肿瘤筛查。本产品仅作为原发性结直肠癌的辅助诊断供临床医师参考。
Septin9(胞裂蛋白 9)是高度保守的三磷酸鸟苷结合蛋白septin 家族成员之一,广泛存在于人体细胞,具有重要的肿瘤抑制作用,其甲基化被证实与结直肠癌的发生密切相关。SDC2(多配体蛋白聚糖-2)在结肠间充质细胞中表达,参与细胞增殖、细胞迁移和细胞-基质相互作用,可以通过多种途径抑制肿瘤形成。BCAT1(支链氨基酸转移酶 1)为原癌基因 MYC 直接调控的下游靶基因之一,其表观遗传沉默可导致 Wnt 信号激活,诱导肿瘤发生。研究发现,结直肠癌患者血浆样本中 Septin9、SDC2 及 BCAT1 三基因启动子区域呈高度甲基化。甲基化可导致基因转录受到抑制,从而影响基因的正常表达,并使其抑癌功能丧失。
三、Septin9/SDC2/BCAT1 基因甲基化检测试剂盒(PCR- 荧光探针法)的产品包装规格
30 人份/盒。
四、Septin9/SDC2/BCAT1 基因甲基化检测试剂盒(PCR- 荧光探针法)的产品检验原理
提取血浆中的游离 DNA,然后用亚硫酸盐转化未发生甲基化的胞嘧啶,通过脱氨基反应产生尿嘧啶磺酸盐,发生甲基化的胞嘧啶则不会被亚硫酸盐转化。将亚硫酸盐转化的 DNA(BisDNA)做多重 PCR 扩增,PCR 反应中的引物、探针能区分甲基化和非甲基化序列,甲基化序列优先得到扩增,与甲基化 Septin9、SDC2、BCAT1 基因序列特异性结合的荧光素探针可以在 PCR 反应中专一地检测出甲基化序列。内参对照 ACTB(β-actin)基因用于评估检测中 DNA 量是否足够。
五、Septin9/SDC2/BCAT1 基因甲基化检测试剂盒(PCR- 荧光探针法)的主要原材料的选择
本产品的主要原材料包括引物干粉、PCR反应液、人类基因组DNA和Hela细胞基因组DNA。这些原料均是通过外购的方式获得。
其中引物的序列均由艾克伦医疗自行设计,由合成公司经过合成、修饰、纯化方式获得;PCR反应液由供应商化学合成获得;人类基因组DNA和Hela细胞基因组DNA由供应商提取纯化获得。
艾克伦医疗对主要原材料进行了供应商的选择,通过功能性实验筛选出合格供应商,制定了各主要原材料的技术要求和质量标准并经检验合格。
六、Septin9/SDC2/BCAT1 基因甲基化检测试剂盒(PCR- 荧光探针法)的企业参考品设置情况
本产品企业参考品包括阳性参考品、阴性参考品、精密度参考品以及检测限参考品,组成如下:
阳性参考品包括3种,由一定DNA浓度下,Septin9、SDC2、BCAT1三基因不同甲基化比例样本组成。
阴性参考品包括3种,其中两种为不同DNA浓度下,Septin9、 SDC2、BCAT1均无甲基化的参考品,一种为三基因均甲基化但
甲基化比例低于检测限的阴性参考品。
精密度参考品包括2种,为一定DNA浓度下,Septin9、SDC2、BCAT1三基因均甲基化,但甲基化程度高低不同的精密度参考
品。
检测限参考品包括1种,为一定DNA浓度下,Septin9、SDC2、BCAT1三基因甲基化略高于检测限水平的参考品。
七、Septin9/SDC2/BCAT1 基因甲基化检测试剂盒(PCR- 荧光探针法)的生产工艺及反应体系研究
艾克伦医疗对试剂盒反应体系的研究中包括引物探针浓度的确定、PCR反应液的选择、阴/阳性质控品配方的确定等;对PCR
过程中的退火温度进行研究;完成样本的用量以及样本保存时间的研 究 ; 对 该 产 品 三 种 适 用 机 型 宏 石 PCR 分 析 系 统
SLAN-96P、Applied Biosystems 7500,Roche Lightcycler 480的反应程序及分析条件进行了研究。
通过功能性实验,最终确定了最佳的反应体系。艾克伦医疗根据试剂盒中试剂及组件的主要生产工艺的研究结果,确定了最
佳的生产工艺。
八、Septin9/SDC2/BCAT1 基因甲基化检测试剂盒(PCR- 荧光探针法)的分析性能评估探究
本产品分析性能评估内容包括:准确性(阳性符合率、阴性符合率)、精密度、检测限、分析特异性的评估;核酸提取试剂的性能评估;三种适用的 PCR 仪机型(宏石 PCR 分析系统SLAN-96P、Applied Biosystems 7500,Roche Lightcycler 480)评估。
准确性研究分别使用三个批次的试剂盒对企业阴/阳性参考品及临床样本来源的结直肠癌阴/阳性样本池在三种适用机型上进行检测,检测结果为阳性符合率 100%、阴性符合率 100%。 将三个基因的甲基化模板 DNA 混合成 DNA 不同浓度和不同甲基化水平的样本,使用试剂盒在三种适用机型上对其进行检测,准确性为 100%。将临床结直肠癌样本来源的 DNA,配制成不同甲基化比例的 Septin9、SDC2、BCAT1 单基因甲基化样本,在三种适用机型上对试剂盒检测的准确性进行研究,准确性为100%。
精密度的研究使用了两种不同的样本。第一种样本是精密度参考品,使用三批次试剂盒分别在三种适用的仪器上进行检测。第二种样本是临床样本混合的阴性样本池和阳性样本池样品,对三批试剂盒的批次内/间、日内/日间(20 天)、操作者间及不同实验室间的精密度进行评价。研究结果显示 Septin9、SDC2、BCAT1 和 ACTB 基因 Ct 值的变异系数均小于 10%。检测限研究,以阴性血浆样本为基质,对不同游离 DNA 浓度下含有不同比例甲基化 DNA 的血浆样本进行检测,确定血浆样本的检测限,并在三种适用机型上进行验证。结果表明在血浆 DNA 浓度为 0.02ng/µL 时,试剂盒检测 P 值为阳性的检测限为 0.2%三基因甲基化,0.5%的 Septin9 基因甲基化、2%的 SDC2基因甲基化和 0.5%的 BCAT1 基因甲基化。特异性研究的扩增产物SNP分析显示人群中的SNP位点对检测结果无影响。交叉反应研究显示,检测试剂对于发生肠转移的其它原发癌症(包括子宫内膜癌、宫颈癌)检出率较低,特异性均超过 80%,说明产品仅适用于原发性结直肠癌的检测。检测其它癌症包括胃癌、食管癌、胰腺癌、宫颈癌、子宫内膜癌的特异性均超过 80%。检测自身免疫性疾病包括红斑狼疮和类风湿性关节炎的特异性均超过 90%。检测其它肠道良性疾病包括肠腺瘤、肠息肉和肠炎样本的特异性超过 85%。在有其它基因(SHOX2 和/或 RASSF1A)甲基化的肺癌样本中,检测的特异性超过 90%。
干扰实验显示,样本中含有以下干扰物:未甲基化 DNA(150ng/ml)、胆红素(0.20mg/ml)、血红蛋白(10mg/ml)、甘油三酯(12mg/ml)、蛋白(血清白蛋白,120mg/ml)、红细胞(0.4% v/v)、K2EDTA(20mg/ml)、胆固醇(5mg/ml)、尿酸(0.235mg/ml)和葡萄糖(10mg/ml),对检测结果无影响。常见治疗药物,包括感冒药、消炎药、心脑血管疾病药、糖尿病药、胃病药、维生素、高血压药、安定药、镇痛药等在最大使用剂量范围内,不影响试剂盒对样本检测的 Ct 值及 P 值判定。
对与试剂盒配套使用的血浆样本处理试剂(核酸提取试剂,京昌械备 20180004 号,北京艾克伦医疗科技有限公司)进行了性能评估,结果表明其与市场常用的核酸提取转化试剂(Qiagen游离核酸提取和快速亚硫酸氢盐转化试剂盒)在 DNA 提取效率、重复性及抗干扰能力性能相当。试剂盒对于临床样本游离DNA 的提取效率为 85.16%,提取转化均符合进一步 PCR 检测的要求。采用精密度研究中相同样本进行了配套使用的血浆样本处理试剂的提取精密度研究,结果表明在核酸提取过程中DNA 提取量、P 值的变异系数小于 10%。
对该产品适用的三种仪器宏石 PCR 分析系统 SLAN-96P、Applied Biosystems 7500,Roche Lightcycler 480 进行了性能评估,结果显示在三种适用机型上的阴/阳性符合率、检测限、精密度均符合质量要求,可以作为该产品的适用机型。
九、Septin9/SDC2/BCAT1 基因甲基化检测试剂盒(PCR- 荧光探针法)的阳性判断值研究
艾克伦医疗采用三基因拟合 P 值公式法确定阳性判断值。每个样本进行 3 次 PCR 平行测试,计算 Septin9、SDC2、BCAT1 和ACTB 基因 3 个复孔平均 Ct 值,其中各个基因无扩增时,Ct值定义为 45.0。ACTB 基因的 Ct 值≤35.0 时,样本检测结果有效。在确定样本检测结果有效的情况下,样本 P 值≥1.2 则判断样本为阳性,样本 P 值<1.2 则判断样本为阴性。阳性判断值研究入组(训练集和验证集)有效样本数共计513 例样本,包括正常样本 237 例、结直肠癌病人样本 146 例、其它干扰样本(包括肠腺瘤、肠息肉、肠炎、胃癌、食管癌和肝癌)130 例。样本数据进行多种方法统计分析,包括 1/3 次PCR 反应 Ct 值、2/3 次 PCR 反应 Ct 值、3/3 次 PCR 反应 Ct 值、3 次 PCR 反应平均 Ct 值、单基因、两基因、三基因、三基因组合拟合公式等,比较不同分析方法的检测灵敏度、特异性、总符合率,最终确定使用三基因拟合 P 值公式法检测准确率最高。并使用测试集样本再次验证三基因拟合公式和其它阳性判断值方法,测试集研究入组有效例数 350 例样本,包括肠道正常样本 119 例、结直肠癌病人样本 106 例、其它干扰样本(包括肠腺瘤、肠息肉、肠炎、胃癌、食管癌和肝癌)125 例进行验证,结果表明三基因拟合 P 值公式法特异性为 94.67%,灵敏度为90.57%,总符合率为 93.43%。
十、Septin9/SDC2/BCAT1 基因甲基化检测试剂盒(PCR- 荧光探针法)的稳定性研究
艾克伦医疗对该产品的稳定性的研究包括长期稳定性、使用稳定性(包括开瓶稳定性、冻融稳定性和热稳定性)及样本稳定
性(包括全血、血浆及 BisDNA 的稳定性)。长期稳定性:选择三批次试剂盒置于-20±5℃冰箱中保存,在储存后的第 0、3、6、9、12、13 个月进行检测,结果显示产品在生产后 13 个月的产品性能符合技术要求,试剂性能稳定。确定产品有效期可达 12 个月。
使用稳定性:将三批试剂盒置于-20±5℃开瓶放置,分别于第 2 周、4 周和 6 周后,检测其外观、准确性、灵敏度、精密度等指标,稳定性结果 P 值及 CV 值均无显著差异,无显著变化趋势,其产品的主要性能均符合技术要求。将三批次试剂盒在规定的储存条件下,取出试剂盒反复冻融 6 次,检测每次冻融后的试剂盒的性能均符合技术要求。将三批试剂盒置于 37℃,分别于 1 天、2 天、3 天后检测产品性能,均符合技术要求。
艾克伦医疗对全血样本、血浆样本及 BisDNA 的样本稳定性进行了研究,研究结果表明使用 EDTA 抗凝管(BDVacutainer®,6mL,国械注进 20152222083)采集全血,建议选用 2~8℃放置 4 小时以内的新鲜血样分离血浆后用于检测;使用康为游离DNA 采血管(康为世纪,5mL,苏械注准 20192220059)采集全血,建议选用室温放置 4 天以内的血样分离血浆后用于检测;使用 Streck Cell free 采血管(DNA Cell-Free DNA BCT®BLOOD COLLECTION TUBE,货号 218962)采集全血,建议选用室温放置 6 天以内的血样分离血浆后用于检测。分离后的血浆样本建议在-20±5℃保存 30 天以内,在 2~8℃保存 12 小时以内进行检测;BisDNA 保存期限为在-20±5℃保存 4 天以内,在 2~8℃保存 16 小时以内进行 PCR 检测。血浆样本和 BisDNA 样本仅可冻融一次。

来源:嘉峪检测网


