您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-03-08 08:17
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtes
今日头条
礼来GLP-1的Ⅲ期临床达主要终点。礼来制药GIP/GLP-1双重激动剂tirzepatide在治疗2型糖尿病的Ⅲ期临床SURPASS-2中达主要终点。在二甲双胍的治疗背景下,tirzepatide与注射型索马鲁肽(semaglutide,1mg)相比,显著降低患者糖化血红蛋白(A1C)水平和体重。三种不同剂量(5mg,10mg,15mg)tirzepatide组治疗后达到A1C水平低于7%的患者比例分别为85.50%、88.90%和92.20%,而对照组为81.10%;患者体重分别降低7.8kg(-8.5%)、10.3kg(-11.0%)和12.4kg(-13.1%),而对照组为6.2kg(-6.7%)。此前,tirzepatide已在两项Ⅲ期临床试验中达到主要终点。
国内药讯
1.百济神州PD-1第6项适应症上市申请获受理。NMPA受理百济神州PD-1抗体百泽安®(替雷利珠单抗)用于治疗接受铂类化疗后出现疾病进展的局部晚期或转移性非小细胞肺癌(NSCLC)患者的新适应症上市申请。此项sBLA是基于一项RATIONALE 303研究的中期分析结果。百济神州将于2021年医学会议上公布该研究成果。替雷利珠单抗目前已在国内批准3项适应症,分别用于治疗霍奇金淋巴瘤、尿路上皮癌、鳞状NSCLC。还有3项适应症正在审评中。
2.新型谷氨酸盐调节剂Ⅲ期临床进展。标新公司新型谷氨酸盐调节剂troriluzole(BHV4157)治疗脊髓小脑性共济失调(SCA)的国际Ⅲ期临床BHV4157-206完成中国受试者入组。该项研究计划入组大约210例经基因检测确诊的18-75周岁SCA患者,包括基因亚型1、2、3、6、7、8和10。主要疗效终点为治疗48周时疾病进展较基线的变化(基于改良的共济失调功能评分量表进行评估)。
3.普克鲁胺治疗新冠患者Ⅲ期临床在美获批。开拓药业新一代雄激素受体(AR)拮抗剂普克鲁胺治疗轻中症新冠男性患者的Ⅲ期临床获FDA正式批准。2021年1月,开拓药业公布的一项临床数据显示,与安慰剂相比,普克鲁胺可显著抑制新冠患者自轻症至重症的转化,两组需要住院治疗的患者比例分别为0%和27%;且在研究期间未观察到药物相关严重不良事件。除了男性患者,该公司也在探索普克鲁胺治疗新冠女性患者的潜力。
4.绿叶脂质体新药申报临床。绿叶制药创新产品盐酸罗哌卡因脂质体混悬注射液的临床试验申请获CDE受理。盐酸罗哌卡因是一种新型长效酰胺类局麻药,适用于术后镇痛和产科麻醉。绿叶制药目前拥有多款脂质体在研药物,其中盐酸伊立替康氟脲苷脂质体注射液(LY01616)是一种同时包载伊立替康和氟脲苷的复方脂质体的创新药物,拟用于晚期结直肠癌的治疗。据悉,LY01616也是国内首个申报临床的复方脂质体药物。
5.君实生物高尿酸血症新药申报临床。君实生物1类新药JS103 注射液临床试验申请获国家药监局受理。JS103是一种聚乙二醇化尿酸酶衍生物,主要用于高尿酸血症伴或不伴有痛风的治疗,其可通过催化尿酸氧化成溶解度显著高于尿酸的尿囊素, 从而达到降低血尿酸的作用。目前,国内常用的降尿酸药物包括抑制尿酸合成(别嘌醇、非布司他)和促进尿酸排泄(苯溴马隆)两类。其他药物包括尿酸酶类,目前国内只有注射用拉布立海获批上市。
6.百奥泰终止三个新药项目止损。百奥泰3月4日晚间发布公告,宣布终止其Trop-2靶向抗体偶联药物(ADC)BAT8003 以及 PD-1单抗BAT1306的临床试验。BAT8003由Trop2单抗与Batansine偶联而成,拟用于治疗Trop2阳性晚期上皮癌患者。BAT8003项目终止主要基于该药与该公司另一款ADC药物BAT8001(乳腺癌III期临床失败)技术特征类似(均连接batansine),存在较高的临床开发风险;而且国内同靶点抗体项目竞争激烈。BAT1306项目终止是由于其开展的临床均为与BAT8001联用的临床试验。截至目前,百奥泰今年共终止了3个新药项目,累计已投入研发资金近3.4亿元。
7.联拓生物引进一款抗病毒候选药。联拓生物宣布与ReViral公司达成独家合作许可协议,获得ReViral候选药物sisunatovir在中国大陆、香港、澳门地区,以及新加坡共同开发和商业化权益。sisunatovir是一种用于治疗呼吸道合胞病毒(RSV)感染的小分子药物,已获FDA快速通道资格,目前正在进行Ⅱ期临床开发。根据协议,ReViral将获1400万美元的首付款,可能高达1.05亿美元的里程碑付款,以及合作产品的销售分成。
国际药讯
1.儿童多动症新药获FDA批准上市。FDA批准KemPharm复方胶囊制剂AZSTARYS(KP415)上市,用于治疗6岁及以上患者的注意力缺陷多动障碍(ADHD)。在一项III期研究(NCT03292952)中,AZSTARYS显著改善了这类患者的症状,其SKAMP-C评分(ADHD儿童课堂行为的有效评级)较安慰剂平均降低5.4分。AZSTARYS是一种复方制剂,由70%右哌甲酯(d-MPH)前药serdexmethylphenidate (SDX)和30%速释d-MPH组成。
2.罗氏托珠单抗获FDA批准治疗罕见肺病。FDA批准罗氏(ROC)旗下基因泰克IL-6抑制剂Actemra(tocilizumab)扩展适应症,用于减缓系统性硬化病(硬皮病)相关间质性肺病(SSc-ILD)成年患者的肺功能下降速度。这也是FDA批准用于这类患者的首款生物制品治疗产品。在一项Ⅲ期临床中,与安慰剂组相比,Actemra治疗组48周时患者用力肺活量(FVC)下降水平更小,两组患者FVC分别降低14毫升和255毫升。FDA此前已批准Actemra用于治疗中重度类风湿性关节炎患者。
3.创新疗法OTL38获FDA优先审评资格。FDA受理On Target Laboratories公司荧光染料OTL38注射液(pafolacianine sodium)的新药申请(NDA),并授予其优先审评资格。OTL38是一种新分子实体,通过与叶酸受体结合,在手术中可以在近红外光产生荧光,作为辅助手段给医生完全切除卵巢癌提供更大的确定性。一项发表于Gynecologic Oncology上的Ⅱ期临床结果显示,使用OTL38能够帮助医生在48.3%的患者中发现额外的肿瘤病变。
4.抗炎药filgotinib中期临床安全性数据积极。吉利德与Galapagos NV合作开发的JAK1抑制剂Jyseleca(filgotinib),在用于治疗炎症性肠病(MANTA研究)和风湿性疾病(MANTA-RAy研究)的两项研究中获良好的安全性数据。这2项研究正在评估这款抗炎药对男性患者精子参数的影响。结果显示,filgotinib治疗组与安慰剂组相比,第13周精子浓度下降≥50%的患者比例相似(6.7%vs8.3%)。完整数据预计今年年底或明年年初公布。
5.安进收购创新胃癌一线疗法。安进与Five Prime Therapeutics公司达成最终协议,将以约19亿美元的金额收购Five Prime公司并获得其临床后期抗体药物bemarituzumab。该药物是一款潜在“first-in-class”抗FGFR2b抗体疗法,其针对晚期胃癌或胃食管衔接部癌的临床已进入III期开发阶段。此前,再鼎医药已与Five Prime达成合作协议,获得这款创新疗法在大中华区的开发和商业化权益。
医药热点
1.中国疫苗无偿援助60多个国家。3月4日晚,十三届全国人大四次会议举行新闻发布会,大会发言人张业遂介绍了大会议程,并针对人大工作相关问题回答中外记者提问。张业遂介绍,中国政府已经或正在向60多个有需要的国家提供新冠疫苗无偿援助,宣布向世卫组织“新冠疫苗实施计划”提供1000万剂疫苗,用于满足发展中国家急需。
2.美国限制用于疫苗生产的原材料出口。全球最大疫苗生产商印度血清研究所和世卫组织日前同步发出警告,美国政府为“确保美国药企辉瑞优先获得生产新冠疫苗所需的原材料和关键设备”而限制疫苗原材料出口,恐将使全球新冠疫苗的生产出现瓶颈,导致产能滞后。印度血清研究所目前已获授权,负责为英国阿斯利康以及美国Novavax生产数以亿计的新冠疫苗。世卫疫苗合作伙伴、国际药品制造商协会联合会、发展中国家疫苗厂商下周将在网络会议中就此问题开展讨论。
3.瑞典报告胎儿在母亲子宫内感染新冠案例。发表于《英国妇产科杂志》上的一篇来自瑞典研究人员的最新研究表明,胎儿在母亲子宫内可以感染新冠病毒。据悉,这名孕妇在去年因急性腹痛被送到瑞典一家医院时,已有新冠疑似症状。在紧急剖宫产手术后,母亲和新生儿的新冠病毒检测均呈阳性,基因测序显示感染的病毒同源。该研究也排除了新生儿来自母亲的传染,而且对胎盘的检测中发现了大量病毒蛋白质。
4.华为副总裁出任云南白药CEO。云南白药3月5日发布公告,宣布聘任董明先生担任公司首席执行官(总裁)。据公开信息,董明,男,生于1976年10 月,学士学历。出任云南白药集团CEO之前,是华为中国区副总裁,同时也是中国虚拟现实产业联盟的副理事长。
审评动向
1. CDE新药受理情况(03月07日)
申请临床:
祐和医药的YH003注射液、君实生物的JS103注射液(高尿酸血症)、绿叶制药的盐酸罗哌卡因脂质体混悬注射液(长效酰胺类局麻药)、辉瑞的Tanezumab注射液、新基的注射用Luspatercept(2个规格)、德琪医药的ATG-016片(2个规格)、联辉医药的注射用EC-DG。
申请生产:
百济神州的替雷利珠单抗注射液(非小细胞肺癌)、雅培的雌二醇地屈孕酮片。
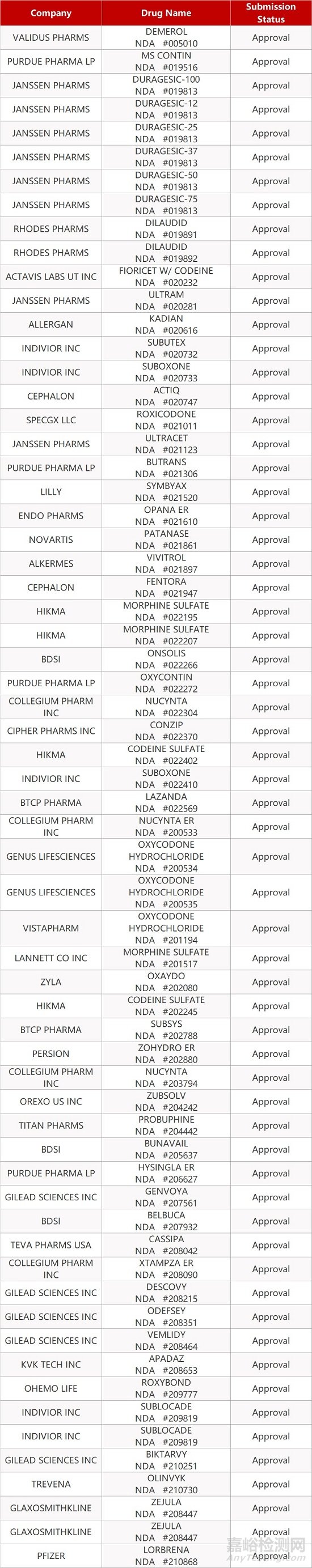
2. FDA新药获批情况(北美03月4日)
股市资讯
【金城医药】公司参与投资的上海仟德的参股公司东方略,东方略的美国合作方Inovio宣布联合研发的一项DNA治疗药物VGX-3100与器械 CELLECTRATM 5PSP联合治疗HPV-16/18相关宫颈高度鳞状上皮内病变(HSIL)的首个III期临床试验(REVEAL1)的积极结果,在全部可评估受试者中,达到临床疗效的主要终点和所有次要终点。
【拱东医疗】(1)2020年实现营收约8.3亿元,同比增长50.03%;归母净利润约2.26亿元,同比增长98.86%;扣非归母净利润约2.15亿元,同比增长95.28%。(2)公司2021年度预计与关联方浙江恒大医疗器械有限公司交易不超过1,600万元。
【药明康德】2020年实现营收约165.36亿元,同比增长28.46%;归母净利润约29.6亿元,同比增长59.62%;扣非归母净利润约23.85亿元,同比增长24.6%。

来源:药研发


