您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2019-09-03 09:09
「本文共:15条资讯,阅读时长约:3分钟 」
今日头条
FDA公布肿瘤药试验安慰剂与设盲行业指南最终版。FDA于8月28日公布肿瘤药物临床试验安慰剂与设盲的行业指南最终版。指南最终稿明确,对于恶性血液癌症和肿瘤疾病,如果存在替代治疗药物可用的情况,为避免双盲、随机对照临床试验中使用安慰剂导致的现实和伦理问题,只限于在维持性治疗,附加试验设计,辅助治疗试验,以及没有治疗药物可用的适应症的情况下设立安慰剂对照。在其他临床试验中,随机对照临床试验仍然是检测上市销售药品安全性与有效性的“金标准”
国内药讯
1.泰瑞沙在华获批一线治疗非小细胞肺癌。阿斯利康奥希替尼(泰瑞沙)获国家药监局批准,一线治疗EGFR突变阳性晚期/转移非小细胞肺癌(NSCLC)。泰瑞沙是阿斯利康研发的第三代口服、不可逆的选择性EGFR突变抑制剂,是全球首个上市,也是我国首个获批的用于EGFR T790M突变阳性的局部晚期/转移非小细胞肺癌的肿瘤药物。一项比较泰瑞沙与第一代EGFR靶向药(标准疗法)的FLAURA研究显示,与标准疗法相比,奥希替尼组患者的中位无进展生存期显著延长8.7个月,达18.9个月;中位缓解持续时间为17.2个月,标准疗法组为8.5个月;客观缓解率为80%,标准疗法组为76%。
2.博际生物IL-15融合蛋白在美获批临床。博际生物自主研发的首款肿瘤靶向性IL-15融合蛋白(BJ-001)获FDA临床批件。IL-15是一种多效能细胞因子,在NK细胞、T细胞和B细胞的发育、存活和活化中起着核心作用,重组IL-15已在动物试验中被证明具有抗肿瘤作用,且在人体首次试验中被证明在黑色素瘤的肺转移中有疗效。据悉,博际生物的BJ-001可克服重组IL-15半衰期短的缺点,其肿瘤靶向性可使IL-15在靶点高表达的肿瘤中富集,降低系统毒性并增强疗效。此外,IL-15可在肿瘤局部增殖淋巴细胞,将提高现有肿瘤免疫治疗药物的治疗效率。
3.亚宝药业婴儿血管瘤药物拟纳入优先审评。亚宝药业β-受体阻断药盐酸普萘洛尔的上市申请拟纳入优先审评公示名单。该药拟用于需要系统治疗的增殖性婴儿血管瘤。2014年3月,Pierre Fabre公司口服盐酸普萘洛尔(Hemangeol)获FDA批准用于治疗需予全身疗法的增殖期婴儿血管瘤患者,是首个也是唯一一款用于该适应症的药物。一项Ⅱ/Ⅲ期临床显示,在接受Hemangeol每日口服3mg/kg治疗6个月婴儿患者组中,60.4%的患者的目标血管瘤获完全或几近完全的消退。但在停止治疗后,11.4%的婴儿需再次接受治疗。不过,该药也有一些常见副作用,甚至可能引起低血糖症等严重副反应。
4.科济生物CAR-T产品获FDA孤儿药资格。科济生物自主研发的全人BCMA CAR-T细胞(CT053)获FDA授予治疗多发性骨髓瘤的孤儿药资格。一项探索性Ⅰ期临床数据表明,CT053具有积极的临床疗效和良好的安全性。在24例复发难治的多发性骨髓瘤患者中,有19例达完全缓解(完全缓解率79.2%),且无3级及以上细胞因子释放综合征。科济生物将在国际多发性骨髓瘤研讨会(IMW2019)会议上口头报告该项研究结果。CT053目前也正在中国进行注册临床研究。
5.华领医药糖尿病新药dorzagliatin联合用药的临床进展。华领医药在研糖尿病新药dorzagliatin(HMS5552)与二甲双胍联用的Ⅲ期临床完成受试者入组。Dorzagliatin是一款糖尿病创新口服药物,旨在通过对2型糖尿病患者血糖传感器葡萄糖激酶的功能修复,重塑人体血糖稳态平衡,控制渐进性退变性疾病发展,达到治疗2型糖尿病的目的。该研究将在2型糖尿病患者中评估dorzagliatin与二甲双胍联合用药对比二甲双胍单药治疗的疗效与安全性。预期2020年第二季度公布最新试验结果。
6.智飞生物组份百白破疫苗获批临床。智飞生物吸附无细胞百白破(组份)联合疫苗(百白破疫苗)获国家药监局临床批件。百白破疫苗是针对百日咳、白喉、破伤风三种疾病的联合疫苗,分为全细胞百白破疫苗(DTwP)和无细胞百白破疫苗(DTaP)。其中DTwP预防接种后的副反应较多、较严重,国内已不再使用。智飞生物的吸附无细胞百白破(组份)联合疫苗是新一代的无细胞百白破疫苗,采用单独纯化的百日咳有效组份配制出的质量均一疫苗产品。
国际药讯
1.中外制药Kadcyla在日本提交上市申请。罗氏制药旗下中外制药的HER2靶向药物Kadcyla(trastuzumab emtansine)在日本提交上市申请,用于接受新辅助(术前)治疗后存在残留浸润性疾病的HER2阳性早期乳腺癌患者的辅助(术后)治疗。一项III期临床KATHERINE结果显示,与赫赛汀辅助治疗相比,Kadcyla辅助治疗将浸润性乳腺癌复发或全因死亡风险(无浸润性疾病生存,iDFS)显著降低50%(HR=0.50,95%CI: 0.39-0.64,p<0.0001);在治疗3年时,Kadcyla治疗组有83.3%的患者乳腺癌没有复发,赫赛汀治疗组为77.0%,绝对改善为11.3%;Kadcyla在总生存方面没有优于赫赛汀。
2.阿斯利康替卡格雷III期临床THEMIS结果公布。阿斯利康抗凝血剂Brilinta(替卡格雷)公布III期临床THEMIS完整数据。该研究在无心肌梗塞或中风病史且合并冠状动脉疾病的2型糖尿病患者中评估Brilinta联合阿司匹林与单用阿司匹林对主要不良心血管事件(MACE)的影响。结果显示,与单用阿司匹林相比,Brilinta合用将MACE相对风险降低10%,有统计学意义。合用组中虽有较低的心肌梗塞和中风发生率,但安全性方面增加了颅内出血风险。
3.诺华Entresto最新心衰Ⅲ期研究未达终点。诺华心血管药物Entresto Ⅲ期Paragon-HF试验未达主要终点。4822例左心室射血分数正常的心衰(HFpEF)患者接受Entresto或缬沙坦治疗,结果显示,尽管与缬沙坦相比,Entresto将患者的心力衰竭住院率和心血管死亡率降低13%,但数据不具统计学意义的差异。不过诺华表示,Entresto在较小的亚组中显示出能够提高患者生活质量以及带来肾功能方面的改善。Entresto是缬沙坦和脑啡肽酶抑制剂sacubitril的复方组合,此前已获批用于治疗左心室射血分数下降心衰患者。
4.Viela Bio拟IPO。生物技术公司Viela Bio递交IPO申请拟融资1.5亿美元,用于主打产品inebilizumab的开发和推广,以及用于在研融合蛋白VIB4920和处于早期研究阶段的抗ILT7单抗VIB7734的临床开发。Viela Bio公司去年初从MedImmune公司脱离正式成立。该公司抗CD19单抗inebilizumab拟用于治疗视神经脊髓炎谱系疾病(NMOSD)患者的上市申请刚被FDA受理,有望明年上半年得到回复。Viela公司还计划在下半年以及明年分别开展inebilizumab用于治疗肾移植脱敏和治疗重症肌无力的临床研究。此外,明年还将开展VIB4920治疗干燥综合症和肾移植排斥反应的Ⅱ期试验。
5.Cognate BioServices完成新一轮融资。生物技术公司Cognate 完成新一轮融资,投资方为EW Healthcare Partners。此轮融资Cognate公司将用于进一步开发并商业化如CD-Tcar-T、NK细胞、TIL和MIL等细胞免疫治疗产品,并完善商业制造基础设施,扩大其客户和潜在客户范围。Cognate公司成立于2002年,致力于为从事细胞产品开发的公司和机构提供全面的临床试验和制造服务,是目前少数能够开发个性化产品的合同开发和制造组织(CDMO)之一。
医药热点
1.首批儿童血液病定点医院公布。国家卫健委医政医管局印发《关于公布第一批全国儿童血液病定点医院和恶性肿瘤(实体肿瘤)诊疗协作组的通知》。100多家医院成为第一批全国儿童血液病定点医院,同时,成立70多个儿童恶性肿瘤(实体肿瘤)诊疗协作组。《通知》要求,组建专家组、完善医疗质量控制管理制度以及建立动态调整机制,确保定点医院、诊疗协作组能力水平满足诊疗需求;诊疗协作组要明确组内牵头单位和成员单位职责,完善协作制度流程,为患儿提供全周期、连续性诊疗服务。
2.河南脑卒中患者救治时间再“提速”。河南省人民医院、河南省脑血管病医院一站式多模态影像卒中救治平台正式启动运行。据了解,“一站式多模态影像卒中救治平台”采用“诊疗零距离”设计理念,以最短的路径和稳定的手术系统,缩短救治时间,降低治疗风险。该平台将患者从入院到介入治疗时间由原来的70分钟上下降至15分钟。同时,此次启用的一站式卒中解决方案,将CT、磁共振和血管造影机置于同一个手术室,使脑卒中患者可获得真正的无缝隙院内抢救。
3.浙江:基层公立医疗机构使用基药金额比例不低于40%。浙江省卫健委等七部门发布完善国家基本药物制度的实施意见。意见要求,《国家基本药物目录》内的药品为浙江各级公立医疗机构临床诊疗的首选药品,应全面配备、优先使用。三级甲等综合医院及中医医院采购使用基本药物的总金额,不少于本单位采购使用全部药品总金额的20%,三级乙等医院不少于25%,二级甲等医院不少于30%,二级乙等医院及基层医疗机构不少于40%。
【贝达药业】盐酸恩沙替尼药品注册临床试验数据更新。
【一品红】截止2019年8月31日,公司累计以集中竞价交易方式回购公司股份118.15万股,占公司现有总股本的0.73%。
【普利制药】公司股东瑞康投资减持计划时间过半,已累计减持154.24万股公司股份,减持比例为0.56%。
审评动向
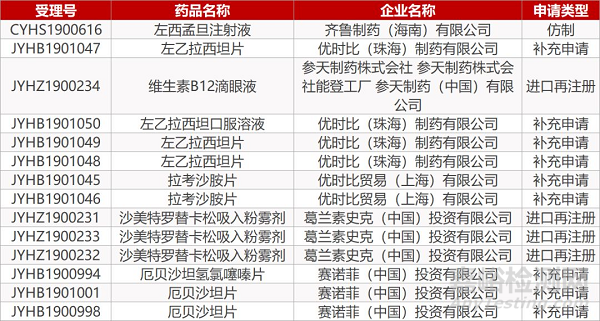
1. CDE最新受理情况(09月02日)
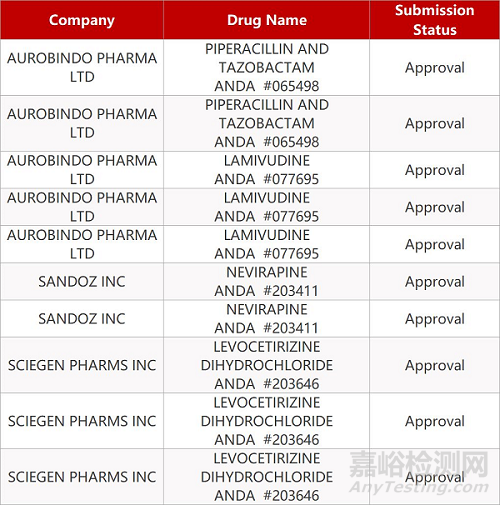
2. FDA最新获批情况(北美09月01日)

来源:药研发


