今日头条
科济骨髓瘤CAR-T获批上市。科济药业BCMA靶向CAR-T产品赛恺泽®(泽沃基奥仑赛注射液,CT053)获国家药监局批准上市,用于治疗既往经过至少3线治疗后进展的复发或难治性多发性骨髓瘤成人患者。公布于《Haematologica》上的IIT试验结果显示,中位随访为17.4个月时,总缓解率达到87.5%,其中完全缓解率为79.2%。此前,该新药已获FDA和EMA授予孤儿药资格、再生医学先进疗法以及优先药物。
国内药讯
1.辉瑞湿疹新药获批用于青少年。辉瑞JAK1抑制剂阿布昔替尼片获国家药监局批准新适应症,用于治疗难治性中重度特应性皮炎青少年(12-18岁)患者。在国际III期JADE TEEN研究中,与安慰剂组相比,阿布昔替尼组(100mg和200mg)患者(12-18岁)实现IGA为0/1的比例更高(41.6%和46.2%,vs24.5%),达到EASI-75应答的患者比例也更高(68.5%和72.0%,vs41.5%)。此前,该产品已获批用于治疗难治性、中重度特应性皮炎成人患者。
2.普米斯免疫双抗拟纳入突破性疗法。普米斯PD-L1/VEGF双抗PM8002获CDE拟纳入突破性治疗品种,联合注射用白蛋白结合型紫杉醇一线治疗不可手术的局部晚期/复发转移性三阴性乳腺癌(TNBC)。在Ib/II期临床中,PM8002治疗总缓解率达到78.6%,疾病控制率(DCR)为95.2%。去年11月,普米斯公司已将PM8002在全球(大中华区除外)的开发、生产和商业化权利授予BioNTech公司。
3.BMS两款新药拟纳入突破性认定。百时美施贵宝PD-1抑制剂Opdivo(纳武利尤单抗)和CTLA-4抑制剂Yervoy(伊匹木单抗)两款新药获CDE拟纳入突破性治疗品种,拟定适应症为,Yervoy联合Opdivo一线治疗不可切除或转移性微卫星高度不稳定性(MSI-H)或错配修复缺陷型(dMMR)结直肠癌患者(mCRC)。在III期CheckMate-8HW研究中,Opdivo+Yervoy联合治疗较化疗将疾病进展或死亡风险降低79%(HR:0.21;95% CI:0.14-0.32;p<0.0001)。
4.南京尧唐基因编辑药物获批临床。尧唐生物(YolTech Therapeutics)1类生物制品YOLT-201注射液获国家药监局临床许可,拟开发用于治疗转甲状腺素蛋白淀粉样变性(ATTR)。这是该公司自主研发的首个体内基因编辑药物,采用脂质纳米颗粒(LNP)递送技术,旨在人肝脏中实现高效特异的TTR靶基因敲除,有望一次给药终身降低血液中的TTR蛋白水平。
5.星眸眼科双靶点基因疗法获批IND。星眸生物自主研发的首款基因治疗药物XMVA09注射液获国家药监局临床许可,拟用于治疗湿性年龄相关性黄斑变性(wAMD)。XMVA09同时靶向血管内皮生长因子(VEGF)和血管生成素-2(ANG-2)双靶点,并采用全新的AAV衣壳,通过玻璃体腔内注射即可感染到紧贴脉络膜病灶的视网膜色素上皮层(RPE)细胞,以改善患者视力。
国际药讯
1.强生c-Met/EGFR治疗肺癌获FDA完全批准。强生EGFR/c-Met双抗Rybrevant(amivantamab)获FDA完全批准,联合化疗(卡铂和培美曲塞)一线治疗确认带有EGFR外显子20插入突变、局部晚期或转移性非小细胞肺癌(NSCLC)患者。2021年5月,Rybrevant针对这一适应症已获得FDA加速批准上市。在Ⅲ期验证性PAPILLON试验中,与单纯化疗相比,Rybrevant联合化疗显著改善患者的无进展生存期(PFS),将疾病进展或死亡风险降低61%。
2.Cardiff公司结直肠癌新药Ⅱ期临床积极。Cardiff Oncology公司第三代口服PLK1抑制剂onvansertib治疗RAS突变转移性结直肠癌(mCRC)患者的Ⅱ期临床试验ONSEMBLE获得了最新的积极数据。在未曾接受过VEGF抗体bevacizumab治疗的患者中,onvansertib(20mg和30mg)加入标准疗法FOLFIRI与bevacizumab的组合方案,与标准疗法FOLFIRI联合bevacizumab组合相比,患者的客观缓解率(ORR)更高(50%vs0%);并且药物安全性良好。
3.Biomind公司老年痴呆新药Ⅱ期临床积极。Biomind Labs基于致幻化合物5-MeO-DMT开发的舌下给药制剂BMND08,在用于治疗阿尔茨海默病相关抑郁和焦虑的Ⅱ期临床获得了积极结果。第5周时,BMND08(12mg)治疗达到了100%的应答率,患者在状态焦虑(STAI-S)、抑郁(BDI-II)和压力(DASS STRESS)量表上的减少均具有统计学显著性。该公司计划寻求FDA的突破性疗法认定。
4.FogPharmag融资开发FIC新药。FogPharmag公司宣布完成1.45亿美元的E轮融资,以用于支持其潜在“first-in-class”药物FOG-001的持续临床开发。FOG-001是一款由FogPharma专有Helicon平台所开发出的细胞内β-catenin抑制剂,目前正在Ⅰ/Ⅱ期研究中评估其治疗实体瘤的潜力。此轮融资还将加速其独特发现项目组合的开发,深化其数据科学能力并加强其核心Helicon治疗平台的开发。
5.Kenai公司融资加速帕金森病iPSC疗法。致力于神经系统领域开发诱导多能干细胞(iPSC)药物公司Kenai宣布完成8200万美元的A轮融资,用于推进其主要候选疗法RNDP-001提交IND申请,并完成Ⅰ期临床。RNDP-001是一款同种异体多巴胺前体细胞疗法,拟开发用于治疗特发性和遗传性帕金森病。在临床前研究中,RNDP-001已在帕金森病动物模型中显示出良好的存活率、神经支配和行为恢复的潜力。
6.Minerva公司精神分裂症新药上市遭拒。Minerva公司5-HT2A/σ2受体拮抗剂Roluperidone用于治疗精神分裂症阴性症状的新药申请(NDA)再次收到FDA完整回复函(CRL)。FDA要求,Minerva必须提供Roluperidone额外临床数据,进一步证实Roluperidone与其他抗精神病药物对比的安全性和有效性;以及Roluperidone与其它抗精神病药物联合用药的安全性和有效性。此前,该新药已两次被FDA拒绝批准。
医药热点
1.河北省互联网医院管理办法实施细则出台。河北省卫健委结合实际制订发布《河北省互联网医院管理办法实施细则》。《细则》提出,互联网医院要加强内部管理,严格遵守医疗质量、患者安全、网络安全、信息安全等相关法律法规和规定;互联网诊疗信息系统应与省级监管平台对接,满足对互联网诊疗服务全过程监管需要;互联网诊疗实行实名制,患者有义务向医疗机构提供真实信息和病历资料。
2.AZ在无锡新建小分子药物工厂。3月1日,阿斯利康宣布,与无锡国家高新技术产业开发区管理委员会正式签署无锡小分子药物新工厂投资合作协议,将在无锡高新区投资4.75亿美元新建小分子药物工厂,预计未来在国内上市的阿斯利康特定小分子药物将在无锡新工厂实现从制剂到包装的生产,并供应国内外市场。
3.超加工食品或增加30多种健康隐患。近日,《英国医学杂志》发表的一项新研究显示,吃过多的超加工食品可能对多个身体系统有害。许多证据一致表明,与超加工食品密切相关的健康隐患竟多达32种,包括癌症、重大心肺疾病、精神健康障碍和过早死亡。超加工食品包括包装烘焙食品、零食、碳酸饮料、含糖谷类和即食或加热食品,经过多种工业流程处理,通常含有色素、乳化剂、香料和其他添加剂。这些产品往往高糖、高脂、高盐,但维生素和纤维含量较低。
4.韩国孕妇可随时鉴定胎儿性别。2月28日,韩国宪法法院以6比3的投票结果裁定,禁止医务人员在妊娠32周前向孕妇或其家属告知胎儿性别的现行《医疗法》第20条第2项违宪,判决即刻生效。这代表韩国孕妇今后可随时鉴定胎儿性别。韩国宪法法院认为,限制妊娠32周前鉴定胎儿性别的做法已不再合理,这侵害了父母得知胎儿性别等信息的权利。
评审动态
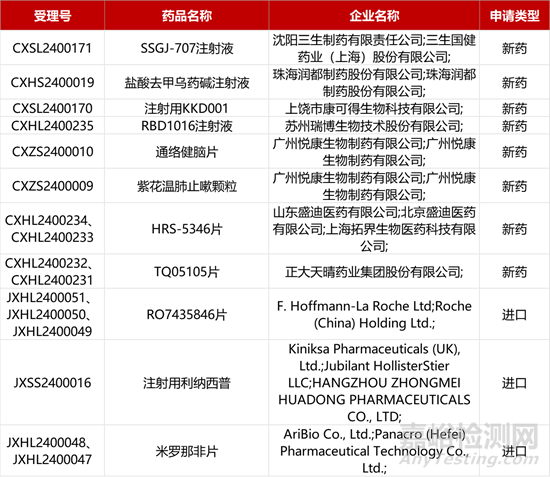
1. CDE新药受理情况(03月02)
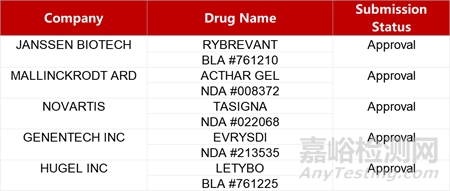
2. FDA新药获批情况(北美03月01日)