您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-08-04 11:27
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.CLL-1靶向CAR-T白血病临床积极。南开大学附属第一中心医院赵明峰团队与南开大学生命科学学院张宏恺团队联合开发的靶向CLL-1的CAR-T疗法,在《Journal of Hematology & Oncology》上发表用于治疗成人复发难治性急性髓细胞白血病(R/R AML)的的首次临床试验积极结果。数据显示,CLL-1-CAR-T达到70%完全缓解率;中位随访为173天(15-488天)时,总生存率为60%。药物总体耐受性良好,虽然可能出现严重的粒细胞缺乏,但CLL-1 CAR-T细胞为这类患者提供移植前达到完全缓解的机会。
2.先为达GLP-1药物糖尿病II期临床积极。杭州先为达开发的GLP-1药物XW003(Ecnoglutide)用于治疗2型糖尿病(T2D)的II期临床达到主要研究终点。XW003(0.4mg、0.8mg和1.2mg)治疗组患者20周后的HbA1c与基线相比分别降低1.8%、1.9%和2.4%,而安慰剂组患者这一数值为0.5%(P<0.0001);1.2mg XW003队列中达到HbA1c≤7.0%患者比例为88%(vs21%),达到HbA1c≤6.5%患者比例为72%(vs9%);XW003还能剂量依赖性降低患者的体重,并改善多个代谢和心血管疾病相关参数。此外,药物的总体耐受性良好。
3.恒瑞KRAS G12D抗肿瘤药获批临床。恒瑞医药开发的1类化药HRS-4642注射液获国家药监局临床试验默示许可,拟用于KRAS G12D突变晚期实体瘤的治疗。目前该新药靶点尚未披露。据统计,目前全球范围内的26个KRAS G12D靶点新药项目中,11个有国内企业参与,包括7个化药,2个PROTAC,2个TCR-T;除医院开发的TCR-T之外,仅北京智康博药的CTB-02获批临床,其他国内企业项目均处于临床前状态。
4.凌科新型激酶抑制剂获批皮炎临床。凌科药业新型激酶抑制剂LNK01004获国家药监局临床试验默示许可,拟用于特应性皮炎的治疗。LNK01004在体内外可同时抑制多个细胞因子诱导的信号通路;而且LNK01004具有组织限制性的特点,可潜在地避免系统暴露而带来的安全性问题。该新药此前已获批开展用于轻中度斑块型银屑病患者的临床试验,目前这项Ⅰ期临床已完成首批受试者给药。
5.硕迪拟加速推进口服GLP-1R小分子开发。硕迪生物宣布,在2021年10月完成的1亿美元B轮融资的基础上,获得了3300万美元的超额认购。此次扩展融资包括新投资者Deep Track Capital和Piper Heartland Healthcare Capital。硕迪生物管线中共6款在研药物,其中口服小分子GLP-1R激动剂GSBR-1290进展最快,正在开展Ⅰ期临床,适应症为2型糖尿病和肥胖症患者。目前,全球共10款GLP-1R多肽药物上市,但尚无口服GLP-1R小分子药物上市。
国际药讯
1.FDA批准乌司奴单抗用于儿童银屑病关节炎。强生旗下杨森IL-12/IL-23抑制剂乌司奴单抗(Stelara)获FDA扩大适应症,用于治疗6岁及以上活动性银屑病关节炎(PsA)的儿童患者。IL-12/IL-23信号通路在多种免疫介导的慢性炎症性疾病中发挥关键作用。目前,FDA已批准Stelara用于治疗中重度斑块状银屑病的成人和六岁及以上的儿童患者;活动性银屑病关节炎的成人和六岁及以上儿童;中重度活动性克罗恩病的成人患者;中重度活动性溃疡性结肠炎的成人患者。
2.三萜类抗真菌药sNDA获FDA优先审评。FDA受理SCYNEXIS公司新型抗真菌药物Brexafemme的补充新药申请(sNDA),用于预防复发性外阴阴道念珠菌病(RVVC)。FDA同时授予其优先审评资格,PDUFA日期为2022年11月30日。Brexafemme是一种三萜类的新型口服抗真菌药,能够通过抑制葡聚糖合酶杀死念珠菌属的真菌。此前它已被FDA批准用于治疗患有VVC的成人和初潮后的女童患者。
3.CD47抑制剂/K药组合获FDA快速通道资格。ALX Oncology制药公司CD47抑制剂evorpacept获FDA快速通道资格,联合PD-1单抗Keytruda一线治疗PD-L1阳性晚期头颈部鳞状细胞癌(HNSCC)。在一项I期临床ASPEN-01中,这一组合在未接受过检查点抑制剂治疗的二线或以上晚期HNSCC患者中达到40%的客观缓解率。该项结果支持2021年5月与默沙东合作启动的随机、开放标签的III期ASPEN-03研究,旨在评估evorpacept与Keytruda联合治疗用于上述适应症。
4.抗肿瘤组合疗法公司IDRx完成A轮融资。IDRx公司宣布完成1.22亿美元的A轮融资。IDRx致力于开发创新组合疗法,高效靶向肿瘤的驱动基因突变,以及覆盖耐药性信号通路,以帮助肿瘤患者获得更持久的缓解。IDRx研发管线目前包含两款小分子酪氨酸激酶抑制剂(IDRX-42和IDRX-73),它们旨在抑制非PDGFR驱动的胃肠道间质瘤(GIST)中的关键遗传驱动因子和耐药性突变。此前,IDRX-42已获得FDA授予用于GIST的孤儿药资格。
5.吉利德2022H1业绩公布。8月3日,吉利德公布2022年上半年财务报告,上半年总收入128.50亿美元,同比增长1%,其中产品收入126.72亿美元,同比增长2%。2022年上半年,HIV药物收入79.35亿美元(+5%);HCV药物收入8.47亿美元(-20%);TROP-2 ADC药物Trodelvy收入3.05亿美元(+90%);细胞疗法(Yescarta和Tecartus)收入6.42亿美元(+57%);Veklury(瑞德西韦)收入19.80亿美元(-13%)。
6.NKG2A抑制剂头颈鳞癌III期临床失败。Innate Pharma与阿斯利康联合开发的NKG2A抗体monalizumab和cetuximab(西妥昔单抗)构成的组合方案,在用于治疗既往接受过含铂化疗和PD-(L)1抑制剂治疗的复发或转移性头颈部鳞状细胞癌(R/M SCCHN)的III期临床(INTERLINK-1)未达到主要研究终点。与西妥昔单抗相比,联合方案未能在这类患者中达到预先设定的疗效阈值。阿斯利康目前已宣布终止该项研究。
医药热点
1.山东肾脏病专科联盟正式成立。7月30日,山东第一医科大学附属省立医院(山东省立医院)肾脏病专科联盟成立大会在潍坊召开,省立医院肾脏病专科联盟正式成立,共有86家成员单位。肾脏病专科联盟成立后,山东省立医院肾内科将依托各级医院资源,与各联盟成员单位实现“共建、共享、共赢”,在医、教、研各方面共同进步、共同发展,促进山东省肾脏病诊疗标准化、规范化。
2.西安市儿童医院庞贝病MDT成立。近日,西安市儿童医院庞贝病多学科诊疗中心(庞贝病MDT)正式成立。庞贝病是一种罕见的常染色体隐形遗传的溶酶体贮积症,可导致心血管、神经肌肉、呼吸系统等多脏器受累, 且临床表现差异性大,目前确诊率普遍较低。庞贝病MDT成立旨在为广大庞贝病患儿打造疾病筛查、诊治、康复一站式服务平台,为更多罕见病患儿带来康复的希望。
3.新冠导致糖尿病风险提高81%。2022年7月19日,英国伦敦国王学院研究团队在Plos Medicine发表的最新研究成果显示,早期COVID-19感染导致糖尿病病例增加了81%,并在感染后4至12周内保持在27%;早期COVID-19感染与总体心血管疾病病例增加6倍相关,其中肺栓塞增加11倍,房性心律失常增加6倍,静脉血栓形成增加5倍;心血管疾病病例在感染COVID-19 4至12周后下降,并在感染后12周至1年内恢复到基线水平或以下。
评审动态
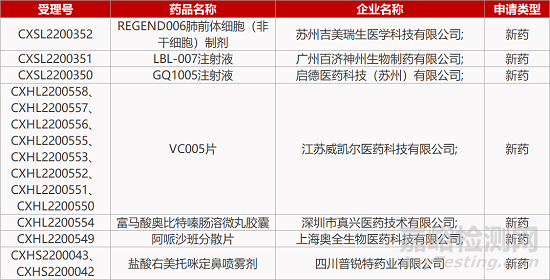
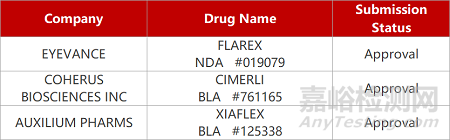

来源:药研发


