您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2021-09-28 23:36
内容提要:随着医用电气设备安全通用标准GB 9706.1-2020 在国内的发布和即将实施,高频手术设备相关的专用安全标准IEC 60601-2-2 最新版本第6.0 版标准在国内的转化也即将提上日程。现结合高频手术设备的实际特性,解读IEC 60601-2-2 第6.0 版与GB 9706.4-2009(等同采用IEC 60601-2-2 第4.0 版)在条款内容上的差异,以期有助于加深对标准的理解,保障该标准的顺利转化及实施。
关 键 词:IEC 60601-2-2 高频手术设备 GB 9706.4 差别解读
随着医疗科技的发展,医疗器械发展迅猛,不管是沿海还是内陆,医疗器械生产厂家不断增加,医疗器械在临床的使用也多样化。近年来,微创手术以“创伤小、恢复快”等优点,被越来越多的医生与患者接受。高频/ 射频类手术设备作为微创手术中常用的设备之一,发展也尤其快速,广泛应用于普通外科、胸外、脑外、五官科和颌面外科等手术中。但高频/ 射频手术设备生产使用风险较高,在医疗器械分类目录中管理类别多为Ⅲ类,因此,对高频/ 射频手术设备的生产、使用和监管环节有很高的要求。GB 9706.4-2009[3]是我国目前现行的高频手术设备安全专用要求,该标准用于规范高频手术设备的生产设计、上市前的注册检验及上市后的监管等各个环节。但GB 9706.4-2009等同采用的是国际标准IEC 60601-2-2:2006。随着GB 9706.1-2020的发布(修改采用国际标准IEC 60601-1:2005/AMD1:2012),接下来会有一系列配套的专用标准会面临配合第三版通用标准的转换工作。高频手术设备安全专用标准也是其中的一个。本文将简述IEC 60601-2-2 的发展及在我国的转化历程,重点解读最新国际标准IEC 60601-2-2:2017(第6.0 版本)[1] 和GB9706.4-2009 的差异,并探讨这些差异可能对高频手术设备设计、检测等环节产生的影响,以期使医疗器械相关生产和监管人员更全面深入地了解IEC 60601-2-2:2017版本的主要变化,为该标准的转化及平稳顺利实施提前做好准备。
1. IEC 60601-2-2的发展及在我国的转化历程
IEC 60601-2-2 在1982 年1 月1日发布第1.0版。国内并没有对1.0 版本的IEC 60601-2-2 进行转化,而是在1991 年10月31 日国际电工委员会发布IEC 60601-2-2 的2.0 版本后,经过8 年的时间,我国对2.0 版本进行了第一次的等同转换,并在1999 年8 月2 日发布GB 9706.4-1999,从1.0 版本的发布到2.0 版本在国内的成功转换,历时约18 年,但本标准的发布意义重大,这意味着我国从1999 年开始高频/射频类手术设备有了专用的国家标准要求。随后在1998 年、2006 年国际电工委员会又发布了IEC 60601-2-2的3.0、4.0版本。目前我国现行的高频手术设备安全专用标准GB 9706.4-2009 就是对IEC 60601-2-2第4.0版本的等同转换。但是目前国际上最新的IEC 60601-2-2是2017年发布的6.0版本。图1展示了IEC 60601-2-2 的发展及在我国的转化历程。
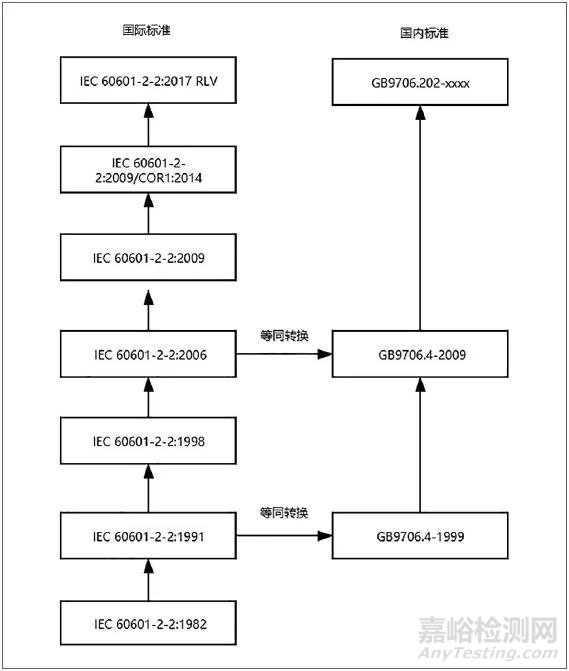
图1. IEC 60601-2-2 的发展及在我国的转化历程
2. IEC 60601-2-2第6.0版和GB 9706.4-2009(IEC 60601-2-2第4.0)的主要差异
2.1 IEC 60601-2-2第6.0版章节号与GB 9706.4-2009版本的编排区别
在IEC 60601 系列3.0 版以后的标准中,章节号与此前的版本编排有所区别。在专用标准的编号前面增加“201”(比如本标准中的201.1 对应于通用标准中的第一章);适用的并列标准增加前缀“20x”,这里x 指的是并列标准文档的最后一位数字。
下面以IEC 60601-2-2 第6.0 版的章节为基础,将从以下几个角度重点介绍与第GB 9706.4-2009(IEC 60601-2-2第4.0版)的重大技术更改。
2.2 完善和新增所界定的术语
新增201.3.218 Heating factor 发热因子:此定义在GB9706.4-2009(IEC 60601-2-2 第4.0 版本)的附录A中出现过,在6.0 版本中把该定义放到了正文中,可以理解为每欧姆阻抗所耗散的能量,用来描述中性电极在一个有限的时间内受到的热应力。
新增201.3.219 High current mode大电流模式:在最大的工作周期和最大的输出电流下,预期使发热因子在任意60s内超过30A 2s的单极输出模式。
新增201.3.222 HF Patient circuit高频患者电路:包含一个或多个患者连接的任何电路,包括高频手术设备的任何导电部分和在正常状态和单一故障状态下有高频电流在医疗设备和患者之间流通的附属设备电路。
新增201.3.226 maximum output current 最大输出电流:对于每一个高频手术模式,在预期使用时高频输出电路的最大值。主要用于计算最大的发热因子。
修改完善201.3.208 双极:一种在两个或多个手术电极之间向患者施加高频电流的方法,不需要单独连接中性电极,其中一个或多个手术电极附近的组织将产生效果。
修改完善201.3.210 凝(固):使用高频电流来产生热效应,以控制或防止出血、引起组织破坏或引起组织收缩。增加注2:电灼、干凝、喷凝、强凝、快凝、软凝和氩束(等离子体)凝固都是凝固类型的名称。
修改完善201.3.231.2 Rated accessory voltage额定附件电压双极和单极分开定义。
2.3 完善和新增对使用说明书和技术说明书的要求
对使用说明书和技术说明书的要求,完善内容如下:① 201.7.9.2.2.101a)10)有导电植入物的患者,由于高频电流的聚集或者重定向可能会有风险。若有疑问,要给出适合有效的建议。② 201.7.9.2.2.101b) 警告:高频手术设备运行时产生的干扰可能对其他电子设备的运行有不利影响。比如对于携带心脏起搏器或者其他有源植入物的患者,因为对起搏器的工作的干扰或者损坏起搏器,患者可能会有风险。如有疑问应给出合适的有效的建议。③ 201.7.9.2.2.101i) 使用说明书中应有高频手术设备对于每一个连接类型的手术附件及电缆的最大允许的长度。④ 201.7.9.2.14e)对于附属设备和手术附件包括单独提供的零部件,要给出额定的附件电压,同时要给出警告高频手术设备的峰值输出电压不能大于额定附件电压。
新增内容如下:①201.7.9.2.14j)对于手术电极和手术手柄,评估以下危险情况的信息:连接到手术手柄的手术电极的明显外露的金属;手术手柄和手术电极之间的电气连接不良的情况;手术手柄和手术电极适配不良的情况。②对技术说明书的要求201.7.9.3.1 新增两个条款:其一,每一个高频手术模式要给出最大输出电流;其二,在任意60s 内,高频手术设备在任何高频电流模式下产生的最大发热因子。
2.4 增加风险分析和基本性能条款
IEC 60601-2-2 的6.0 版本配套的通用标准是IEC 60601-1:2005/AMD1:2012(第三版),并对通用标准进行补充、修改、替换和完善等,配合第三版通用标准使用。第三版通用标准引入了基本性能及风险管理的新理念,对世界各国的医疗器械监管和产业都产生了较大影响[2]。第三版通用标准最大的革新是安全理念的变化,扩大了安全的范围和概念,给了企业更大的自由和设计空间,通过引入风险管理的流程,要求企业在产品的整个生命周期内进行风险控制,风险控制的范围扩大到基本安全和基本性能[2]。因此在IEC 60601-2-2 的6.0 版本中也有风险分析的相应要求,201.4.2.3.101 中要求制造商应在其风险分析中应包含高频手术设备和/ 或高频手术附件在大电流模式下使用的潜在可能性,以及这对中性电极的发热有什么影响。另外,201.4.3 基本性能要求201.8.4.101 中性电极监测电路和201.12.4.101 大电流模式的使用需要作为基本性能进行考虑。
2.5 进一步明确高频手术设备和高频手术附件试验验证的相互独立性
在201.4.1.101 条款中,标准明确指出对于高频手术设备和高频手术附件的符合性验证应是相互独立的,除非供应商对一致性测试有特别要求。另外,条款201.7.2.10.101 指出,高频手术附件(高频附属设备除外),不要求标识BF or CF符号在附件、外包装或者随机文件中,除非风险管理文档确定了不可接受的风险。对于201.8.5.1.2患者防护措施(MOPP)该部分明确说明不适用于高频手术附件,高频手术附件的要求在201.8.8.3 手术附件的绝缘和201.15.101.4 中性电极的绝缘中已做要求和测试。201.8.8.2固体绝缘的穿透距离或薄层材料的使用指出,通标中的8.8.2a) 和8.8.2b) 不适用于高频手术附件。
2.6 对中性电极监测电路、成人中性电极的使用及中性电极的绝缘提出了新的要求
首先,6.0 版本中,条款201.8.4.101 中性电极监测电路的适用范围有所调整,在GB 9706.4-2009中标准要求为,额定输出功率大于50W的单极高频手术设备应有中性电极连续性监测器和/或接触质量监测器,但6.0 版本修改为只要有中性电极连接的高频手术设备均适用该要求,并不局限于额定输出功率大于50W。另外,在GB 9706.4-2009中标准要求必须配有中性电极连续性监测电路或接触质量监测器中的任意一种电路,但在6.0 版本中,标准允许新增一个可替代方法,只要确保中性电极不会发生不可接受的温升,则不一定需要配有中性电极连续性监测电路或接触质量监测器,但任何可替代的方法都应作为基本性能进行考虑,且通过检查制造商的风险管理文档来验证这种方式的符合性。
其次,增加了201.15.101.9 常规程序下使用的成人中性电极的相关要求:用于成人患者,或者体重超过15kg 的患者的中性电极应是可监测中性电极,这个要求不应用于大电流模式的中性电极。
为什么会提出这个新的要求?主要源于近年来不良事件监测分析发现,可监测中性电极和接触质量监测器一起使用会显著的降低热灼伤的风险。现今市面上的大部分高频手术设备都配备有接触质量监测器,然而由于不可监测中性电极允许使用且市场价格低廉,导致接触质量监测器的益处并未体现出来。所以希望通过增加该要求使这种现象能得到显著改善,也同时影响大部分临床电外科手术[1]。
但是一些特殊的应用比如小患者、大电流模式,和电容性中性电极可豁免此要求。
最后,201.15.101.4 中性电极线缆的绝缘中,修改了漏电流的限值,并增加了等效电容的要求,二者满足其一即可。
2.7 对具有或使用大电流模式的设备提出了新的要求
大电流模式是指单极输出模式的预期用途(最大输出电流和最大持续周期)产生的发热因子在任何一个60s 周期内大于30A2s 的高频手术模式。ECRI 研究表明:经尿道(TUR膀胱镜)手术中用的电流最大,持续时间最长。TUR手术中,平均电流切为680mA,凝为480mA;持续周期平均15%,最大45%[1]。最大电流700mA,持续时间60s远远超过一个膀胱镜(TUR)手术中最大可能的电流和持续时间,因此发热因子为30A2s可以作为一个保守的实验判据。
但是新临床手术要求使用比以前更高的电流和更长的激活时间。这种组合能产生大于传统中性电极(那些经过201.15.101.5 验证的)设计特性的热应力[1]。因此,201.12.4.101 中对于使用大电流模式的设备提出要求:高频手术设备应提供一种解决方案(无论是提供还是推荐),以便在大电流模式下,确保他们的中性电极能安全地处理其输出时的预期热应力,以确保不会出现不可接受的温升。为了做到这一点,对于大电流模式,201.15.101 中性电极条款应在风险管理文档中进行具体分析。且该条款应作为基本性能进行考虑。现在要求生产具有大电流模式医疗设备的制造商。
3.IEC 60601-2-2 6.0 版本主要变化项目对医疗器械检测和生产的影响
通过对比两版标准,新增和完善的相关术语可以帮助检测和生产相关人员更好的理解标准。两版本标准使用说明书和技术说明书的差异则需要生产相关人员重点关注哪些内容是需要完善和新增的内容,是否适用于自己的产品,若适用则应对说明书相关内容进行整改,以免在日后的抽验中出现不合格情况。另外,风险分析是GB 9706.4-2009中没有的内容,6.0 版本涉及到大电流模式和中性电极监测电路相关要求的具体分析,风险管理文档应进行重点的关注。最后,对成人和体重超过15kg 的患者中性电极应使用可监测中性电极的要求可能对生产也会产生重大的影响,需要相关人员重点关注。
4.小结
综上所述,IEC 60601-2-2第6.0版修改了GB 9706.4-2009(第4.0 版)中不合理的内容,增加了对高频手术设备和手术附件的一些新的要求,使得要求和试验方法更具可操作性。通过分析、比较第6.0 版和GB 9706.4-2009(第4.0 版)内容的主要差异,加深对标准的理解,随着GB 9706.1-2020在国内的发布和即将实施,IEC 60601-2-2 第6.0 版的转化也将提上日程,本文为该标准的转化提前做好充足的准备,将有助于保障该标准的顺利转化及实施,从而促进医疗器械产业的健康、快速发展。
作者:官辉 赖玉菡* 李娟
单位:四川省药品检验研究院(四川省医疗器械检测中心) (四川 成都 611731)

来源:中国医疗器械信息


