您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-02-02 07:36
本研究基于“莲蓬”的特殊生物结构,开发出内部可生长血管的3D打印支架促进骨修复。利用微流控技术制备了负载去铁胺(DFO)脂质体的GelMA微球作为“莲子”,并巧妙的与陶瓷支架——“外衣”进行物理结合,成功构建了内部血管化的3D打印支架。该复合支架在体内外具备出色的血管化和成骨能力,在骨修复领域有广阔的应用前景。
01、研究内容简介
骨组织是人体内高度血管化和钙化的系统,尽管具有自我再生能力,但因高能量创伤、严重的感染、骨肿瘤切除等原因导致大段骨缺损——缺损达到2cm以上,给社会和家庭带来沉重的负担。骨缺损内部血供不足,进而导致骨组织缺血、骨坏死和骨丢失,最终导致骨不连。组织工程在骨再生或替代中发挥了重要的作用,但如何在骨组织工程支架的内部迅速有效地生成结构良好的血管网,是多年来研究和临床面临的一大挑战。3D打印支架,不仅完美解决了对于不同形态骨缺损模型的加工问题,还可以精确地控制材料的整体特性,准确的模拟松质骨的孔径和孔隙率,被认定为构建仿生组织工程支架的有效手段。然而,3D打印支架内部血管一直是困扰3D打印支架在骨修复领域的难题。
“莲蓬”是埋藏莲花雌蕊的海绵质的花托,花托表面具有多数蜂窝状孔洞,每一个孔洞内生有1枚小坚果即为“莲子”,基于这种特殊的生物结构及骨缺损修复过程中内部血管化的启发。近期,山东大学附属济南市中心医院龚维明主任和上海交大医学院附属瑞金医院崔文国团队联合通过3D打印构建多孔生物陶瓷支架作为莲蓬的“外衣”,利用脂质体负载血管化药物DFO,通过浸渍吸附的方式将DFO脂质体与微流控水凝胶微球物理结合并作为“莲子”,随后将“莲子”直接注射到3D打印支架内部,从而构建内部血管化的“莲蓬”生物陶瓷3D打印支架以促进骨缺损的修复(Fig.1)。
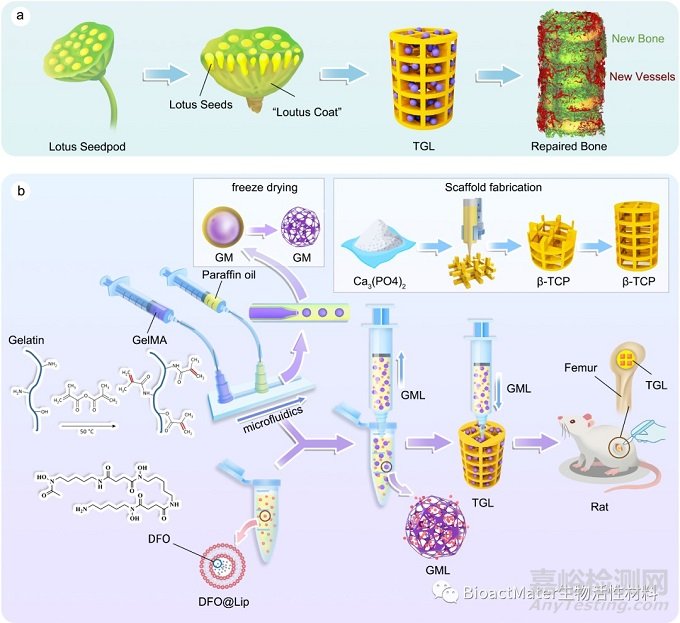
Fig. 1. Schematic diagram of composite scaffold that incorporated GelMA microsphere @ Liposome (GML) into β - TCP scaffold (TGL) and its biological affects in bone repair process in rat bone defect model. (a) The unique biological structure of lotus seedpod and inspirational. (b) Construction process of TGL scaffolds. The synthesized GelMA were made into microspheres (GM) using microfluidics and the DFO loaded liposomes were assembled into the microspheres (GML) via physical adsorption. Finally, the GML was integrated to β-TCP through direct injection to construct the composite TGL. The bone repair capabilities of composite scaffolds were studied in rat distant femur defect model.
首先将制备好的GelMA微球进行了光镜和SEM的检测,可以看到微球大小均一,表面成多孔状。研究发现,与单纯支架相比,复合支架填满了微球,并且无论从孔隙率及力学强度上都与天然骨组织相匹配。体外释放数据显示,DFO在6小时内快速释放了36%,这有利于早期血管的侵入,而在随后的7天中,DFO缓慢释放69%,这对今后支架内部血管网路的成熟和骨缺损的修复有积极的意义(Fig. 2)。
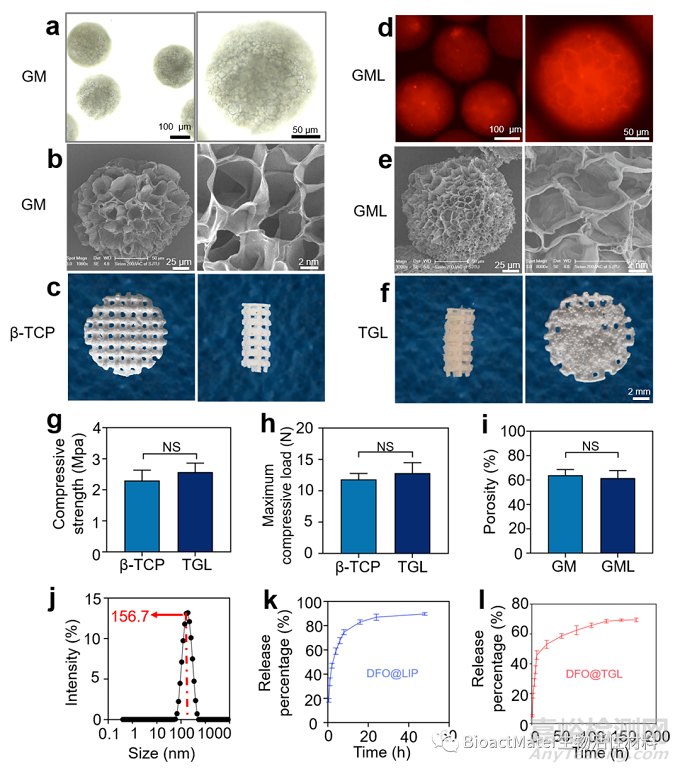
Fig. 2. Characterization of the scaffolds. (a) Light microscopic photos of GelMA microspheres (GM). (b) SEM images of GelMA Microspheres (GM). (c) Digital camera photos of Ca3(PO4)2 scaffold (β-TCP). (d) Fluorescent microscope images of GelMA Microsphere @ Liposome (GML). (e) SEM images of Liposome @ GelMA Microspheres (GML). (f) Digital camera photos of GML @ β-TCP (TGL). (g–h) Mechanical properties of β-TCP and TGL scaffold. (I) Porosity data of GM and GML (j) Characterization of liposome particles via DLS. (k) The in vitro release profile of DFO in the liposome.(i) The in vitro release profile of DFO in the TGL scaffolds. (T-test, NS, no significant difference.)
本研究通过体外细胞实验验证了DFO有效促进了人脐带血内皮细胞聚合成管状,并通过RT-qPCR、Western-blot证实了DFO是通过激活Hif1-α通路, 上调VEGF的表达,来促进新生血管生成的。(Fig. 3)。
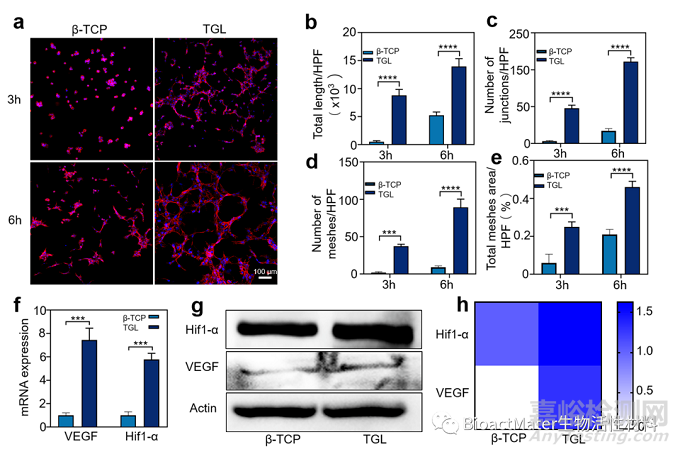
Fig. 3. The vascularization studies of β - TCP and TGL scaffolds in vitro. (a) Endothelial network formation of HUVECs at 3 and 6 h after cell culture. (b–e) The differences of total length (b), number of junctions (c), number of meshes (d) and total meshes area per high power field (HPF) were analyzed. (All the above pictures were taken by laser scanning confocal microscope. Two-way ANOVA was used; ***, p < 0.001; ****, p < 0.0001) (f) The expression of Hif1-α and VEGF on β-TCP and TGL scaffolds (T-test, ***, p < 0.001). (g) The results of Western blot showed that HUVECs were cultured on the scaffold for 24 h. (h) Summarized data showing the difference of Hif1-α and VEGF expression of western-blot results.
该研究在体内构建大鼠远端股骨缺损的动物模型,从Micro-CT及组织学两个方向验证了支架在体内的成骨效率。结果发现(Fig.4),相对于空白组以及单纯支架组,该复合支架通过释放DFO,促进支架内部的血管化及骨髓间充质干细胞(BMSCs)向成骨细胞分化,进而显著加快骨缺损的修复进程。(Fig. 4)。
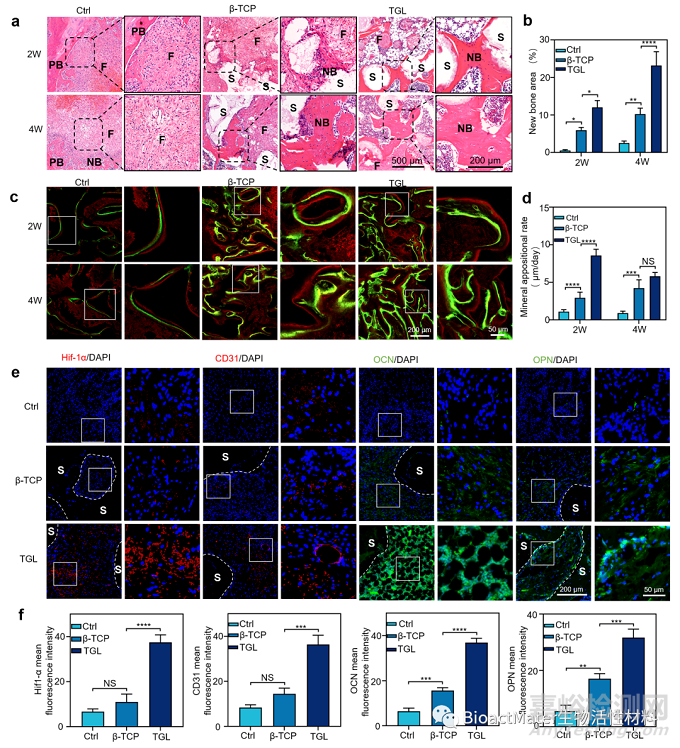
Fig. 4. Histological analysis of the new regenerated tissues in the defect area with the scaffold implantation. (a) Representative HE staining images indicating newly formed tissues including newly mineralized bone tissue (NB), fibrous tissue (F) primitive bone (PB) and scaffolds (S). (b) The quantification of new bone area in HE staining calculated by Image J software. (c) The LSCM scanning results of double calcein labelling at given time points (2 weeks and 4 weeks). The labeled calcein (green) and Alizarin Red S (red) were displayed. The panel in the left is enlarged to clearly show the double marker line. (d) The quantitative distance results of two marker lines was summarized. (e) Immunofluorescence staining of the decalcified bone slices, the angiogenesis and osteogenesis related genes Hif1-α, CD31, OPN and OCN significantly increased in the TGL group. (f) The expression difference of related proteins was quantified. (One-way ANOVA was used; *, p < 0.05; **, p < 0.01; ***, p < 0.001; ****, p < 0.0001); NS, no significant difference). (For interpretation of the references to colour in this figure legend, the reader is referred to the Web version of this article.)
因此,仿生“莲蓬“的生物结构,本研究开发出内部血管化的3D打印支架。该研究证实了其优越的材料学和生物学性能。由于该支架兼具内部血管化及诱导BMSCs向成骨分化的潜能,促进了3D打印支架的应用潜力。期待这一领域的3D打印支架得到不断开发和深入研究,以推动3D打印支架促骨修复的快速发展。
02、论文第一/通讯作者简介
第一作者:韩晓宇
山东第一医科大学附属中心医院,骨科,2018级硕士研究生,研究方向为生物材料介导的骨缺损的修复,上海市伤骨科研究所联合培养。
第一作者:孙明杰
硕士,山东大学附属济南市中心医院脊柱外科医师,临床从事原发性骨质疏松,颈椎病及腰椎间盘突出的诊疗,主要研究方向为生物材料促进骨缺损的修复。
通讯作者:王鹏
博士,主治医师,山东大学附属济南市中心医院骨外科,脊柱外科。主要从事脊柱外科相关疾病的诊治工作。任山东省医学会骨科分会脊柱学组青年委员、肿瘤学组青年委员。山东省康复医学会脊柱微创学组委员。济南医学会骨矿盐与代谢疾病专业委员会委员、秘书。发表SCI论文5篇,主持山东省自然科学基金等项目2项,获山东省科技进步三等奖。
通讯作者:龚维明
主任/教授/硕导,山东大学附属济南市中心医院骨外科主任,脊柱外科主任。主要从事骨科及脊柱外科相关疾病的诊治工作。任山东省医学会骨科学分会委员,山东省康复医学会骨科分会副主任委员,济南医学会骨矿盐与代谢疾病专业委员会主任委员。发表SCI论文10余篇,主持多项省、市级科研项目,获山东省科技进步三等奖。
通讯作者:崔文国
教授/博导,上海交通大学医学院附属瑞金医院/上海市伤骨科研究所。主要基于转化生物医用材料,从事骨、关节等组织修复重建的研究。以第一/通讯作者发表SCI论文120余篇(IF>10的40多篇),引用7000多次,H=45,专利40多项,主编Elsevier书籍1本、参编10本国际书籍章节。主持国家自然科学基金项目重点项目、科技部重点研发项目、面上项目等各类课题10余项,获国家级青年人才计划等支持。曾参与获得2018年教育部高等学校科学研究优秀成果奖一等奖等奖项等。
03、资助信息
该研究得到了国家自然科学基金(51873107)等项目的支持。
04、原文信息
Xiaoyu Han1, Mingjie Sun1, Bo Chen , Qimanguli Saiding , Junyue Zhang , Hongliang Song , Lianfu Deng , Peng Wang*, Weiming Gong*, Wenguo Cui*,
Lotus seedpod-inspired internal vascularized 3D printed scaffold for bone tissue repair.
Bioactive Materials 6 (2021)1639-1652.

来源:BioactMater生物活性材料


