您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-01-29 15:56
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「 本文共:15条资讯,阅读时长约:3分钟 」
今日头条
百济PD-1食管鳞状细胞癌临床结果积极。百济神州PD-1替雷利珠单抗注射液(百泽安®)对比化疗(紫杉醇、多西他赛或伊利替康)用于治疗既往接受过全身疗法的晚期不可切除或转移性食管鳞状细胞癌(ESCC)的国际Ⅲ期临床RATIONALE 302达到总生存期这一主要终点。试验结果表明,针对意向治疗人群(ITT),百泽安®在总生存期中取得了具有统计学意义的显著提高。百泽安®的安全性数据与已知风险相符,未出现新的安全警示。
国内药讯
1.双鹭药业达格列净片申报上市。双鹭药业达格列净片4类仿制上市申请获CDE受理。达格列净是一种新型口服降糖药物,属于SGLT2抑制剂。米内网数据显示,2019年在中国公立医疗机构终端及中国城市实体药店终端达格列净片剂合计销售额超过4亿元。目前,该品种国内仅有阿斯利康一家产品获批上市,鲁抗医药和福元医药以仿制4类提交的上市申请正在审评审批中。
2.百奥泰贝伐珠单抗美国申报上市。FDA受理百奥泰公司贝伐珠单抗生物类似药BAT1706注射液的生物制品上市申请(BLA),用于治疗转移性结直肠癌、非鳞状非小细胞肺癌、复发胶质母细胞瘤、转移性肾细胞癌以及持续性、复发性或转移性宫颈癌。BAT1706是百奥泰继阿达木单抗之后第二款递交上市申请的生物类似药。据悉,该公司在研的生物类似药还包括托珠单抗、戈利木单抗、乌司奴单抗、司库奇尤单抗等。
3.倍特药业氨甲环酸注射液申报上市。倍特药业氨甲环酸注射液4类仿制上市申请获CDE受理。氨甲环酸是一款止血用药,是手术创伤较大的人工关节置换术等围术期药物。在中国公立医疗机构终端氨甲环酸的销售额已突破8亿元。目前,该品种暂无企业获批通过一致性评价;申报氨甲环酸注射液一致性评价补充申请的企业有3家,分别为扬子江南京海陵药业、瑞阳制药和利尔制药。
4.恒瑞1类新药SHR2150胶囊获批临床。恒瑞医药TLR7选择性激动剂SHR2150获CDE四项临床试验默示许可,拟开发的临床适应症均为用于HIV-1感染患者的治疗。TLR7是Toll样受体(TLR)成员之一,负责识别病原体单链RNA,在人体识别和清除病原微生物过程中发挥重要作用。TLR7受体激动剂可通过刺激浆细胞样树突状细胞(分泌干扰素-α(IFN-α),并作用于其他免疫细胞,发挥免疫增强的作用。SHR2150此前已获批在晚期/转移性恶性肿瘤中开展临床研究。
国际药讯
1.默沙东Keytruda新适应症欧盟获批。欧盟委员会批准默沙东PD-1抑制剂Keytruda一线单药治疗转移性高微卫星不稳定性(MSI-H)或错配修复缺陷(dMMR)结直肠癌成人患者。在一项关键Ⅲ期KEYNOTE-177试验中,与化疗组相比,Keytruda显著降低疾病进展或死亡的风险40%(HR=0.60 [95%CI,0.45-0.80]; p=0.0002);两组中位PFS分别为16.5个月(95%CI,5.4-32.4)和8.2个月(95%CI,6.1-10.2),ORR分别为 44%(95%CI,35.8-52.0)和33%(95%CI,25.8-41.1);中位 DOR 未达到。
2.第一三共CD19 CAR-T细胞疗法日本获批上市。日本厚生劳动省批准第一三共制药与吉利德旗下Kite公司合作开发的CD19 CAR-T细胞疗法Yescarta(axicabtagene ciloleucel)上市,用于治疗先前接受过2种或多种系统治疗的复发/难治性大B细胞淋巴瘤(LBCL)成人患者,包括弥漫性大B细胞淋巴瘤(DLBCL)、原发性纵隔B细胞淋巴瘤(PMBCL)、转化后的滤泡性淋巴瘤(tFL)、高级别B细胞淋巴瘤(HGBL)。
3.阿斯利康阿卡替尼日本获批上市。日本厚生劳动省(MHLW)批准阿斯利康BTK抑制剂阿卡替尼(Calquence)上市,用于治疗复发或难治性慢性淋巴细胞白血病(CLL,包括小细胞淋巴瘤[SLL])成人患者。在一项III期ASCEND试验中,与标准护理相比,Calquence将疾病进展或死亡风险显著降低69%;在第12个月时,Calquence治疗组有88%的患者病情没有进展,对照组为68%;Calquence单药治疗组的中位PFS尚未达到,而对照组为16.5个月。
4.礼来、GSK、Vir合作开发新冠中和抗体组合疗法。礼来新冠中和抗体bamlanivimab(LY-CoV555)联合Vir/葛兰素史克新冠中和抗体VIR-7831(GSK4182136),将在低风险的轻中度COVID-19患者中开展联合用药的临床研究。VIR-7831是一种具有双重作用机制的单克隆抗体,采用Fc端的修饰设计不但让它能够阻断病毒进入健康细胞,还能够激活免疫系统,具有清除受到感染细胞的潜力。目前礼来已扩展其正在进行的BLAZE-4试验,以评估这一组合疗法的效果。
5.辉瑞托法替尼上市后安全性研究结果公布。辉瑞(Pfizer)公布类风湿关节炎(RA)药物托法替尼(XELJANZ®)上市后安全性研究ORAL Surveillance(A3921133;NCT02092467)的共同主要终点结果。该研究评估托法替尼与TNF抑制剂(TNFi)相比用于治疗50岁及以上、至少有一个额外心血管(CV)危险因素的RA患者的安全性。结果显示,在主要心血管不良事件(MACE)和恶性肿瘤(不包括非黑色素瘤皮肤癌 [NMSC])方面,与TNFi相比,托法替尼不具非劣效性。
6.罕见病肝豆状核变性基因疗法美国获批临床。罕见病新药研发公司Ultragenyx拟用于治疗肝豆状核变性(hepatolenticular degeneration)的AAV9基因疗法UX701的新药临床试验申请(IND)获FDA批准。这是一项无缝、单方案Ⅰ/Ⅱ/Ⅲ期临床试验,该研究分为三个阶段,依次为:初始安全性和剂量探索评估阶段、关键临床数据的最佳剂量评估阶段以及长期随访阶段。UX701旨在单次静脉输注后稳定表达ATP7B铜转运蛋白,已在美国和欧洲获孤儿药资格。
医药热点
1.豪森氟马替尼片降价63%。陕西省公共资源交易中心发布关于调整甲磺酸氟马替尼片等产品挂网限价的通知。根据企业申请,将豪森的甲磺酸氟马替尼片等其他部分产品挂网限价进行调整,调整后价格即日起执行。其中,豪森药业自主研发用于治疗费城染色体阳性的慢性髓性白血病(Ph+ CML)慢性期成人患者的创新药甲磺酸氟马替尼片(规格:0.2g,豪森昕福)价格从5280元调整至1950元,降幅达63%。
2.中国居民基本医保覆盖率达96.8%。国家卫健委28日发布《全国第六次卫生服务统计调查报告》。覆盖全国31个省(自治区、直辖市)、156个县(市、区)、752个乡镇(街道)、1561个行政村(居委会)、94076户居民的《调查报告》数据显示,基本医保覆盖率达到96.8%,比2013年提高1.7个百分点,城市和农村的基保参保率分别为96.1%和97.6%。在费用方面,数据显示医疗费用增长速度趋缓,费用增幅得到一定程度的控制。
3.新版职业病诊断管理办法突出用人单位义务。1月26日,国家卫健委发布新版《职业病诊断与鉴定管理办法》。新版《办法》对2013年2月19日原卫生部发布的《职业病诊断与鉴定管理办法》进行了修订,突出了用人单位的相关义务,细化了劳动者提供相关证明资料的要求,明确并缩短了职业病诊断办理时限。
4.疫情造成全球精神科医生需求显著增加。世卫组织驻俄罗斯联邦代表梅利塔·武伊诺维奇在一份声明中表示,由于新冠肺炎疫情大流行,全球对精神科医生和治疗师的服务需求显著增加。在一项世卫组织针对新冠病毒对神经和精神健康的影响进行的调查研究中,该组织的130个国家/地区中有93%报告了由于疫情流行而导致的精神健康障碍疾病,显示出对精神医疗服务需求的显著增加。
股市资讯
【海思科】全资子公司辽宁海思科制药有限公司的注射用艾司奥美拉唑钠通过仿制药一致性评价。
【步长制药】全资子公司泸州步长的产品“注射用重组人促红细胞生成素-Fc融合蛋白”获得了北京大学人民医院伦理审查委员会批件,正式启动III期临床试验,其适应症为慢性肾功能衰竭或肿瘤化疗引起的贫血。
【君实生物】子公司拓普艾莱向FDA提交了特异性抗TIGIT单克隆抗体注射液用于治疗晚期恶性肿瘤的临床试验申请并获得受理。公司将在获得FDA的正式批准后于美国开展TAB006/JS006的临床试验。
审评动向
1. CDE最新受理情况(01月28日)
2. FDA最新获批情况(北美01月26日)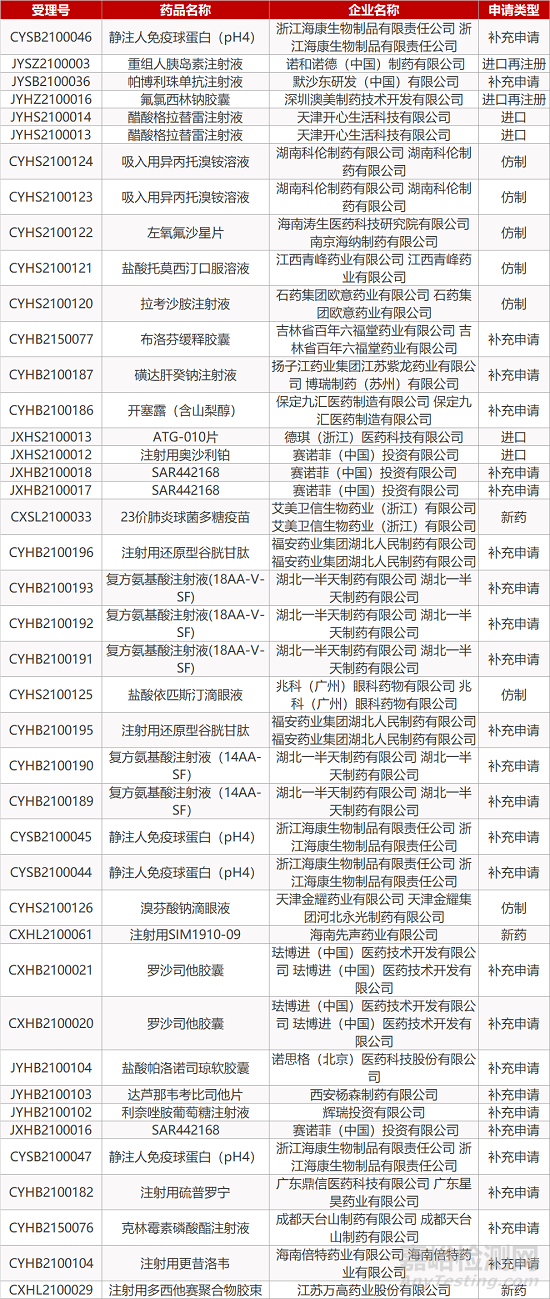
暂无
- The End -

来源:药研发


