您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2019-11-26 09:08
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「本文共:15条资讯,阅读时长约:3分钟 」
今日头条
罗氏PD-L1+贝伐组合治疗肝癌Ⅲ期结果积极。罗氏(Roche)公司公布其PD-L1抗体Tecentriq(atezolizumab,阿替利珠单抗)与VEGF抗体Avastin(bevacizumab,贝伐珠单抗)构成的组合疗法,在治疗既往未接受过全身治疗的不可切除肝细胞癌(HCC)患者的Ⅲ期临床IMbrave150中获积极结果。结果显示,与标准疗法索拉非尼相比,Tecentriq/Avastin组合将患者死亡风险降低42%,使疾病进展或死亡风险降低41%。该组合疗法此前已获FDA授予一线治疗晚期或转移性HCC的突破性疗法认定。罗氏的Tecentriq/Avastin/化疗三联疗法也已获FDA批准用于治疗非小细胞肺癌。
国内药讯
1.国内首个PD-L1单抗即将获批。阿斯利康PD-L1单抗Durvalumab 注射液(Imfinzi)在国内的上市申请处于「在审批」状态,预计近期获批成为国内首个上市的PD-L1单抗药物,用于治疗不可手术的Ⅲ期非小细胞肺癌(NSCLC)。2017年5月,Imfinzi获FDA批准用于治疗晚期或转移性尿路上皮癌。2018年2月,FDA又批准Imfinzi用于治疗Ⅲ期不可手术切除的局部晚期NSCLC患者。一项在不可手术切除的III期NSCLC同步放化疗后未进展患者中开展的III期临床PACIFIC中,与安慰剂组相比,Imfinzi显著延长PFS超过11个月(16.8个月vs5.6个月)。Imfinzi 是第一个在III期NSCLC患者带来PFS显著获益的免疫检查点抑制剂。
2.普利制药地氯雷他定片通过一致性评价。普利制药地氯雷他定片通过一致性评价并获《药品补充申请批件》。地氯雷他定为非镇静性的长效三环类抗组胶药,为氯雷他定的活性代谢物,可通过选择性地阻断外周H1受体,抑制各种过敏性致炎的化学介质的释放,缓解过敏性鼻炎或慢性特发性荨麻疹的相关症状。该药原研药由Sepracor公司研制,Schering-Plough公司开发并在全球53个国家上市。目前地氯雷他定片已获批进口中国,商品名:恩理思,规格:5mg。
3.现代制药米卡芬净钠即将获批。现代制药旗下注射用米卡芬净钠的注册审评状态变更为“审批完毕—待制证”。据了解,米卡芬净由安斯泰来研制开发,最早于2002年在日本获批上市,2006年获批进口中国,用于治疗由曲霉菌和念珠菌引起的真菌血症、呼吸道真菌病、胃肠道真菌病。目前,该产品国内获批的主要生产企业有安斯泰来制药(中国)、海正药业、豪森药业。根据米内网统计数据,2018年该类产品上述生产企业在国内四大终端销售收入近44,790万元人民币。
4.默沙东Keytruda肺鳞癌中国临床数据发布。在ESMO Asia 2019大会上,默沙东公司公布其PD-1抑制剂Keytruda(帕博利珠单抗)联合化疗,对比安慰剂联合化疗,用于转移性鳞状非小细胞肺癌(NSCLC)患者一线治疗的Ⅲ期研究KEYNOTE-407中国亚组(包括中国扩展队列)中期分析数据。KEYNOTE-407中国扩展研究数据显示,与安慰剂联合化疗相比,Keytruda联合化疗降低56%的死亡风险(而全球研究这一数据为29%,中国人群数据优于全球数据),两组中位OS分别为17.3个月vs12.6个月;降低68%的疾病进展或死亡风险,两组中位PFS分别为8.3个月vs 4.2个月。
5.百济神州替雷利珠单抗G/GEJ腺癌临床数据公布。在ESMO Asia 2019大会上,百济神州公布其在研抗PD-1抗体替雷利珠单抗联合化疗,用于治疗胃/胃食管结合部(G/GEJ)腺癌患者以及食管鳞状细胞癌(ESCC)患者的Ⅱ期临床的初步数据。在G/GEJ腺癌队列中,7例患者(46.7%)达部分缓解(PR),客观缓解率(ORR)为46.7%,中位缓解持续时间(DoR)尚未成熟,中位无进展生存期(PFS)为6.1个月,OS率在6个月时为85%,在12个月时为62%。在ESCC队列中,7例患者(46.7%)达PR,ORR为46.7%,中位DoR估计值为12.8个月,中位PFS为10.4个月,OS率在6个月时为71%,在12个月时为50%。
6.2款中国药物获FDA授予孤儿药资格。FDA上周共授予2款中国药物孤儿药资格。一款为和记黄埔的索凡替尼(surufatinib),获授予治疗胰腺神经内分泌肿瘤的孤儿药资格。索凡替尼具有抗血管生成和免疫调节双重活性,多重作用机制让它可以与其它癌症免疫疗法联用,治疗多种类型的癌症。另一款为百济神州的在研PD-1抑制剂(替雷利珠单抗,tislelizumab),获授予治疗肝细胞癌的孤儿药资格。据悉这款药物具有对PD-1的高亲和性和特异性,通过Fc段改造而与目前已获批的PD-1抗体存在潜在的区别,该药此前也已获FDA授予治疗食管癌的孤儿药资格。
国际药讯
1.武田ALK抑制剂Alunbrig治疗肺癌长期疗效积极。武田(Takeda)开发的下一代ALK抑制剂Alunbrig(brigatinib)在一线治疗ALK阳性非小细胞肺癌(NSCLC)患者的Ⅲ期临床ALTA-1L中表现出良好的长期疗效。与常见一代ALK抑制剂crizotinib相比,Alunbrig将患者疾病进展或死亡的风险降低57%,Alunbrig组患者的无进展生存期(PFS)为29.4个月,而crizotinib组的PFS为9.2个月;在脑转移的患者中,Alunbrig将疾病进展或死亡风险降低76%,Alunbrig组的PFS为24个月,crizotinib组为5.6个月。Alunbrig 2017年4月已获FDA加速批准,用于治疗接受crizotinib治疗之后疾病进展的ALK阳性转移性NSCLC患者。
2.武田登革热四价疫苗III期临床最新结果。武田公布其登革热四价疫苗TAK-003(2针免疫,间隔3个月)用于4-16岁的健康人群预防4种血清型登革热病毒感染的III期TIDES研究的最新结果。结果显示,在有足够数量病例的次要终点方面均达到所有次要终点。研究第二部分的总VE(疫苗效力)和安全性结果与主要终点分析报告的数据基本一致:第二针18个月分析的总VE为73.3%,主要终点分析(第二针免疫后12个月)的VE为80.2%(95%CI:73.3%至85.3%,p<0.001)。主要终点分析的总VE数据已于本月初发表于《新英格兰医学杂志》(NEJM)。
3.Heat细胞疗法HS-110联合Opdivo临床数据积极。Heat Biologics公司T细胞激活细胞疗法HS-110,联合BMS肿瘤免疫疗法Opdivo(纳武单抗),治疗晚期非小细胞肺癌(NSCLC)的II期临床队列A获顶线数据。在经治的、且未接受过检查点抑制剂的患者中,中位总生存期(mOS)为16.9个月(中位随访17个月时,有50%的患者仍然存活),而在CheckMate-057研究中Opdivo单药治疗相似患者群体的mOS为12.2个月;经历皮肤注射部位反应的患者组(即ISR阳性患者)的mOS为42.1个月(95%CI:15.8-42.1),而ISR阴性患者组的mOS为5.9个月(95%CI:1.4-11.6);ISR阳性患者组的无进展生存期和mOS与ISR阴性患者组相比有统计学意义的改善。
4.美敦力新型紫杉醇药物涂层设备在美获批。美敦力紫杉醇涂层球囊IN.PACT AV获FDA批准,该球囊是专门为帮助清除接受透析治疗的患者使用的静脉通路而设计的。IN.PACT AV先前已获CE标志,用于终末期肾脏疾病的患者,帮助其重新张开塌陷的动静脉瘘。一项临床IN.PACT AV ACCESS IDE研究评估IN.PACT™ AV通道药物涂层球囊与经皮腔内血管成形术在治疗上肢自体AV瘘的原发病变或再狭窄阻塞性病变中的安全性和有效性。研究表明,180天后,IN.PACT治疗组有86.1%目标血管保持开放,接受传统经皮腔内血管成形术的患者中的这一比例为68.9%;两组在12个月内的死亡率无显著差异。
5.诺华欲收购降脂RNAi疗法开发公司。诺华拟以近70亿美元收购The Medicines Company,将获得其降低低密度脂蛋白胆固醇(LDL-C)的创新RNAi疗法inclisiran。Inclisiran是一款靶向编码PCSK9蛋白的mRNA的RNAi疗法,患者只需每年接受两次inclisiran注射治疗,就可以成功降低LDL-C水平。目前,inclisiran已在3项Ⅲ期临床(ORION-9、ORION-10和ORION-11)中达到主要终点,不但能够在不同类型患者中将LDL-C水平降低超过50%,而且表现出良好的安全性。The Medicines Company计划在今年向FDA递交其上市申请,在明年第一季度向欧盟递交监管申请。
医药热点
1.5部放疗质控指南出台。由国家癌症中心放疗质控专家委员会主办的2019放疗质控专家委员会在京召开。会上,国家癌症中心放疗质控专家委员会发布5部放射治疗相关的指南,主要供医学物理师在开展放疗设备的质量控制时使用。据悉,这是我国首次发布的针对不同放疗技术和设备的相关指南。这5部指南分别是《医用电子直线加速器质量控制指南》《后装治疗机的质量控制和质量保证》《螺旋断层放疗系统的质量保证》《放射治疗记录与验证系统质量控制指南》《调强放疗剂量验证实践指南》。
2.我国糖尿病患病率上升趋势未改变。中华医学会糖尿病学分会第二十三次全国学术会议召开,此次会议由中华医学会、中华医学会糖尿病学分会主办,以“聚焦前沿、创新管理、注重预防”为主题,并设置了血糖全程管理、“运动是良医”“5公里健康跑”临床营养等实践版块,并举行联合国糖尿病日和“蓝光行动2019”成就展览等活动,呼吁全社会共同关注糖尿病防治。据悉,近40年来,中国的糖尿病患病率呈上升趋势,糖尿病发病率为每年2%,而且77%的糖尿病可以通过控制代谢来预防,合理饮食、减少肥胖等因素来消除。
3.上海再推“创新医疗服务品牌”。上海市第三批30个“创新医疗服务品牌”出炉。据了解,第三批品牌项目更注重“数据流动”“流程优化”“服务智能”“人文关怀”等四个方面的创新。如复旦大学附属金山医院打造“数字胶片云”,推进不同医院之间医疗影像信息的互通、共享;上海交大医学院附属仁济医院通过扁平化和多中心一体化管理实现资源利用最大化、诊疗水平同质化,“一站式专病诊疗”与“日间手术”模式的推行实现服务和效率双提升;复旦大学附属妇产科医院打造信息智能同步、资源动态调配、AI智能宣教和精准全预约管理。
股市资讯
.
【普利制药】全资子公司浙江普利收到《药品生产许可证》,新增软膏剂生产范围。
【九强生物】截至2019年11月23日,股东程辉减持公司股票计划时间已届满,合计减持190万股(总股本0.38%),拟继续减持500万股(总股本0.9964%)。
【一品红】截止2019年11月22日,公司累计通过股票回购专用证券账户以集中竞价交易方式回购164.59万股(总股本1.02%),成交均价为40.11元/股,支付的总金额为6601.72万元(不含交易费用)。
审评动向
1. CDE最新受理情况(11月25日)
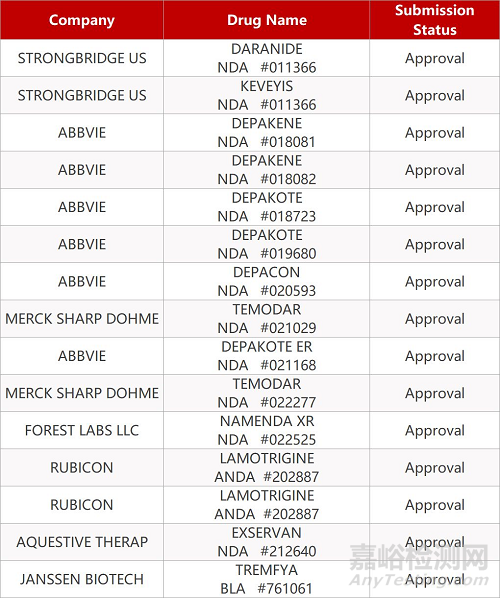
2. FDA最新获批情况(北美11月24日)


来源:药研发


