您当前的位置:检测资讯 > 生产品管
嘉峪检测网 2025-08-11 18:55
纳米药物,是指使用纳米技术生产纳米级颗粒形式的活性药物成分,或将活性药物成分与合适的纳米材料相结合以进一步配制成多功能剂型的纳米级颗粒。其发展过程分为3 个阶段:初级研究阶段(第1 阶段,1964 — 1995 年),始于1964 年发现脂质体结构,1995年美国食品和药物管理局(FDA)批准了首个基于脂质体阿霉素(DOX)递送系统的纳米药物Doxil®[1];第2阶段(1995 — 2007年),相关研究开始迈向临床验证和商业化;第3阶段(2007年至今),纳米医学迅速发展,出现多种创新的纳米药物[2]。纳米药物的优点有:易进入细胞,更高效;比表面积大,可承载的功能基团或活性中心多;性能优越,便于生物降解或吸收,因有多孔、多层、中空等结构特性,易于实现药物的缓释、控释等功能。2021年8月国家药品监督管理局药品审评中心(CDE)发布的《纳米药物质量控制研究技术指导原则(试行)》[3]指出,与普通药物相比,纳米药物具有基于纳米结构的尺度效应。纳米药物特殊的纳米尺寸、纳米结构和表面性质等可能导致药物体内外行为的明显变化,从而实现临床获益;但纳米尺度效应带来的安全性风险可能会相应增加。本研究中参考《纳米药物质量控制研究技术指导原则(试行)》,并检索药智网及FDA、国家药品监督管理局(NMPA)官方网站,总结了纳米药物的分类、上市情况、质量控制指导,并提出针对性建议,为保障纳米药物的有效性和安全性提供参考。现报道如下。
1 分类
1. 1 药物纳米粒
无需载体材料,利用纳米制备技术可将活性成分通过高强度机械力直接粉碎成纳米级的纳米晶体药物。通常以结晶态分散粒子存在,当以液体形式存在时,又常被称为纳米混悬剂。具有粒径小、比表面积大的特点,可显著提高药物溶解性和生物利用度。与其他纳米给药系统相比载药量大,适合大剂量给药,同时高载药量可减少给药体积,多为口服制剂,是发展最早的纳米药物类型,如1996年获批于美国上市的盐酸替扎尼定片。
1. 2 载体类纳米药物
是利用各种材料(包括脂质、聚合物、蛋白质、金属和无机材料)制备的纳米载体负载药物,借助适当的载体材料与药物结合,对疾病进行靶向治疗。可利用各种纳米载体进行体内药物递送,通过主动靶向或被动靶向等多种机制实现跨生物屏障运输,将药物递送至肿瘤等病变部位,实现靶向治疗。目前研究较多的纳米载体主要有脂质体、纳米乳、聚合物胶束、聚合物纳米粒、无机纳米粒等。
脂质体:是由磷脂双分子层包裹形成的封闭囊状体系,其水性内腔可用于水溶性肽类药物的运载,磷脂双分子层则起到阻滞药物泄漏的作用,同时可在表面进行功能化修饰以提高吸收效率。脂质体具有细胞膜样脂质双层结构,可同时负载疏水和亲水药物,具有稳定性好、生物相容性高、无毒性等优点[4]。但由于其复杂和异质的结构,需克服囊泡系统的物理和化学不稳定性相关的特定问题。目前已批准上市的脂质体药物主要集中于肿瘤治疗,同时也涉及感染、麻醉、疫苗、肺部疾病等领域。剂型主要为无菌混悬液和冻干粉,多用于静脉输注、肌内注射和鞘内注射。Doxil®脂质体的治疗范围已扩展到各种疾病,可有效负载一系列小分子和生物大分子药物(如肽、单克隆抗体等)[5 - 6]。
纳米乳:是一种由2 种不混溶液体组成的各向同性、透明/ 半透明、异质系统,由药物在纳米液滴中的精细分散组成[7],是热力学和动力学稳定的系统(长期储存期间无任何明显的絮凝或聚结),具有极小的液滴尺寸(20~400 nm)、均匀的尺寸分布及与其他乳液( > 500 nm)不同的物理、化学和生物学特性[8]。且对亲水性和亲脂性物质的溶解度较高,载药量百分比高,以及作用于赋形剂(与特定组织相互作用中起重要作用)的能力。纳米乳作为药物递送载体已被广泛用于注射、口服、经皮渗透等多种给药途径,由于透皮吸收效率较高,其已被证明是用于各种药物的皮肤和透皮递送的多功能载体[9],如负载司来吉兰的纳米乳液,可用于鼻内递送司来吉兰治疗帕金森病。
聚合物胶束:是在液体基质中形成的自组装聚合物,其特征在于核壳结构是由两亲性嵌段共聚物形成的纳米尺寸的球状胶束,具有疏水性核心和亲水性外壳,疏水性核心可包封水溶性差的药物,亲水性外壳可负载亲水性药物并使其维持稳定状态。在与高于其临界胶束浓度的水性介质接触时,通过共聚物的自组装形成载药聚合物胶束[9]。胶束分子特征灵活,可用于封装复杂、水溶性差的药物,将不同的两亲体组合在一个单一的聚集体中并产生能利用不同组分特征的混合胶束,从而大幅扩展了纳米载体的治疗潜力。聚合物胶束药物已达到癌症治疗评估和监管批准的临床阶段,如Genexol - PM®是由甲氧基聚乙二醇-聚DL - 丙交酯组成的共聚胶束,用于增加紫杉醇的水溶性和治疗效果[10];其已获批应用于临床,作为癌症治疗药物。聚合物纳米粒:是一种基于聚合物的控释技术,核心包封活性药物组成的纳米级别的球形聚合物颗粒[11]。聚合物外壳可增加所负载蛋白质和核酸的稳定性,使其免受蛋白酶和核酸酶的降解,可通过筛选不同功能单体或交联剂来调控纳米粒的性质。与其他递送系统相比,聚合物纳米颗粒在储存期间具有更高的保质期稳定性、结构完整性;且其可使治疗剂持续释放,具有改进的特异性生物分布及易于通过静脉内途径给药[12]。常用的聚合物包括天然聚合物(白蛋白和壳聚糖等)及合成聚合物(聚乙二醇等),目前,已获批上市的有用于治疗胰腺癌、转移性乳腺癌的白蛋白- 紫杉醇纳米颗粒Abraxnae®和用于治疗肝细胞性肝癌的阿霉素纳米颗粒Transdrug®[13]。
聚合物- 药物偶联物(PDC):是指一个或多个药物分子的药理活性部分(小分子蛋白质、肽等)与聚合物通过共价偶联形成的纳米药物[14]。由聚合物骨架、接头、靶向配体、药物等模块组成,具有改善药物溶解度、增强药物生物利用度、延长半衰期、提高治疗效果、控制药物递送的优点[15],但其聚合物异质性、偶联物变异性、聚合物的免疫原性、安全性、稳定性是其应用于临床的主要障碍。合成聚合物、多糖等各种大分子被用于PDC充当着药物递送和靶向的载体。
无机纳米粒:是一类具有多种形态、粒径1~100 nm的纳米粒,不仅可进行表面修饰,还可通过不同方式(如疏水相互作用、静电相互作用等)与药物分子结合。主要以碳纳米材料、磁性纳米粒、二氧化硅纳米粒、钙纳米材料等形式存在。其具有良好的生物相容性及光热和光动力效应,与各种配体和生物分子可较好兼容,但体内消除率低,可能存在长期的潜在毒性。
1. 3 其他
随着纳米医学技术的不断发展,越来越多先进的天然材料(蛋白质、多糖等)和合成材料(聚乳酸- 羟基乙酸共聚物、聚乙二醇等)作为纳米药物载体,还有一些新型纳米载体,如细胞外囊泡[16]、仿生和仿生纳米载体[17]、金属有机骨架[18]等也不断涌现。
2 上市情况
目前,全球范围内已有100 余种纳米药物获批上市,主要集中于肿瘤和感染的治疗,美国占据主要市场。在市场或临床转换的各个阶段可获得的纳米药物中,脂质体或脂质基纳米颗粒较普遍,其次为抗体- 药物偶联物、聚合物- 药物偶联物和聚合物纳米粒。其他类型的纳米药物包括病毒载体、细胞衍生载体、无机纳米粒、纳米乳、蛋白质纳米粒、聚合物胶束、纳米晶体、树枝状聚合物、胶体铁等[19]。国外已上市部分纳米药物见表1。
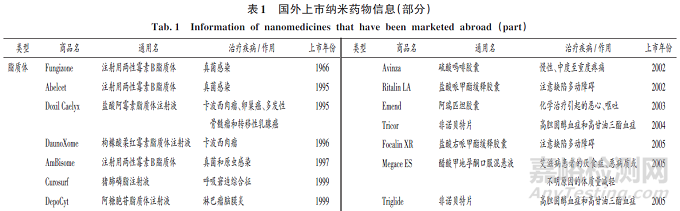
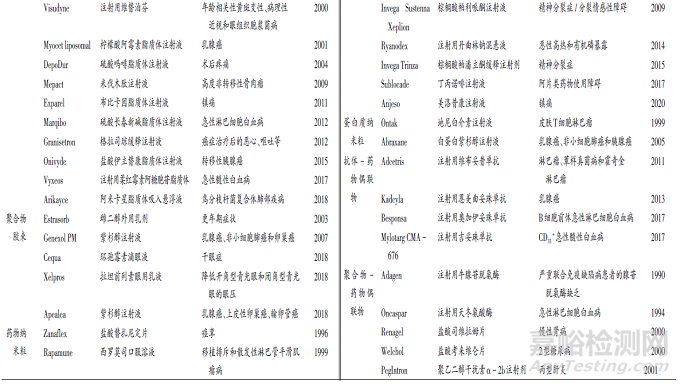
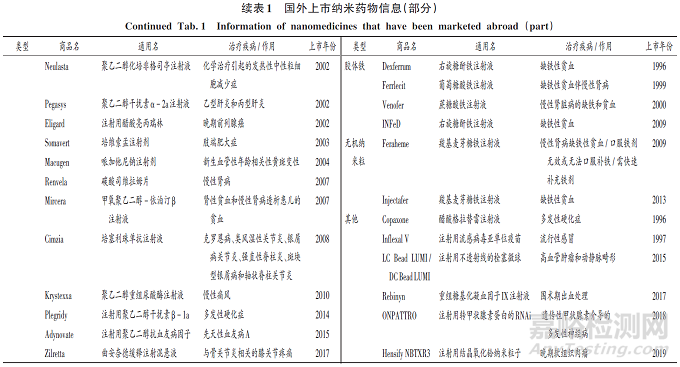
相较于国外,我国纳米药物市场发展起步晚,但发展迅速,我国已上市纳米药物(部分)见表2。
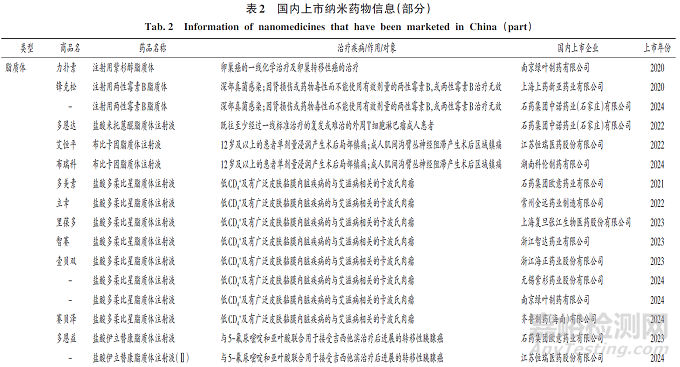

可知,注射用紫杉醇(白蛋白结合型)已有7家生产企业,截至2024 年12 月26 日,取得批准文号的脂质体注射液有16个。2020年上市的注射用紫杉醇脂质体为南京绿叶制药有限公司自主研发的创新制剂,是全球首个获批上市的紫杉醇脂质体产品;2021年,上海谊众药业股份有限公司研制的首个紫杉醇胶束获批国家2. 2类新药上市;2022年批准的国家2. 2类新药盐酸米托蒽醌脂质体注射液是石药集团自主研发的抗肿瘤纳米药物,也是全球首个上市的米托蒽醌纳米药物。
3 质量控制方法
纳米药物的性质有别于传统药物,其相关性能分为制剂基本特性和纳米相关特性两大类。前者相关的质量控制指标包括鉴别、含量测定、有关物质、残留溶剂等;后者主要包括粒径大小及分布、结构及形态、Zeta电位、药物载体的包封率与载药量、药物体外溶出和释放等。不同纳米药物的质量研究重点和内容可能不同,应设置具有针对性、科学合理的评价指标。
粒径大小及分布:纳米药物的粒径大小及分布影响活性成分的载药量和释放行为,并影响其质量和药效作用。通常采用动态光散射法、显微成像技术、纳米颗粒跟踪分析系统等进行分析。朱晓亮等[20]通过马尔文激光粒度仪对利多卡因纳米乳的粒径大小及分布进行测定;LU等[21]采用马尔文激光粒度仪、粒度电位仪和显微镜对布比卡因脂质体的粒度进行分析。结构及形态:纳米药物的结构和形态可能影响其在体内与蛋白质和细胞膜的相互作用、药物的释放、纳米颗粒的降解和转运等。NMPA发布的《盐酸多柔比星脂质体注射液仿制药研究技术指导原则(试行)》和《注射用紫杉醇(白蛋白结合型)仿制药研究技术指导原则(试行)》均将药物形态作为关键质量属性进行要求,可采用电镜法、X 射线衍射法和偏振光显微镜法进行分析。
Zeta电位:纳米药物的表面电荷可维持纳米粒子的稳定性,其取决于纳米药物的粒径大小、组成及分散介质。纳米药物的表面电荷一般基于Zeta电位进行评估,应选择适当的方法和介质进行研究。张淼等[22]采用动态光散射仪对卡巴他赛纳米混悬剂进行Zeta电位测定以筛选稳定剂浓度,同时Zeta电位测定还可用于表征卡巴他赛纳米混悬剂。
药物载体的包封率和载药量:包封率是指包封的药量与纳米药物中总药量的比值,是纳米药物实现高效、低毒的关键。分离方法包括葡聚糖凝胶柱法、超速离心法和超滤法;载药量是指装载的药量与载体类纳米药物量的比值,是纳米粒作为药物载体可行性的一个重要指标。二者一般经样品前处理后根据药物性质采用适宜的测定方法进行测定。马福旺等[23]采用葡聚糖凝胶柱分离固脂纳米粒与游离马钱子碱,并采用高效液相色谱法测定载药量和包封率;李亚男等[24]采用薄膜分散法制备多西他赛他莫昔芬复方脂质体,采用葡聚糖凝胶柱层析法分离脂质体和游离药物,采用高效液相色谱法测定脂质体中多西他赛和他莫昔芬包封率。
药物体外溶出与释放:纳米药物的体外溶出与释放是其重要质量属性,也在一定程度上反映纳米药物的体内行为,从而确保药物临床使用的有效性和安全性。纳米药物的尺度效应导致影响药物释放的因素更复杂,纳米给药系统粒径的多样性和不均匀性、体内释放过程的多样性、纳米载体材料的自身降解、纳米载体孔径大小、外部环境刺激、内部构象、渗透性等均可影响药物释放[25]。测定纳米药物体外释放度的方法主要有透析法、离心法、流通池法等。前2种方法报道较多,但不具有代表性的流体动力学特性且各有其局限性;流通池法能更好地模拟体内流体力学且维持漏槽条件,SIEVENS - FIGUEROA 等[26]分别采用转篮法和流通池法测定灰黄霉素纳米混悬液体外释放度,结果显示,流通池法具有更好的粒径区分能力。
4 结语
纳米药物能改善药物递送、提升药物稳定性、延长体内循环时间、增加药物安全性,目前已被用于递送难溶性药物、抗肿瘤药物、基因药物及需要突破血脑屏障的药物等。随着越来越多纳米药物的上市,其安全性问题和质量研究的相关问题也应得到更多的重视。研发企业应结合纳米药物的载药量和包封率及药物体外溶出与释放行为,设计合理的粒径大小与分布、结构及形态、Zata电位等关键性能,降低纳米尺寸效应带来的安全性风险,提升纳米药物有效性和安全性。CDE发布了《纳米药物质量控制研究技术指导原则(试行)》《纳米药物非临床药代动力学研究技术指导原则(试行)》《纳米药物非临床安全性研究技术指导原则(试行)》,为纳米药物关键质量属性的探索提供了指导意见,标志着国内纳米药物的监管迈出重要一步;但由于纳米药物传递体系的多样性,提高其靶向性、有效性和安全性应引起重点关注,监管部门应建立纳米药物质量控制体系,进一步完善纳米药物监管机制。
参考文献
[1]LIU QY,ZOU JH,CHEN ZJ,et al. Current research trends of nanomedicines[J]. Acta Phar Sin B,2023,13(11):4391 -4416.
[2]JIA YC,JIANG YX,HE YL,et al. Approved Nanomedicine against Diseases[J]. Pharmaceutics,2023,15(3):774.
[3]国家药品监督管理局药品审评中心. 国家药监局药审中心关于发布《纳米药物质量控制研究技术指导原则(试行)》《纳米药物非临床药代动力学研究技术指导原则(试行)》《纳米药物非临床安全性评价研究技术指导原则(试行)》的通告[A / OL].(2021 - 08 - 27)[2022 - 12 - 01]. https://www. cde. org. cn / main / news / viewInfoCommon / 95945bb17 a7dcde7b68638525 ed38f66.
[4]ZHAI YJ,ZHAI GX. Advances in lipid - based colloid systems as drug carrier for topic delivery[J]. Journal of Controlled Release,2014,193:90 - 99.[5]KHAN AA,MUDASSIR J,MOHTAR N,et al. Advanced drug deliverytothelymphaticsystem:lipid-basednanoformulations[J]. International Journal of Nanomedicine,2013,8:2733 - 2744.
[6]BOAFO GF,SHI YJ,XIAO QQ,et al. Targeted co - delivery of daunorubicin and cytarabine based on the hyaluronic acid prodrug modified liposomes[J]. Chinese Chemical Letters,2022,33(10):4600 - 4604.
[7]CHEN HB,KHEMTONG C,YANG XL,et al. Nanonization strategies for poorly water - soluble drugs[J]. Drug Discovery Today,2011,16(7 - 8):354 - 360.
[8]RAI VK,MISHRA N,YADAV KS,et al. Nanoemulsion as pharmaceutical carrier for dermal and transdermal drug delivery:Formulation development,stability issues,basic considerations and applications[J]. Journal of ControlledRelease,2018,270:203 - 225.
[9]PHAM DT,CHOKAMONSIRIKUN A,PHATTARAVORAKARN V ,et al. Polymeric micelles for pulmonary drug delivery :a comprehensive review[J]. Journal of Materials Science,2021,56:2016 - 2036.
[10]MANDAL A,BISHT R,RUPENTHAL ID,et al. Polymeric micelles for ocular drug delivery:From structural frameworks to recent preclinical studies[J]. Journal of Controlled Release,2017,248:96 - 116.
[11]ROSE F,WERN JE,GAVINS F,et al. A strong adjuvant based on glycol - chitosan - coated lipid - polymer hybrid nanoparticles potentiates mucosal immune responses against the recombinant Chlamydia trachomatis fusion antigen CTH522[J]. Journal of Controlled Release ,2018 ,271 :88 - 97.
[12]SONI G,KALE K,SHETTY S,et al. Quality by design(QbD) approach in processing polymeric nanoparticles loading anticancer drugs by high pressure homogenizer[J]. Heliyon,2020,6(4):e03846.
[13]刘君,许银银,李萌,等. 纳米药物的研究进展[J].药学与临床研究,2020,28(1):51 - 55.
[14]GRECO F,VICENT MJ. Combination therapy:opportunities and challenges for polymer - drug conjugates as anticancer nanomedicines[J]. Advanced Drug Delivery Reviews,2009,61(13):1203 - 1213.
[15]EKLADIOUS I,COLSON YL,GRINSTAFF MW. Polymer - drugconjugatetherapeutics:advances,insightsandprospects[J]. Nature Reviews Drug Discovery,2019,18(4):273 - 275.
[16]HERRMANN IK,WOOD MJA,FUHRMANN G. Extracellular vesicles as a next - generation drug delivery platform[J]. Nature Nanotechnology,2021,16(7):748 - 759.
[17]PARODI A,MOLINARO R,SUSHNITHA M,et al. Bio - inspired engineering of cell - and virus - like nanoparticles for drug delivery[J]. Biomaterials,2017,147:155 - 168.
[18]HE S,WU L,LI X,et al. Metal - organic frameworks for advanced drug delivery[J]. Acta Pharmaceutica Sin B,2021,11(8):2362 - 2395.
[19]SHAN XT,GONG X,LI J,et al. Current approaches of nanomedicines in the market and various stage of clinical translation[J]. Acta Pharm Sin B,2022,12(7):3028 - 3048.
[20]朱晓亮,陈志良,李国锋,等. 利多卡因纳米乳的制备及质量控制[J]. 中国医院药学杂志,2008,28(1):30 - 33.[21]LUBH,MAQY,ZHANGJ,etal. Preparationandcharacterization of bupivacaine multivesicular liposome:A QbD study about the effects of formulation and process on critical quality attributes[J]. International Journal of Pharmaceutics,2021,598:120335.
[22]张淼,何瑶. 卡巴他赛纳米混悬剂的制备与质量评价[J].中国药师,2018,21(7):1167 - 1171.
[23]马福旺,宋金春,郭咸希. HPLC 法测定马钱子碱固脂纳米粒冻干粉的包封率和载药量[J]. 中国药师,2009,12(12):1716 - 1718.
[24]李亚男,王文锋,徐月红. 多西他赛他莫昔芬复方脂质体包封率的测定[J]. 北方药学,2020,17(10):1 - 5.
[25]杨子毅,盛利娟,朱霖,等. 纳米药物体外溶出测定方法研究进展[J]. 医药导报,2022,41(11):1615 - 1621.[26]SIEVENS - FIGUEROA L,PANDYA N,BHAKAY A,et al.Using USP Ⅰ and USP Ⅳ for discriminating dissolution ratesof nano - and microparticle - loaded pharmaceutical strip -films[J]. AAPS PharmSciTech,2012,13(4):1473 - 1482.

来源:Internet


