创新药物的获批,不仅仅代表着我们国家药物研发的发展,更意味着患者有了更多更新的治疗选择,根据国家药品监督管理局(NMPA)官网批件信息统计,2023年共有超过80款新药在中国首次获批上市,其中获批的1类新药超30款(不包括诊断类药物和疫苗),创下近年来的新高。本文章汇总并简介了2023年NMPA批准上市的1类化学新药和1类生物制品,不包含中药、血液制品等。
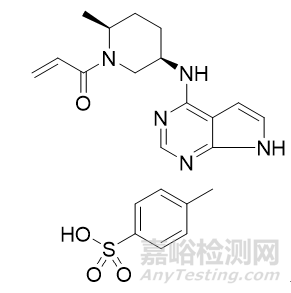
艾诺米替片
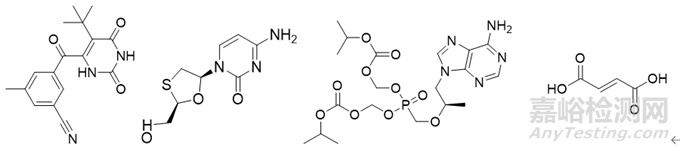
2023年1月4日,NMPA发布公告,宣布批准江苏艾迪药业申报的1类新药艾诺米替片(商品名:复邦德)上市,该药物有效成分由艾诺韦林、拉米夫定(3TC)和富马酸替诺福韦二吡呋酯(TDF)组成的复方制剂,用于治疗成人HIV-1感染初治患者。其中,艾诺韦林片为艾迪药业研发的治疗HIV感染的新一代非核苷类逆转录酶抑制剂,TDF、3TC 为治疗 HIV 的核苷类逆转录酶抑制剂。
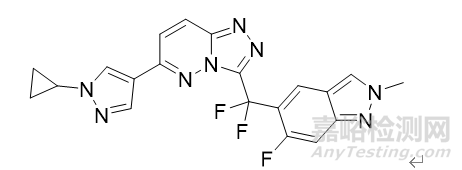
琥珀酸莫博赛替尼胶囊
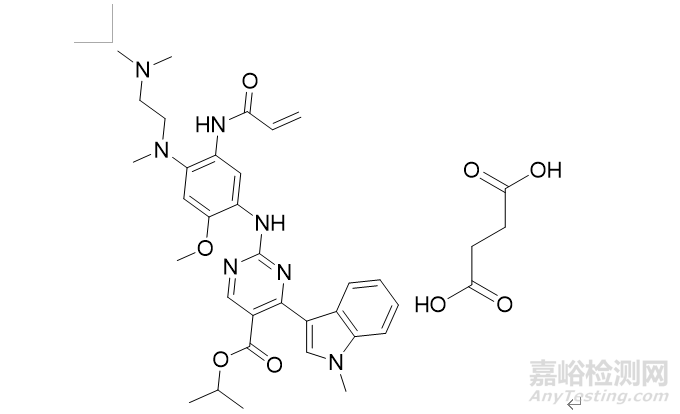
2023年1月11日,NMPA发布公告,宣布武田制药公司申报的1类创新药琥珀酸莫博赛替尼胶囊(商品名:安卫力/EXKIVITY)上市。该药适用于含铂化疗期间或之后进展且携带表皮生长因子受体(EGFR)20号外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。莫博赛替尼是一种靶向EGFR第20外显子插入突变的不可逆的酪氨酸激酶抑制剂,是首个且目前唯一获批专为EGFR 20号外显子插入突变晚期非小细胞肺癌患者研发的口服靶向药物。
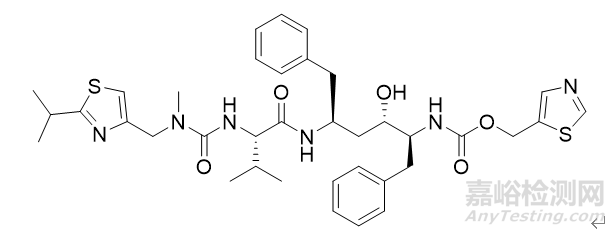
先诺特韦片/利托那韦片组合包装
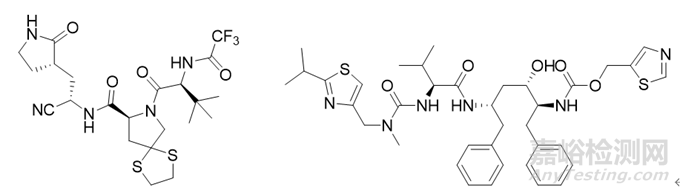
2023年1月29日,NMPA发布公告,宣布附条件批准海南先声药业有限公司申报的1类创新药先诺特韦片/利托那韦片组合包装(商品名称:先诺欣)上市,用于治疗轻中度新型冠状病毒感染(COVID-19)的成年患者。
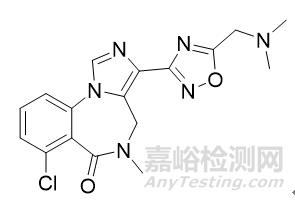
氢溴酸氘瑞米德韦片
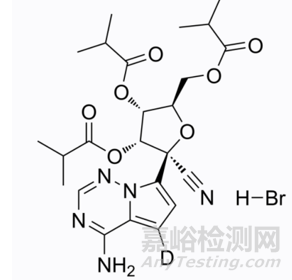
2023年1月29日,NMPA发布公告,宣布附条件批准上海君实生物医药科技有限公司申报的1类创新药氢溴酸氘瑞米德韦片(商品名称:民得维)上市,用于治疗轻中度新型冠状病毒感染(COVID-19)的成年患者。该药物是一种具有高度口服活性的核苷类抗病毒剂,可抵抗SARS-CoV-2和呼吸道合胞病毒(RSV)感染,是国产首个靶向COVID-19 的氘代物。
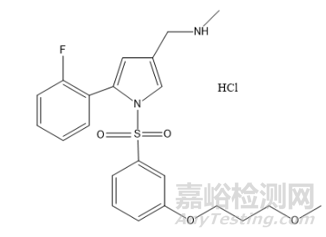
盐酸凯普拉生片
2023年2月15日,NMPA发布公告,宣布批准江苏柯菲平医药股份有限公司申报的1类创新药盐酸凯普拉生片上市。该药品适用于十二指肠溃疡和反流性食管炎的治疗。盐酸凯普拉生是一种新型钾离子竞争性酸阻滞剂,通过与H+-K+-ATP酶上的K+结合位点结合,抑制胃酸分泌。
阿得贝利单抗注射液
2023年2月28日,NMPA发布公告,宣布批准江苏恒瑞申报的1类创新药阿得贝利单抗注射液上市,用于联合化疗一线治疗广泛期小细胞肺癌(ES-SCLC),本品是一种人源化抗 PD-L1 单克隆抗体,能够通过与 PD-L1 特异性结合,阻断 PD-1/PD-L1 信号传导通路,恢复 T 细胞对于肿瘤细胞的免疫应答,激发机体对肿瘤细胞的杀伤作用,发挥抗肿瘤作用。
谷美替尼片
2023年3月8日,NMPA发布公告,宣布附条件批准上海海和药物研究开发股份有限公司申报的1类创新药谷美替尼片上市。该药品适用于具有间质-上皮转化因子(MET)外显子14跳变的局部晚期或转移性非小细胞肺癌的治疗。谷美替尼能够选择性抑制c-Met激酶活性,进而抑制肿瘤细胞的增殖、迁移和侵袭。
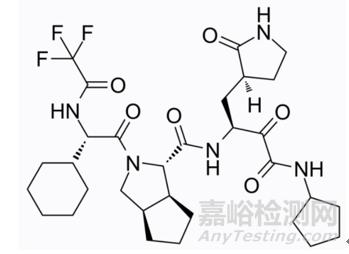
来瑞特韦片
2023年3月23日,NMPA发布公告,宣布附条件批准广东众生睿创生物科技有限公司申报的1类创新药来瑞特韦片(商品名称:乐睿灵)上市。来瑞特韦是一种具有口服活性的SARS-CoV-2 主要蛋白酶慢紧抑制剂,为口服小分子新冠病毒感染治疗药物,用于治疗轻中度新型冠状病毒感染(COVID-19)的成年患者。
艾贝格司亭α注射液
2023年5月6日,NMPA发布公告,宣布批准亿一生物申报的1类创新药艾贝格司亭α注射液上市,用于成年非髓性恶性肿瘤患者在接受容易引起发热性中性粒细胞减少症的骨髓抑制性抗癌药物治疗时,降低以发热性中性粒细胞减少症为表现的感染发生率。
泽贝妥单抗注射液
2023年5月12日,NMPA发布公告,宣布批准博锐生物制药有限公司申报的1类创新药泽贝妥单抗注射液上市,适用于CD20(B淋巴细胞表面携带的一种分子标记物)阳性弥漫大B细胞淋巴瘤。该药是国内首个获批上市的国产CD20抗体1类新药。
奥磷布韦片
2023年5月17日,NMPA发布公告,宣布批准南京圣和药业股份有限公司申报的1类创新药奥磷布韦片(商品名:圣诺迪)上市。该药为我国自主研发并拥有自主知识产权的创新药,适用于与盐酸达拉他韦联用,治疗初治或干扰素经治的基因1、2、3、6型成人慢性丙型肝炎病毒(HCV)感染,可合并或不合并代偿性肝硬化。奥磷布韦是HCV NS5B RNA依赖性RNA聚合酶(为病毒复制所必需)抑制剂,是一种核苷酸前体药物,在细胞内代谢为具有药理活性的代谢产物(SH229M3),可被NS5B聚合酶嵌入HCV RNA中而终止复制。
甲磺酸贝福替尼胶囊
2023年5月17日,NMPA发布公告,宣布批准贝达药业股份有限公司申报的1类创新药甲磺酸贝福替尼胶囊(商品名:赛美纳)上市。该药适用于既往经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂治疗出现疾病进展,并且伴随EGFR T790M 突变阳性的局部晚期或转移性非小细胞肺癌患者的治疗。甲磺酸贝福替尼是第三代表皮生长因子受体酪氨酸激酶抑制剂,能够选择性地抑制EGFR敏感突变和EGFR T790M耐药突变激酶。
伏罗尼布片
2023年6月8日,NMPA发布公告,宣布批准贝达药业股份有限公司申报的1类创新药伏罗尼布片(商品名:伏美纳)上市。该药品与依维莫司联合,用于既往接受过酪氨酸激酶抑制剂治疗失败的晚期肾细胞癌患者。伏罗尼布为多靶点受体酪氨酸激酶抑制剂,对VEGFR2、KIT、PDGFR、FLT3和RET均有较强的抑制作用,主要通过抑制新生血管形成发挥抗肿瘤作用。
安奈拉唑钠肠溶片
2023年6月25日,NMPA发布公告,宣布批准轩竹(北京)医药科技有限公司申报的1类创新药安奈拉唑钠肠溶片(商品名:安久卫)上市。该药为我国自主研发并拥有自主知识产权的创新药,适用于治疗十二指肠溃疡。安奈拉唑为质子泵抑制剂,属于苯并咪唑类化合物,可通过抑制胃壁细胞H+-K+-ATP酶活性和降低质子转运能力而抑制胃酸分泌。
磷酸瑞格列汀片
2023年6月28日,NMPA发布公告,宣布批准江苏恒瑞医药股份有限公司申报的1类创新药磷酸瑞格列汀片(商品名:瑞泽唐)上市,该药适用于改善成人2型糖尿病患者的血糖控制。磷酸瑞格列汀是二肽基肽酶4(DPP-4)抑制剂,通过抑制DPP-4水解肠促胰岛激素,从而增加活性形式的胰高血糖素样肽-1(GLP-1)和葡萄糖依赖性促胰岛素多肽(GIP)的血浆浓度,以葡萄糖依赖的方式增加胰岛素释放并降低胰高血糖素水平,进而降低血糖。
奥特康唑胶囊
2023年6月28日,NMPA发布公告,宣布批准eVENUS PHARMACEUTICAL LABORATORIES INC.申报的1类创新药奥特康唑胶囊上市。该药品用于治疗重度外阴阴道假丝酵母菌病(VVC)。奥特康唑是一种抗真菌药物,属唑类金属酶抑制剂,靶向抑制真菌甾醇14α去甲基化酶(CYP51)。
伊鲁阿克片
2023年6月28日,NMPA发布公告,宣布批准鲁制药有限公司申报的1类创新药伊鲁阿克片(商品名:启欣可)上市。该药适用于既往接受过克唑替尼治疗后疾病进展或对克唑替尼不耐受的间变性淋巴瘤激酶(ALK)阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者的治疗。伊鲁阿克为ALK抑制剂,可通过抑制 ALK 和 ROS1 激酶的磷酸化进而阻断 ERK、STAT5 和 AKT 等下游信号通路蛋白的激活,从而诱导肿瘤细胞死亡(凋亡)。
培莫沙肽注射液
2023年6月30日,NMPA发布公告,宣布批准江苏豪森药业集团有限公司申报的1类创新药培莫沙肽注射液(商品名:圣罗莱)上市。该药适用于未接受红细胞生成刺激剂(ESA)治疗的成人非透析患者,及正在接受短效促红细胞生成素(EPO)治疗的成人透析患者(本品不适用于在需要立即纠正贫血的患者中替代红细胞输注)。培莫沙肽是长效多肽类EPO受体激动剂,可促进体内红细胞增殖,改善慢性肾病患者的贫血及相关症状。
拓培非格司亭注射液
2023年6月30日,NMPA发布公告,宣布批准特宝生物申报的1类新药拓培非格司亭注射液上市,用于非髓性恶性肿瘤患者在接受容易引起发热性中性粒细胞减少症的骨髓抑制性抗癌药物治疗时,降低以发热性中性粒细胞减少症为表现的感染发生率。拓培非格司亭注射液为Y型聚乙二醇(PEG)修饰的人粒细胞刺激因子(rhG-CSF),通过刺激骨髓造血干细胞向粒细胞分化,促进粒细胞增殖、成熟和释放,恢复外周血中性粒细胞数量,以降低肿瘤患者化疗后的感染发生率。
伊基奥仑赛注射液
2023年6月30日,NMPA发布公告,宣布附条件批准南京驯鹿生物医药有限公司申报的1类新药伊基奥仑赛注射液(商品名:福可苏)上市。该药品用于治疗复发或难治性多发性骨髓瘤成人患者,既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)。伊基奥仑赛注射液是一种自体免疫细胞注射剂,系采用慢病毒载体将靶向B细胞成熟抗原(BCMA)的嵌合抗原受体(CAR) 基因整合入患者自体外周血CD3阳性T细胞后制备。回输患者体内后,通过识别多发性骨髓瘤细胞表面的BCMA靶点杀伤肿瘤细胞。
托莱西单抗注射液
2023年8月16日,NMPA发布公告,宣布批准信达生物制药申报的1类新药托莱西单抗注射液(商品名:信必乐)上市。该药品适应症为在控制饮食的基础上,与他汀类药物、或者与他汀类药物及其他降脂疗法联合用药,用于在接受中等剂量或中等剂量以上他汀类药物治疗,仍无法达到低密度脂蛋白胆固醇(LDL-C)目标的原发性高胆固醇血症(包括杂合子型家族性和非家族性高胆固醇血症)和混合型血脂异常的成人患者。托莱西单抗注射液为前蛋白转化酶枯草溶菌素9(PCSK9)抑制剂。通过抑制PCSK9,阻断血浆PCSK9与低密度脂蛋白受体(LDLR)的结合,进而阻止LDLR的内吞和降解,增加细胞表面LDLR表达水平和数量,增加LDLR对低密度脂蛋白胆固醇(LDL-C)的重摄取,降低循环LDL-C水平,最终达到降低血脂的目的。
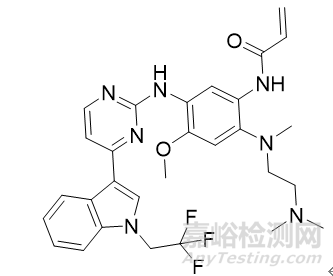
舒沃替尼片
2023年8月23日,NMPA发布公告,宣布批准迪哲(江苏)医药股份有限公司申报的1类创新药舒沃替尼片(商品名:舒沃哲)上市。该药适用于既往经含铂化疗治疗时或治疗后出现疾病进展,或不耐受含铂化疗,并且经检测确认存在表皮生长因子受体(EGFR)20号外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)的成人患者。舒沃替尼是一种EGFR酪氨酸激酶抑制剂。
纳鲁索拜单抗注射液
20239月6日,NMPA发布公告,宣布附条件批准上海津曼特生物科技有限公司申报的纳鲁索拜单抗注射液(商品名:津立生)上市。该药品用于治疗不可手术切除或手术切除可能导致严重功能障碍的骨巨细胞瘤成人患者。纳鲁索拜单抗注射液为重组全人源抗核因子-κB受体活化因子配体(RANKL)单克隆抗体,通过与细胞表面的RANKL特异性结合,抑制RANKL活性,从而抑制其参与介导所引起的骨质溶解和肿瘤生长。
氘可来昔替尼片
2023年10月19日,NMPA发布公告,宣布批准百时美施贵宝公司申报的1类创新药氘可来昔替尼片(商品名:颂狄多)上市。该药适用于适合系统治疗或光疗的成年中重度斑块状银屑病患者。氘可来昔替尼是一种酪氨酸激酶2(TYK2)抑制剂。
甲苯磺酸利特昔替尼胶囊
2023年10月19日,NMPA发布公告,宣布通过优先审评程序批准辉瑞公司申报的1类创新药甲苯磺酸利特昔替尼胶囊(商品名:乐复诺)上市。该药适用于12岁及以上青少年和成人重度斑秃患者。甲苯磺酸利特昔替尼是一种激酶抑制剂,能够不可逆地抑制 JAK3和酪氨酸激酶家族。
注射用埃普奈明
2023年11月2日,NMPA发布公告,宣布批准武汉海特生物制药股份有限公司申报的注射用埃普奈明(商品名:沙艾特)上市。该药品联合沙利度胺和地塞米松用于既往接受过至少2种系统性治疗方案的复发或难治性多发性骨髓瘤成人患者。注射用埃普奈明为重组变构人肿瘤坏死因子相关凋亡诱导配体,可结合并激活肿瘤细胞表面的死亡受体4(DR4)/死亡受体5(DR5),通过外源性细胞凋亡途径触发细胞内Caspase级联反应,从而发挥抗肿瘤作用。
纳基奥仑赛注射液
2023年11月8日,NMPA发布公告,宣布附条件批准合源生物申报的纳基奥仑赛注射液(商品名:源瑞达)上市。该药品用于治疗成人复发或难治性B细胞急性淋巴细胞白血病。纳基奥仑赛注射液是通过基因修饰技术将靶向 CD19 的嵌合抗原受体(CAR)表达于 T 细胞表面而制备成的自体 T 细胞免疫治疗产品。输注至体内后会与表达 CD19 的靶细胞结合,激活下游信号通路,诱导 CAR-T 细胞的活化和增殖并产生对靶细胞的杀伤作用。
伯瑞替尼肠溶胶囊
2023年11月16日,NMPA发布公告,宣布附条件批准北京浦润奥生物科技有限责任公司申报的1类创新药伯瑞替尼肠溶胶囊上市。该药适用于治疗具有间质-上皮转化因子(MET)外显子14跳变的局部晚期或转移性非小细胞肺癌患者。伯瑞替尼是一种细胞-间质上皮转化因子(c-MET)受体酪氨酸激酶抑制剂,可抑制 c-MET高表达肿瘤细胞的增殖。
阿泰特韦片/利托那韦片组合包装
2023年11月24日,NMPA发布公告,宣布附条件批准福建广生中霖生物技术有限公司申报的1类创新药阿泰特韦片/利托那韦片组合包装(商品名称:泰中定)上市。该药品为口服小分子新冠病毒感染治疗药物,用于治疗轻型、中型新型冠状病毒感染( COVID -19)的成年患者。
地达西尼胶囊
2023年11月29日,NMPA发布公告,宣布批准浙江京新药业股份有限公司申报的1类创新药地达西尼胶囊上市。该药适用于失眠患者的短期治疗。地达西尼属于苯二氮䓬类药物,是γ-氨基丁酸A型(GABAA)受体的部分正向别构调节剂,通过部分激活GABAA受体,产生促进睡眠的作用。
索卡佐利单抗注射液
2023年12月21日,NMPA发布公告,宣布批准兆科肿瘤药物有限公司申报的1类新药索卡佐利单抗注射液上市,用于治疗复发性或转移性宫颈癌。该产品能与PD-L1蛋白结合,阻断PD-L1蛋白与其受体PD-1间的相互作用,从而解除PD-1或PD-L1信号通路对T细胞的抑制,增强T细胞对肿瘤的杀伤作用。而且,它还能够通过传统的抗体依赖性细胞介导的细胞毒作用(ADCC)来杀死癌细胞。
总结
2023年度NMPA批准的1类新药大致分为肿瘤领域、消化系统领域、内分泌系统领域、呼吸系统领域等,明显看出,肿瘤仍是众多药企争相追逐的重要市场,其次是抗感染药,第三为抗变态反应药物。2023年我国新药获批数量呈明显的上升趋势,国产创新药占主要比例,也期待新的一年中国创新药研发有更进一步的突破,有更多新药好药造福患者。