您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-12-02 03:58
机械循环辅助(MCS)装置是一种生命支持技术,在20世纪50年代首先被应用于临床,经过几十年的发展,已经成为心脏急性事件及终末期心力衰竭等患者的重要“桥梁”治疗,临床应用也越来越广泛。
主动脉内球囊反搏(IABP)
IABP通常通过腋动脉或股动脉插入,使用反搏来增加平均动脉血压、冠状动脉灌注和心输出量,从而降低左心室舒张末压、左心室壁应力和心肌需氧量。IABP提供的支持质量取决于心率、心律和全身血管阻力这些因素。
IABP的禁忌证包括严重的外周血管疾病和主动脉夹层、迂曲和动脉瘤。此外,如果存在有临床意义的主动脉瓣反流的情况下,反搏会适得其反,导致左心室壁压力增加,而不是产生预期的心脏保护作用。
经皮左心室辅助装置
经皮左心室支持装置的两个主要类别是轴流泵(如Impella)和体外离心装置,两种装置都可以增加心输出量和平均动脉血压,并相应增加冠状动脉和全身灌注压。有效的左心室“去负荷”可降低左心室舒张末压,从而降低室壁张力和心肌需氧量。微轴流装置穿过主动脉瓣,连续排出左心室腔内的血液,实现“去负荷”。
放置左侧微轴流泵的禁忌证包括严重的主动脉瓣狭窄(≤0.6 cm2)、中重度主动脉瓣反流、有临床意义的外周动脉疾病以及机械主动脉瓣或左心室血栓。
Impella装置的理想位置是主动脉瓣下方约3.5 cm,进入左心室中部。
TandemHeart经皮辅助装置是一种连续流动的离心泵,用于左心房到股动脉系统。其工作原理是通过房间隔穿刺,将导管放置至左心房,轴流泵将血液从左心房抽吸出来后,再回输至主动脉,达到心脏辅助的作用。尽管使用TandemHeart观察到血流动力学方面的获益,但由于需要经房间隔穿刺,尚未广泛应用,特别是在紧急情况下。放置不当或装置移位到右心房可导致大量脱氧血液从右向左分流。因此,器械固定至关重要,因为位置的微小变化也会损害预期的循环支持效果。
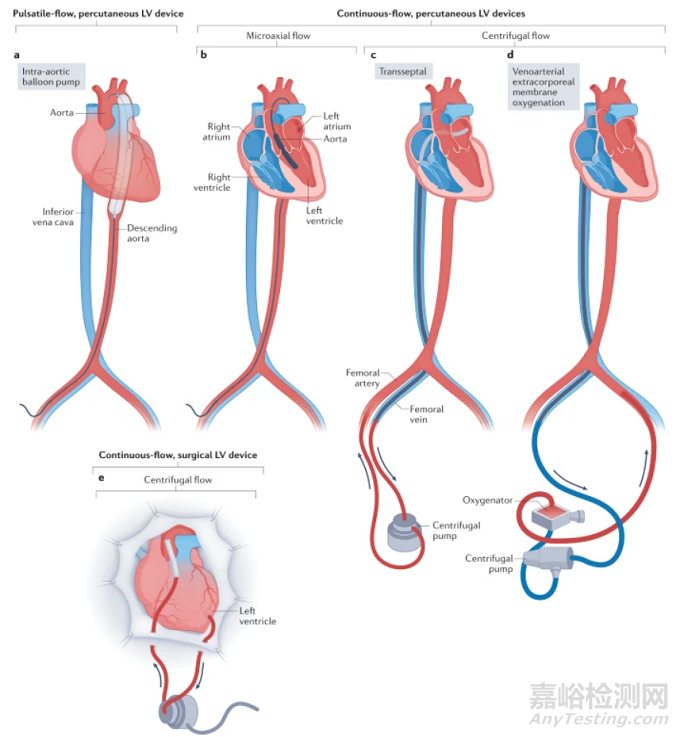
左心室循环辅助装置
经皮右心室辅助装置
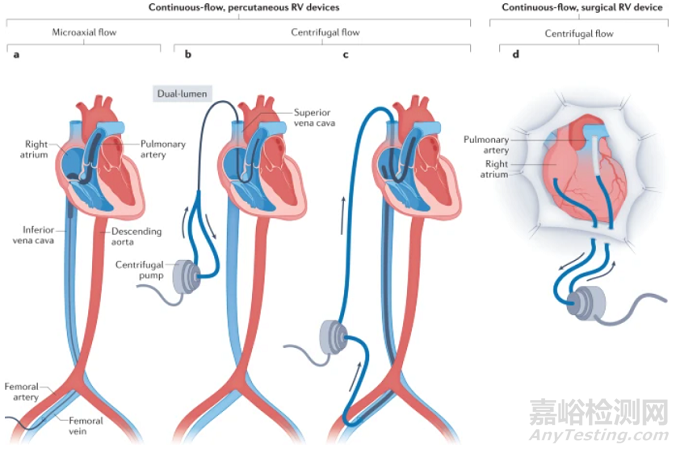
右心室循环辅助装置
经皮右心室装置也包括微轴装置和体外离心泵装置,可直接降低右心房和右心室压,增加通过肺动脉的血流量,在保留或辅助左心室功能的情况下,使平均肺动脉压、左心室前负荷以及心输出量增加。
Impella RP系统是一种经皮微轴右室辅助装置,其工作原理与其他Impella设备相同。尽管缺乏在右心室衰竭情况下普遍或常规使用Impella RP的数据,但其已获得紧急使用授权,专门用于治疗与新冠肺炎相关的右心室衰竭,包括肺栓塞患者。
ProtekDuo在设计上与Impella RP不同,它是一种双腔经皮右室辅助装置,可将血液从右心房引入肺动脉,并连接到外部离心泵。该系统支持高达5 l/min的血流量,并且可以插入氧合器进行体外膜肺氧合(ECMO)。ProtekDuo有两种尺寸(29 F和31 F),通常通过右颈内静脉插入。
双腔套管(Spectrum Medical)是另一种先进的双腔经皮右心室辅助装置,通过右颈内静脉插入并连接到离心泵和氧合器(如果有需要)。与ProtekDuo不同,双腔套管辅助装置从右心室排出血液并将血液返回肺动脉。与通过股静脉插入的装置相比,ProtekDuo和双腔插管装置通过颈内静脉插入,患者活动性更大。
右侧器械放置的禁忌证包括机械三尖瓣或肺动脉瓣、重度三尖瓣或肺动脉瓣狭窄或反流、不利于支持装置插入的肺动脉壁病变以及右心房或腔静脉壁血栓。
静脉动脉体外膜肺氧合
静脉动脉(VA)ECMO使用离心泵将静脉血从右心房抽出,通过膜氧合器并经由流出套管进入动脉循环。通常,静脉流入套管(18F-28F)插入股静脉并推送到右心房,而动脉流出套管(15F-19F)放置在股动脉中。其他插管部位包括腋窝血管或通过开胸术或胸骨切开术进行中心插管。
常见适应证包括接受支持治疗时肺毛细血管楔压持续升高(>15 mmHg)或肺动脉舒张压(>25 mmHg)、整个心动周期主动脉瓣关闭、持续性肺水肿、难治性室性心律失常或超声心动图可见左心室扩张。在心源性休克患者中,在ECMO环境下进行微轴流泵辅助左心室减压(所谓的ECPella)已被证明可降低30天死亡率,但由于与单独使用ECMO相比,其并发症发生率不同,其广泛使用仍存在争议。
临床应用
1. 心源性休克
药物治疗无效的心源性休克是临时机械循环辅助装置的最常见指征,可选择的MCS装置包括IABP、pLVAD、VA ECMO。
2. 高危PCI围术期辅助
PCI期间的MCS最常用于AMI-CS患者和接受高风险冠状动脉手术的患者。年龄较大、伴或不伴血流动力学损伤的复杂冠状动脉疾病、射血分数降低和其他相关合并症的患者符合高风险标准。在这些患者中,手术时间通常较长,冠状动脉和全身灌注不足,MCS辅助的PCI可以为完全血运重建留出时间,同时提供足够的心输出量、左心室去负荷以及心肌和终末器官灌注。可选择的MCS装置包括IABP、pLVAD。
目前的AHA/ACC指南指出,对于特定的高危患者,选择性使用血流动力学支持装置作为PCI的辅助手段可能是合理的(IIb)。ESC指南建议,在非紧急、高风险的PCI手术中,应考虑临时MCS,由经验丰富的术者在可获得循环支持和心血管手术的中心进行。
3. 电生理手术
在电生理学手术中使用临时MCS有助于血流动力学不稳定的室性心动过速(VT)的基底标测和消融,以及减轻术后心力衰竭和血流动力学损害。
临时MCS也用于高危患者人群的电生理手术,以减少消融术后急性血流动力学失代偿和心力衰竭恶化。对于考虑进行室速消融术的高风险患者(PAINESD 评分高),可咨询心力衰竭专家和心脏外科医生,考虑预防性使用临时MCS,并酌情评估晚期治疗,如心脏移植或长期MCS。
可选择的MCS装置包括pLVAD、VA ECMO。
4. 心脏手术
虽然MCS最常用于手术后血流动力学衰竭的挽救,但在接受复杂或高风险手术的特定患者中,其作为辅助手段的使用也在增加。
①手术干预前心源性休克的管理
各种瓣膜病、心肌或冠状动脉疾病进行手术干预时可能会发生心源性休克,此时的手术风险较高。临时MCS可作为过渡的桥梁,避免手术相关的死亡风险,为紧急手术赢得准备时间。
②预防性应用于接受手术的高危患者
术后心源性休克和由此导致的多器官功能障碍仍是心脏手术后早期死亡的主要原因,因此,对于正在接受手术的高风险患者,预防性的临时MCS可以提供保护,并促进术后早期的心脏恢复。
③心脏切开术后休克和围术期循环衰竭
心功能不全或损伤、心肌保护不足、缺血再灌注损伤和/或手术并发症都会导致心脏切开术后心源性休克的风险。在这种极端血流动力学损害的情况下,ECMO是最常用的临时MCS形式。但是如果心脏恢复或修复的可能性不大,通常不建议使用临时MCS(ECMO),除非可以选择持久性支持或心脏移植。
虽然心脏手术后循环衰竭并不常见,但其与术后30天死亡率>50%相关。当术后心脏骤停的情况下常规复苏失败时,可以进行体外心肺复苏(ECMO或体外循环)。
5. 晚期心衰
对于患有心力衰竭的手术风险高的特定患者,在进行持久MCS手术之前,可以考虑使用临时MCS,以实现临床稳定性和维持终末器官灌注。
如果在心脏移植时同种异体移植功能欠佳(原发性移植功能障碍),可以使用ECMO、IABP或其他形式的临时MCS,为移植赢取时间,并保持足够的终末器官灌注。
来源:
Benjamin S. Salter, Caroline R. Gross, Menachem M. Weiner, et al. Temporary mechanical circulatory support devices: practical considerations for all stakeholders. Nature Reviews Cardiology, 10 November 2022.

来源:医心


