您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-08-26 12:36
近日,江苏畅医达医疗科技有限公司研发的“颅内动脉瘤辅助栓塞支架”获批上市,下面嘉峪检测网与您一起了解一下该产品在临床前研发阶段做了哪些实验。
一、颅内动脉瘤辅助栓塞支架的结构与组成
该产品由颅内支架、输送元件组成,部分规格含有输送导管。其中,输送元件由输送杆和导入鞘组成;输送导管由微导管和塑形针组成。产品以无菌状态提供,经环氧乙烷灭菌,一次性使用,货架有效期3年。
二、颅内动脉瘤辅助栓塞支架的适用范围
该产品适用于≥18岁的颅内动脉瘤患者,辅助弹簧圈治疗囊状宽颈(瘤颈≥4mm或瘤体/瘤颈比<2)动脉瘤,动脉瘤位于前循环(颈内动脉、大脑中动脉M1/M2段、前交通动脉、大脑前动脉),载瘤血管直径≥2.0mm且≤5.2mm。
三、颅内动脉瘤辅助栓塞支架的工作原理
该产品为自扩张血管支架系统,用于辅助弹簧圈栓塞治疗颅内动脉瘤。支架释放后紧贴血管内壁封堵动脉瘤的瘤口,防止弹簧圈移位或脱落至正常血管及分支血管内。
四、颅内动脉瘤辅助栓塞支架的性能研究
产品技术要求研究项目包括:
1、支架:支架外观、支架尺寸、局部挤压、支架网孔密度、支架金属覆盖率、支架短缩率、相变温度、支架耐腐蚀、弯曲打折、径向支撑力;
2、输送元件:输送杆外观、输送杆尺寸、输送杆的耐腐蚀性、输送杆峰值拉力、输送杆弯曲性能、输送杆破裂性能、导入鞘尺寸、导入鞘峰值拉力、导入鞘外观、导入鞘配合性能;
产品性能研究包括支架物理和机械性能、模拟使用性能、疲劳性能、有限元分析、MRI兼容性等。
五、颅内动脉瘤辅助栓塞支架的生物相容性研究
产品由颅内支架和输送元件组成,部分规格含有输送导管。颅内支架为植入器械,与循环血液长期接触;输送元件和输送导管为外部接入器械,与循环血液短期接触;畅医达对植入器械及外部接入器械分别进行了生物相容性评价。
生物相容性评价内容表
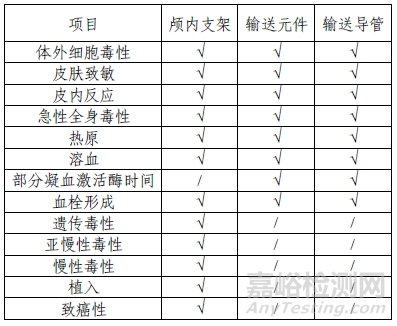
六、颅内动脉瘤辅助栓塞支架的灭菌
产品采用环氧乙烷灭菌,无菌状态提供。灭菌确认报告证明无菌保证水平达10⁻⁶,并对残留毒性进行了研究。
七、颅内动脉瘤辅助栓塞支架的有效期和包装研究
产品货架有效期为3年。畅医达通过加速老化和实时老化验证,包括产品稳定性、包装完整性和模拟运输验证,确保产品在有效期内性能符合要求。
八、颅内动脉瘤辅助栓塞支架的动物研究
该研究目的为评价颅内动脉瘤辅助栓塞支架在新西兰大白兔动脉瘤模型中的有效性、安全性和可操作性。植入后30天、90天、180天分别进行观察,评估动脉瘤治疗效果和对血管组织的影响等。评价指标包括:

来源:嘉峪检测网


