您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-10-30 09:46
泡沫气雾剂近些年来受到国外制药界越来越多的关注,但是在国内发展却十分缓慢。本文从泡沫剂的概念、文献报道、国内外泡沫剂研发情况、泡沫剂处方组成及制备工艺、实例分析等方面简要介绍了这一给药系统,以使读者对其有更多的了解。由于本人能力有限,文中不足之处还望各位同仁批评指正。
什么是泡沫剂
2020版《中国药典》中没有收录任何泡沫剂品种,仅在制剂通则0113气雾剂中提到若气雾剂内容物喷出后呈泡沫状则称为泡沫剂。《欧洲药典》在Monograph 1105中对药用泡沫剂(medicated foam)有较为详细的论述,且提供了两种泡沫剂的表征方法。《欧洲药典》将药用泡沫剂定义为“由药物、表面活性剂和其他辅料组成,并将大量气体分散在上述成分组成的液体中形成的一种制剂”。《美国药典》在1151制剂通则中将泡沫剂定义为“含有分散在液体中的气泡的制剂”,并进一步说明液体应包含活性药物和合适的辅料,可以采用加压容器包装或使用其它的特殊给药装置(如非加压容器)。《美国药典》将这种包装在加压容器中的泡沫剂又称为“foam aerosol”(泡沫气雾剂),其中包含一种或多种活性药物、表面活性剂、水性或非水性液体和抛射剂,目前国外上市的药用泡沫剂大多属于这一类型,本文也重点讨论这种填充抛射剂的泡沫气雾剂。泡沫气雾剂储存于密闭的加压罐装容器中,使用时通过揿压阀门,内容物以泡沫形状喷出。泡沫的密度小,对炎症黏膜的化学刺激和物理刺激性小,吸附性强,较其它传统外用制剂(如软膏剂等)更容易涂布于表皮,患者使用的顺应性好。此外,药用泡沫剂凭借其产生的过饱和环境可促进药物渗透,从而提高药物的生物利用度。
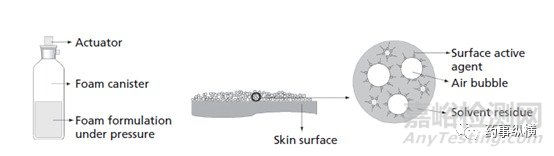
图1泡沫气雾剂
文献情况
上世纪六七十年代,美国杜邦公司(氟利昂即为该公司研发)的气雾剂专家Paul A. Sanders一直从事泡沫剂的研究工作,他在所编写的Handbook of AerosolTechnology一书中系统全面地介绍了泡沫剂的理论。1977年Woodward和Berry首次报道了泡沫剂在皮肤病治疗中的应用,他们研究了倍他米松苯甲酸酯水醇型“快速破裂”(quick-break)泡沫剂与对应的其他半固体剂型的治疗效果,血管收缩实验结果表明该泡沫剂的治疗效果与软膏剂类似,且优于该药的乳膏剂型。2003年,Purdon等人发表了第一篇药用泡沫剂的综述文章(Foam drug delivery indermatology: Beyond the scalp),介绍了泡沫剂给药系统应用于皮肤病治疗领域的优势及前景。2006年,以色列Foamix公司首席科学家Tamarkin发表综述文章“Emollient foam intopical drug delivery”,阐述了乳剂型泡沫剂的处方组成和理化特性,以及这类泡沫气雾剂在皮肤外用给药的优势。2010年,A. Arzhavitina等人在《国际药剂学杂志》发表综述文章“Foams forpharmaceutical and cosmetic application”,从泡沫结构、产生机理、给药装置、泡沫稳定性和泡沫的表征、泡沫剂在制药及个人护理领域的应用等方面进行了详尽地介绍。同一年,天津大学药学院教授赵燕军等人发表文章“Dynamic foams intopical drug delivery”,从辅料选择、处方制备、泡沫稳定性、质量评价以及泡沫剂用于局部给药的优势(如增强药物皮肤渗透)等方面进行了较为详细地阐述。2017年, Tamarkin又撰写了“Foam: A Unique Delivery Vehiclefor Topically Applied Formulations”一文,系统地介绍了泡沫剂的分类以及各类泡沫剂的特点,还对泡沫气雾剂的制备和评价方法进行了简要概述。2019年,Parsa等人发表文章“Foam in pharmaceutical andmedical applications”,对近年来皮肤外用局部泡沫的最新发展情况进行了综述,根据不同泡沫剂配方的不同对其进行了分类,并介绍了文献中局部外用泡沫的一些重要物理参数的测定方法。
国内外泡沫剂研发情况
目前国内通过国家药品监督管理局批准的药用泡沫剂仅有两个,分别是贵州汉方药业的“妇得康泡沫剂”和贵州宏宇药业的“保妇康泡沫剂”,均为中药泡沫剂,用于女性妇科疾病。北京京卫燕康药物研究所有限公司在国内药用泡沫剂研究方面处于领先地位,已有酮康唑泡沫剂和米诺地尔泡沫剂两个品种获得独家临床批件,另有布地奈德泡沫剂、卡伯三醇泡沫剂、地奈德泡沫剂、戊酸倍他米松泡沫剂等项目处于实验室小试阶段。
美国食品药品监督管理局在2004年至2016年13年间共批准了31个药用泡沫剂产品(如下图所示),近几年也陆续有新的品种上市。
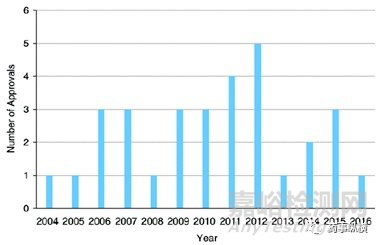
图2FDA批准的泡沫剂数量
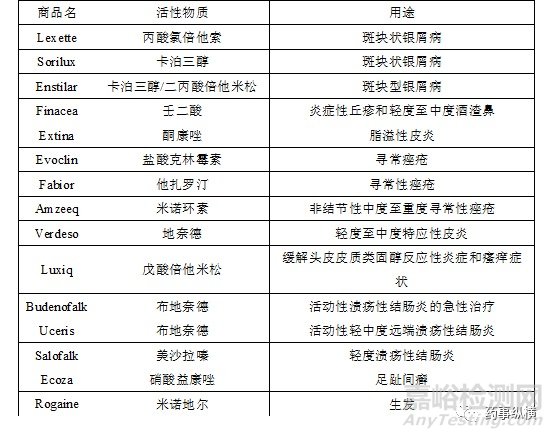
国外药用泡沫剂产品主要集中于治疗皮肤炎症、痤疮、银屑病等皮肤疾病治疗方面,如酮康唑泡沫剂、卡泊三醇泡沫剂、他扎罗汀泡沫剂、丙酸氯倍他索泡沫剂、地奈德泡沫剂、米诺环素泡沫剂等。部分已上市的药用泡沫剂品种信息如下表所示:
表1部分已上市的药用泡沫剂品种信息
泡沫剂处方工艺
泡沫剂类型众多,包括水醇型泡沫剂(hydroethanolic foam)、乳剂型泡沫剂(emollient foam/cream foam)、纳米乳泡沫剂(nano-emulsion foam)、油泡沫剂(oil foam)、软膏型泡沫剂(ointment foam)、混悬型泡沫剂(suspension foam)、糖泡沫剂(saccharide foam)、强溶剂泡沫剂(potent solvent foam)等等。本文将详细介绍目前最常见的乳剂型泡沫剂的处方组成及制备工艺。
乳剂型泡沫剂是指预发泡处方为乳状液的一类泡沫制剂。所谓的预发泡处方(pre-foam formulation,PFF)是指在泡沫制剂灌装到加压容器和充填抛射剂前预先制备好的可发泡组合物。乳剂型泡沫剂由水相和油相组成,根据乳状液的类型分为水包油型(o/w)和油包水型(w/o)。此类泡沫剂对皮肤具有重脂化(refatting)作用,可减少皮肤水分流失,有些具有保湿作用(humectant effect),而增加角质层保水能力。乳剂型泡沫剂一般不含乙醇,不会使皮肤干燥或对皮肤产生刺激性(如灼烧感)。此外,处方中具有润肤(emollient)作用的油性成分有助于改善和缓解皮肤干燥和相关的皮肤疾病,如银屑病和特应性皮炎等。乳剂型泡沫剂产生的泡沫应当是热稳定的(theramally stable),即泡沫在皮肤表面温度下不会立即塌陷,泡沫应当是易碎的(breakable),即较小的外部剪切力作用下即可均匀涂布于患处。
关于泡沫的稳定性和破碎性,Foamix公司首席科学家Tamarkin认为稳定型泡沫(stable)不适合用于皮肤疾病的局部治疗,因为它们太过稳定,即使用较大的剪切力也不容易使其破裂,药物不易进入皮肤。快速破裂型泡沫(quick breaking)是热不稳定的(thermolabile),在人体表皮温度下容易快速破裂。这种快速破裂性通常是因为泡沫剂处方中有乙醇存在,因此乳剂型泡沫剂和水醇型泡沫剂(处方中含有大量乙醇)相比,后者更易破裂,泡沫持续时间短。
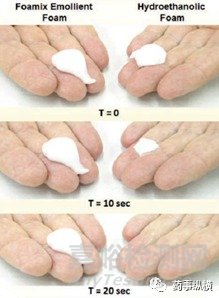
图3 乳剂型泡沫剂VS水醇型泡沫剂塌陷时间
易碎型泡沫(breakable)是热稳定的,即泡沫在皮肤表面的温度下不会立即塌陷,而能在较小的外部剪切力作用下即可均匀涂布于患处。泡沫的稳定性可以用塌陷时间(collapse time)来衡量,指一定量的泡沫被施于皮肤表面后,泡沫在皮肤温度(36℃)下,其高度减少至原来一半所用的时间。从实际使用时的便利性考虑,泡沫应至少在皮肤温度下能保持其结构稳定1分钟,最好大于2分钟或3分钟。
2000年初,FDA批准施泰福实验室(Stiefel)研发的丙酸氯倍他索泡沫剂OLUX®,用于治疗12岁及以上患者头皮中度至重度斑块状牛皮癣和身体其他部位(面部和皮肤擦破区域除外)的中度至重度斑块状牛皮癣。这是一种基于VersaFoam-HF技术的水醇型泡沫剂,处方中的乙醇是主要溶剂,同时也起到渗透促进剂的作用,能够可逆地改变角质层的屏障特性,并通过细胞内途径(intracellular route)驱动药物穿过角质细胞到达活性表皮。此外,由于处方中含有大量的乙醇(占60%),因此OLUX®产生的泡沫是热不稳定的,在皮肤温度下很快就破裂液化(因此使用时不能用手直接接触泡沫),在给药处留下产生了过饱和的药物溶液,也起到促进药物的渗透的作用。但是由于处方中乙醇含量高,在使用时可能会引起刺痛或灼烧感,这可能会降低某些患者的使用意愿。后来,施泰福实验室又开发了丙酸氯倍他索泡沫剂OLUX-E®,用于治疗12岁及以上患者的皮质类固醇反应性皮肤病(又称银屑病和湿疹)的炎症和瘙痒症状。这是一种基于VersaFoam-EF技术的乳剂型泡沫剂,不含乙醇,因此使用时皮肤不会有使用OLUX®泡沫剂的刺激感,泡沫也更稳定,使用时可以将泡沫施放到手上,然后再涂抹于患处,而此前开发的OLUX®泡沫剂在说明书中明确说明不要用手直接接触,否则可能在接触到患处前泡沫就已经液化。该制剂处方中的丙二醇和肉豆蔻酸异丙酯作为渗透促进剂,也可能会使皮肤干燥或存在潜在的刺激性,而处方中的其它成分,如鲸蜡醇、环甲硅油、白凡士林、轻质矿物油作为润肤剂(emollient),能在皮肤表面形成润滑膜,促进皮肤水合,抵消上述不利作用。
4.1乳剂型泡沫剂处方组成
根据Tamarkin等人公开的专利信息,乳剂型泡沫剂一般包括活性药物(API)、水(water)、油(oil)、表面活性剂(surfactants)、聚合物(polymers)、泡沫佐剂(foam adjuvants)、抛射剂(propellant)。此外,根据需要处方中也可加入其他辅料,如极性溶剂、促渗剂、润肤剂、抗氧剂、螯合剂、保湿剂、防腐剂、缓冲剂、PH调节剂等。
4.1.1 活性药物
药用泡沫剂产品中可以只有一种药物,也可为两种或更多药物组成的复方。药物一般溶解在水相或疏水相中,当药物不能完全溶于水相或疏水相时,也可分散在乳液中。可用于制备外用泡沫释药系统的药物包括抗生素类(如四环素、喹诺酮类、大环内酯抗生素等)、抗真菌药(如咪康唑、酮康唑和特比萘芬等)、皮质激素类(如戊酸倍他米松、丙酸氯倍他索、氢化可的松、地奈德等)、维A酸类药物(如他扎罗汀、阿达帕林等)、维生素D3类似物(如钙泊三醇)等等。
4.1.2 油
可供选择的油种类很多,既可以单独使用,也可以两种或两种以上的油合用。常见的有硅油(如二甲硅油、环甲硅油等)、矿物油(如液体石蜡、凡士林等),植物来源的油和酯(如椰子油、大豆油、辛酸/癸酸甘油三酯、肉豆蔻酸异丙酯等),多不饱和脂肪酸(如亚油酸、亚麻酸等)。疏水性溶剂的总含量约占预发泡处方(pre-foam formulation,PFF)的2%至75% (w/w)。较高浓度的疏水性溶剂更适合用于治疗干性皮肤,因其可在皮肤表面形成一层疏水性屏障,减少水分流失。但过高浓度的疏水性溶剂(约25%),会在涂抹后留下油腻感。
4.1.3 表面活性剂
泡沫中的表面活性剂排列在气-液界面处,降低液膜的表面张力,对泡沫的产生及稳定起着非常重要的作用。用量约占PFF的0.1%~5.0% (w/w),一般低于2.0%或1.0%。应根据乳液的类型选择合适HLB值的表面活性剂。通常,水包油乳液要求乳化剂体系的HLB为9-14,油包水乳液组成的泡沫组合物则应选择HLB为4-9的乳化剂体系。离子型表面活性剂是高效的发泡剂,但长期使用或者浓度较大对皮肤具有刺激性,因此最好使用非离子型表面活性剂,如司盘(失水山梨醇脂肪酸酯)、吐温(聚氧乙烯失水山梨醇脂肪酸酯)、卖泽(聚氧乙烯脂肪酸酯)、苄泽(聚氧乙烯脂肪醇醚)、蔗糖脂肪酸酯、脂肪酸甘油酯等。
4.1.4 聚合物
泡沫剂处方中的聚合物也可称为胶凝剂 (gelling agents),可促进具有精细气泡结构的泡沫的产生,泡沫不易塌陷,延长泡沫的持续时间,是用于产生具有所需质地和铺展性能的泡沫的有用组分。此外,一些胶凝剂还具有成膜性,可提高药物在作用部位的滞留时间。用量约占PFF的0.1%~5.0% (w/w)。可以单用也可几种胶凝剂一起合用,以使泡沫获得最佳特性,常见的胶凝剂有:
①天然聚合物:刺槐豆胶、海藻酸钠、黄原胶、黄蓍胶等。
②半合成聚合物:纤维素醚(如MC、HPC、HPMC等)、瓜尔胶衍生物等。
③合成聚合物:聚乙烯吡咯烷酮、聚乙烯醇聚丙烯酸共聚物、卡波姆等。
4.1.5 泡沫佐剂
泡沫佐剂是提高表面活性剂对乳状液稳定能力以及增加泡沫稳定性的一类辅料,主要是高级脂肪醇和脂肪酸。用量约占PFF的0.1%~5% (w/w),最好在0.4%~2.5% (w/w)之间。脂肪醇一般使用含15个以上碳原子的高级脂肪醇,例如鲸蜡醇(十六醇)和硬脂醇(十八醇)或其混合物、花生醇(二十烷醇)、山嵛醇(二十二醇)、1-三十烷醇等。脂肪酸一般使用含16个以上碳原子的高级脂肪酸,例如软脂酸(十六烷酸)、硬脂酸(十八烷酸)、花生酸(二十烷酸)、山嵛酸(二十二烷酸)、褐煤酸(二十八烷酸)等。脂肪醇和脂肪酸也可以是高级不饱和脂肪醇和高级不饱和脂肪酸,如油醇(十八烯醇)。
4.1.6 抛射剂
抛射剂是泡沫剂的喷射动力来源,可兼做药物的溶剂或稀释剂。抛射剂多为液化气体,在常压沸点低于室温,蒸汽压高。当阀门开放时,压力突然降低,抛射剂急剧汽化,借抛射剂的压力将容器内的药液以泡沫状喷出。抛射剂用量为5%~25%(w/w)。药用泡沫剂的抛射剂通常不用压缩空气,如氮气、二氧化碳等。国外上市的药用泡沫剂产品中的抛射剂最常使用的是碳氢化合物类抛射剂,如丙烷、丁烷、异丁烷或它们的混合物。该类抛射剂可以减少容器罐中残余的氧气与活性成分反应的可能性,且用其产生的泡沫质感好,但是存在易燃易爆风险,使用时需注意远离火源。国内尚未有经过批准的药用级碳氢化合物类抛射剂,可使用氢氟烷烃 (HFA)类抛射剂,如四氟乙烷(HFA-134a)代替原研产品中碳氢化合物类抛射剂。
4.2 乳剂型泡沫剂制备工艺及实例分析
根据Tamarkin等人公开的专利信息,乳剂型泡沫剂的制备工艺一般步骤如下:
a.水相混合物制备:将胶凝剂和表面活性剂在搅拌下溶解在水中;将该溶液加热至50-70℃;在搅拌下将水溶性药物及其它水溶性成分加入到水相混合物中。
b.油相混合物制备:将疏水性溶剂加热至相同温度;将泡沫佐剂添加到预热的疏水溶剂中;在搅拌下将油溶性药物及其它油溶性成分加入到油相混合物中。
c.混合:在搅拌下将热的油相逐渐倒入热的水相中,然后用均质器乳化;使混合物冷却至室温;对于热敏性药物,在冷却至室温后,在搅拌下将其加入混合物中。
d.灌装:将得到的预发泡混合物灌装至容器罐中,安装阀门,轧盖,压入抛射剂。
实例一:硝酸益康唑乳剂型泡沫剂
Quinnova制药公司研发了1%硝酸益康唑乳剂型泡沫剂ECOZA®,于2013年10月被FDA批准上市,用于治疗12岁及以上患者由红色毛癣菌,须癣毛癣菌和絮状表皮癣菌引起的趾间足癣。该泡沫剂中的有效成分为硝酸益康唑(econazole nitrate),分子式为C18H15Cl3N2O·HNO3,分子量为444.70。本品内容物为o/w乳液,储存在铝制加压容器中,揿压阀门,药液呈白色至类白色泡沫喷出。规格为70g/罐,每克ECOZA®泡沫剂含10mg硝酸益康唑。
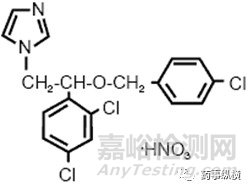
图4 硝酸益康唑
ECOZA®泡沫剂处方组成如下表所示:
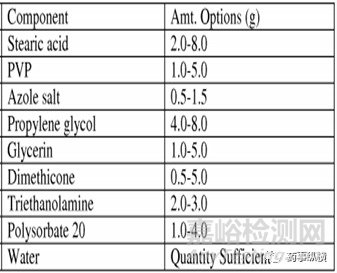
该处方中,泡沫佐剂为硬脂酸,胶凝剂为聚乙烯吡咯烷酮,保湿剂为丙二醇、甘油,润肤剂为二甲硅油,表面活性剂为吐温20,PH调节剂为三乙醇胺。所用的抛射剂为丁烷。
实例二:壬二酸乳剂型泡沫剂
拜耳公司(Bayer HealthCare)联合以色列生物科技公司 Foamix研制的15%壬二酸乳剂型泡沫剂FINACEA®于2015年8月获得了美国FDA的批准,用于局部治疗中度至中度酒渣鼻的炎性丘疹和脓疱。该泡沫剂中的有效成分为壬二酸(Azelaic Acid)分子式为C9H16O4,分子量为188.2。本品内容物为o/w乳液,储存在铝制加压容器中,揿压阀门,药液呈白色至类白色泡沫喷出。规格为50g/罐,每克FINACEA®泡沫剂含0.15g壬二酸。
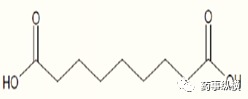
图5 壬二酸
FINACEA®泡沫剂处方组成如下表所示:
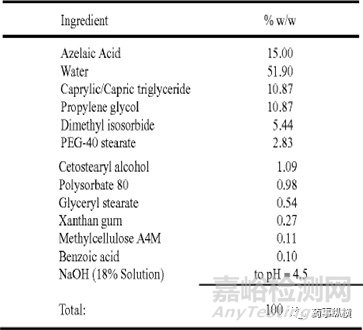
该处方中,辛酸/癸酸甘油三酯为疏水性溶剂,丙二醇、异山梨醇二甲基醚为促渗剂,聚氧乙烯(40)单硬脂酸酯、吐温80、硬脂酸甘油酯为表面活性剂,鲸蜡硬脂醇为泡沫佐剂,黄原胶、甲基纤维素A4M为胶凝剂,苯甲酸为防腐剂,氢氧化钠为PH调节剂。所用的抛射剂为丙烷+丁烷+异丁烷混合气体。

来源:药事纵横


