您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-08-10 22:02
摘要
目的:比较吸入气雾剂递送剂量均一性考察中不同抽样方案的差异。
方法:汇总2020年版《中国药典(四部)》(简称ChP)、《European Pharmacopoeia11.0(VolumeⅠ)》(简称EP)/《British Pharmacopoeia2023(VolumeⅢ)》(简称BP)、《USP-NF online2024》(简称USP)及我国进口药品注册标准(简称JX)中吸入气雾剂递送剂量均一性考察的抽样方案和判定标准。以硫酸沙丁胺醇吸入气雾剂为例,按ChP及USP抽样方案分别测定4家企业(企业A,B,C,D)6批样品的递送剂量均一性。采用蒙特卡洛模拟法进行数据模拟,并绘制工作特性曲线。
结果:按ChP抽样方案,样品的递送剂量均一性均符合规定;按USP抽样方案,仅企业C有1批样品的平均递送剂量不符合规定(低于70µg),且与企业D样品比较差异显著(P<0.05)。ChP的工作特性曲线较其他3种判定标准更宽,接受区域更广;EP/BP与JX抽样方案第一阶段接受概率和总接受概率均较接近;USP与JX抽样方案在标准差较小(≤6)时几乎相同,随着标准差的增大,前者的第一阶段接受概率和总接受概率下降程度更显著,在标准差≥10的情况下,其总接受概率<90%。
结论:不同抽样方案对吸入气雾剂递送剂量均一性的接受概率存在一定差异,USP较ChP,EP/BP,JX对变异较大的产品容忍度更低。
关键词
吸入气雾剂;药典;递送剂量均一性;抽样方案;工作特性曲线;蒙特卡洛模拟法
吸入气雾剂是指原料药或原料药和附加剂与适宜抛射剂共同封装于具有定量阀门系统和一定压力的耐压容器中,形成溶液、混悬液或乳液,使用时借助抛射剂的压力,将内容物呈雾状物喷出而用于肺部吸入的制剂[1]。大多为多剂量贮库型定量阀门气雾剂,为“药械合一”的复杂制剂,每次仅释放1个剂量。递送剂量是指1个单位剂量的药物从吸入制剂的口含器中释放出的药物量,是评估患者可能吸入药物剂量的重要指标。递送剂量均一性反映同一批次产品罐内、罐间递送剂量的差异,通过检测多个揿次点的释药剂量,以确认吸入制剂在整个使用过程中不同给药揿次间的递送剂量是否具有均一性。通过递送剂量及递送剂量均一性检查,可保证制剂在使用过程中递送药物剂量的准确性,从而避免单次给药剂量过高或过低引起安全性或有效性问题。2020年版《中国药典(四部)》(简称ChP)通则0111吸入制剂[1]、《European Pharmacopoeia11.0(Vol-umeⅠ)》[2](简称EP)及《British Pharmacopoeia2023(VolumeⅢ)》[3](简称BP)》均要求控制罐内及罐间递送剂量的均一性,《USP-NF online2024》[4](简称USP)吸入气雾剂项下要求控制递送剂量的均一性。目前,对于递送剂量均一性的抽样原则和判定标准,均采用两阶段计数型判定法(其中EP和BP的抽样方案和判定标准均相同)。ChP和EP/BP通常为10-30法;USP在不同的各论项下曾见20-60法[5],在我国进口药品注册标准(简称JX)中偶见20-40法[6-8]。上述方法规定的限度不同,造成判定标准不统一,给检验及审评工作带来了困惑和挑战。鉴于此,本研究中以硫酸沙丁胺醇吸入气雾剂为例,采用ChP通则0111项下单位剂量取样装置(DUSA),按ChP(EP及BP抽样方案与之类似)及USP抽样方案(JX抽样方案与之类似)分别测定不同企业硫酸沙丁胺醇吸入气雾剂的递送剂量均一性;汇总了ChP,EP/BP,USP,JX中吸入气雾剂递送剂量均一性的抽样方案和判定标准;采用蒙特卡洛数据模拟方法[9-10]进行数据模拟,并绘制工作特性曲线,以期为吸入气雾剂质量标准的制订、药品复核检验及药物评审提供参考。现报道如下。
1递送剂量均一性测定
1.1 仪器与试药
仪器:Ultimate3000型高效液相色谱仪(美国Thermo Fisher Scientific公司,配有四元泵、在线脱气机、自动进样器、紫外检测器和Chromeleon7色谱工作站);XS205DU型电子天平(精度为0.01mg),SevenEasy型pH计,均购自瑞士Mettler Toledo公司。
试药:硫酸沙丁胺醇对照品(中国食品药品检定研究院,批号为100328-201804,含量99.4%);硫酸沙丁胺醇吸入气雾剂[企业A,B,C各1批,企业D(原研)3批,编号分别为a,b,c,d1,d2,d3];甲醇为色谱纯,磷酸二氢钠、磷酸为分析纯,水为纯化水(实验室自制)。
1.2 方法与结果
1.2.1 色谱条件
色谱柱:Hypersil BDS C18柱(200mm×4.6mm,5µm);流动相:0.08mol/L磷酸二氢钠溶液(用磷酸调pH至3.10±0.05)-甲醇(85∶15,V/V);流速:1.0mL/min;检测波长:276nm;柱温:25℃;进样量:100µL。
1.2.2 溶液制备
对照品溶液:取硫酸沙丁胺醇对照品适量,精密称定,加流动相溶解并稀释成质量浓度为1µg/mL的溶液,即得。
供试品溶液:1)ChP方案。(1)罐内供试品溶液。取样品1罐,充分振摇,弃去3揿,收集1揿,用流动相清洗回收橡胶接头、滤纸及DUSA内部,合并洗液,置100mL容量瓶中,用流动相定容,摇匀,过滤,即得第1揿的供试品溶液。按上述步骤同法制备第2,3揿的供试品溶液。弃去94揿(第4~97揿),取下药罐,用甲醇冲洗阀门及驱动器,充分干燥,弃去2揿(第98,99揿),同法制备第100~103揿的供试品溶液。再弃去92揿(第104~195揿),取下药罐,用甲醇冲洗阀门及驱动器,充分干燥,弃去2揿(第196~197揿),同法制成第198,199,200揿的供试品溶液。(2)罐间供试品溶液。取同一批样品10罐,按“罐内”供试品溶液制备方法操作,按表1(其中USP与JX抽样方案同时适用于罐内与罐间)方法取样。2)USP方案。取同一批样品10罐,充分振摇,按表1方法操作,弃去3揿,每罐均制备首揿和末(第200)揿的供试品溶液(共20个)。

1.2.3 方法学考察
系统适用性试验:精密吸取1.2.2项下对照品溶液和供试品溶液各适量,按1.2.1项下色谱条件进样测定,记录色谱图。结果供试品溶液色谱中,在与对照品溶液色谱相应位置有吸收峰。理论板数按硫酸沙丁胺醇峰计不低于3000,分离度大于1.5,基线分离良好。详见图1。
线性关系考察:取硫酸沙丁胺醇对照品适量,加入流动相溶解,稀释成质量浓度分别为0.2,0.5,1.0,2.0,5.0,10.0µg/mL的系列对照品溶液。取适量,按1.2.1项下色谱条件进样测定,记录峰面积。以待测成分质量浓度(X,µg/mL)为横坐标、峰面积(Y)为纵坐标进行线性回归,得回归方程Y=0.7584X+0.0256(r=1.0000,n=6)。结果硫酸沙丁胺醇质量浓度在0.212~10.6µg/mL范围内与峰面积线性关系良好。
检测限与定量限考察:取1.2.2项下对照品溶液适量,逐级稀释,按1.2.1项下色谱条件进样测定,以信噪比(S/N)为3和10时待测成分的质量浓度分别为检测限和定量限。结果硫酸沙丁胺醇的检测限、定量限分别为0.01,0.03µg/mL。
精密度试验:取1.2.2项下对照品溶液适量,按1.2.1项下色谱条件进样测定6次,记录峰面积。结果硫酸沙丁胺醇峰面积的RSD小于2%(n=6),表明仪器精密度良好。
稳定性试验:取样品(d1)适量,按1.2.2项下方法制备供试品溶液,分别于室温下放置0,2,4,8,24,48h时按1.2.1项下色谱条件进样测定。结果硫酸沙丁胺醇峰面积的RSD小于2%(n=6),表明供试品溶液在室温下放置48h内基本稳定。
1.2.4 递送剂量测定
取样品各适量,按1.2.2项下方法制备供试品溶液,按1.2.1项下方法进样测定。结果显示,根据表1判定标准,按ChP抽样方案6批样品的递送剂量均一性均符合规定;按USP抽样方案仅样品c的平均递送剂量不符合规定(低于70µg[13]),且与企业D样品比较差异显著(P<0.05)。详见图2。
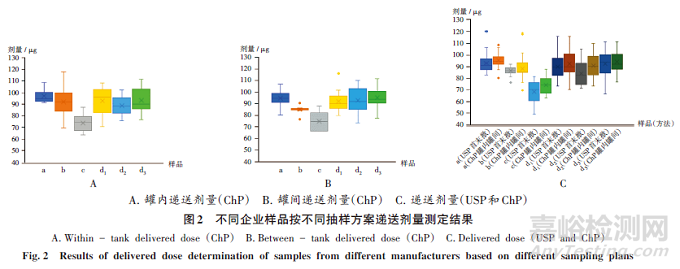
2递送剂量均一性判定标准数据模拟
EP/BP和ChP第一阶段通常规定样本量为10揿,USP和JX均为20揿;第一阶段通常规定平均值在标示量的一定范围内,且结果超出平均值一定范围的数量不得超过规定数目,否则进入第二阶段。EP/BP和ChP第二阶段通常规定样本量为20揿,USP为40揿,JX为20揿;第二阶段通常根据2个阶段的结果共同判定,平均值在标示量的一定范围内,且结果超出平均值一定范围的数量不得超过规定数目,否则判为不符合规定。
参考文献[14-19],采用R语言4.0.0版、通过程序编写,模拟了真实批次标示递送剂量为100.0%,真实生产平均值的75.0%~125.0%,标准差(σ)为1~12的正态分布数据。分别采用表1中4种判定标准,估算第一阶段的接受概率及总接受概率,生成工作特性曲线。步骤:采用计算机从具有规定平均值和标准差的正态分布中随机生成10000次10或20个第一阶段数据集;计算通过第一阶段判定标准数据的比例,估算第一阶段的接受概率。对于未通过第一阶段测试的数据集,从同一正态分布数据中随机生成20或40个第二阶段数据。合并通过第一阶段和第二阶段的数据集,分别采用上述4种判定标准,计算通过第二阶段数据集的比例来估算第二阶段的接受概率。总接受概率=第一阶段接受概率+第二阶段接受概率。2个阶段的工作特性曲线详见图3[其中,黑色、红色、紫色、蓝色线分别为ChP,EP/BP,JX,USP曲线;横坐标均代表递送剂量占平均递送剂量的百分比]。
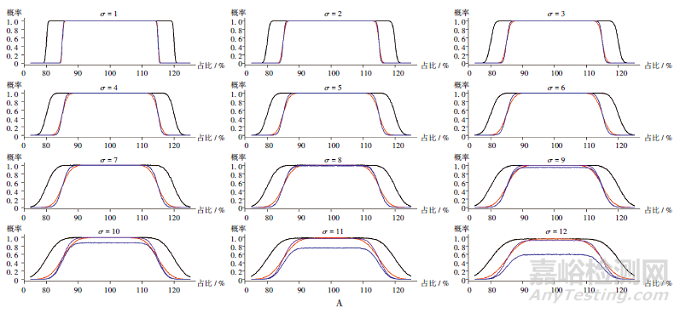

由图3可知,对于具有较小变异性的批次(σ较小),若未能通过第一阶段,该批次通过第二阶段的概率仅有微小的增加;当批次的变异性增大时,第一阶段接受概率与总接受概率的差异随着σ的增大而更显著。ChP的工作特性曲线较其他3种判定标准更宽,接受区域更广,故总体平均值的要求(平均值应为递送剂量标示量的80%~120%)较其他3种判定标准(平均值应为递送剂量标示量的85%~115%)较低;ChP与EP/BP的判定标准第一阶段接受概率与总接受概率的差异较JX和USP略大,即如果某批样品未能通过第一阶段而进入第二阶段的测试,则30个样本量总体的通过概率比第一阶段的通过概率增加的程度而言,ChP和EP/BP比JX和USP增加的程度略大。
总体而言,EP/BP与JX第一阶段接受概率和总接受概率均较接近。USP与JX在σ较小(≤6)时几乎相同;随着σ的增大,前者第一阶段接受概率和总接受概率的下降程度更显著;在σ≥10的情况下,其总接受概率<90%,提示该方法对变异较大的产品容忍度较其他3种标准更低。
3讨论
ChP通则0111吸入制剂中规定应评价吸入剂罐内和罐间的递送剂量均一性,采取10-30法抽样判定;USP采用20-60法,同时考虑了罐内和罐间的递送剂量均一性。工作特性曲线显示USP(20-60法)对变异较大的产品容忍度较其他3种标准更低。混悬型吸入气雾剂较复杂,递送剂量变异性较大,末揿的覆盖样本更多,有利于递送剂量均一性考察。故对于混悬型吸入气雾剂,建议按USP(20-60法)抽样方案及判定标准,以保证用药剂量的准确性。

来源:Internet


