今日头条
徐诺中美双报抗癌药获批IND。徐诺药业新一代广谱RAF抑制剂XP-102获国家药监局批准开展Ⅰ期临床,拟评估用于治疗BRAF V600突变阳性的晚期实体瘤患者的安全性、耐受性、药代动力学和初步疗效,预计今年完成患者入组。多项临床前研究显示,XP-102可能恢复耐药肿瘤的药物敏感性,有望为肿瘤耐药患者提供新的治疗方案。目前,XP-102正在美国开展Ⅰ/Ⅱa期临床试验。
国内药讯
1.成都倍特司美格鲁肽启动Ⅲ期临床。倍特药业3.3类新药司美格鲁肽注射液在Clinicaltrials.gov网站上注册一项Ⅲ期临床,拟评估与诺和诺德司美格鲁肽注射液Ozempic头对头比较,治疗2型糖尿病的有效性和安全性。今年3月,该产品获NMPA批准新IND,适应症为“作为低卡路里饮食和增加体力活动的辅助治疗用于肥胖或超重并且伴有至少一种与超重相关的合并症的成人患者”。
2.上海正序地贫基因编辑疗法获批IND。正序生物碱基编辑药物“CS-101注射液”获国家药监局临床许可,拟用于重型β-地中海贫血的治疗。在研究者发起的临床试验(IIT)中,CS-101已成功治愈首例重型β-地中海贫血症患者,达到持续摆脱输血依赖超过两个月,治疗后8周,患者的胎儿血红蛋白浓度上升至95 g/L,比例上升至81%,表达胎儿血红蛋白的F细胞比例上升至80%。
3.辉瑞2款自免三抗中国报IND。辉瑞炎症与免疫学领域1类生物药PF-07264660注射液和PF-07275315注射液的临床试验申请获NMPA受理。研究发现,IL-13和IL-4是诱导和维持2型炎症反应的关键细胞因子,与多种特应性疾病如特异性皮炎(AD)、哮喘和慢性鼻窦炎伴鼻息肉病(CSwNP)等有关。PF-07275315是一款IL-4/IL-13/TSLP三抗,PD-07264660是IL-4/IL-13/IL-33三抗,两款新药目前正分别在Ⅱ期临床中评估用于治疗特应性皮炎的潜力。
4.恒赛中美双报肿瘤疫苗获批IND。恒赛生物首发管线KSD-101获FDA批准开展新药临床试验。KSD-101是负载EB病毒相关类肿瘤复合抗原的人单核细胞来源自体树突细胞疫苗,通过皮下注射后能在人体内激活EBV特异CTL,从而实现对肿瘤细胞的有效识别及杀伤,具有良好的有效性及安全性。目前恒赛生物正在国内推动KSD-101的注册申报并筹备生产基地的建设。
5.康哲引进一款白癜风新药。康哲药业宣布,旗下公司康哲美丽与Incyte公司就后者临床后期口服小分子JAK1抑制剂povorcitinib订立合作许可协议,应用于非节段型白癜风、化脓性汗腺炎(HS)、结节性痒疹(PN)、哮喘和慢性自发性荨麻疹等治疗。根据协议,康哲药业将拥有在中国大陆、香港、澳门、台湾及东南亚十一国开发及商业化的独家权利,以及在区域内生产产品的非独家许可权利。
国际药讯
1.AZ/第一三共ADC在美报sBLA。阿斯利康与第一三共开发的靶向TROP2的ADC药物Dato-DXd(Datopotamab deruxtecan)的生物制品许可申请(sBLA)获 FDA受理,用于治疗既往在不可切除或转移性疾病阶段接受过系统治疗的HR+、HER2-(IHC 0、IHC 1+ 或 IHC 2+/ISH-)的乳腺癌,PDUFA日期为明年1月。在 III期临床TROPION-Breast 01研究中,与化疗相比,Dato-DXd可将疾病进展或死亡风险显著降低37%。
2.肿瘤疫苗结直肠癌临床积极。Gritstone bio公司个体化癌症疫苗GRANITE联合免疫检查点抑制剂及氟嘧啶/贝伐珠单抗一线维持治疗转移性微卫星稳定性结直肠癌患者的Ⅱ/Ⅲ期临床结果积极。与氟嘧啶/贝伐珠单抗相比,GRANITE组合显著改善了患者无进展生存期PFS(HR=0.82,95% CI:0.34-1.67),延长高危患者的PFS(HR=0.52,95% CI:0.15-1.38);且药物总体耐受性良好。此前,该疫苗已获得FDA快速通道资格。
3.Vistagen公司FIC社恐新药启动Ⅲ期临床。Vistagen公司潜在“first-in-class"鼻喷雾剂fasedienol(PH94B)启动评估急性治疗社交焦虑症(SAD)的Ⅲ期临床PALISADE-3试验。Fasedienol可调节与恐惧和焦虑密切相关的嗅觉-杏仁核神经回路,减弱交感神经自主神经系统的张力。在PALISADE-2试验中,PH94B治疗显著改善了患者的主观焦虑量表评分(-13.8分vs-8.0分),并显著提高了患者的临床应答率(40.6%vs18.6%)。蔼睦医疗拥有该产品在中国、韩国和东南亚地区的开发和商业化权益。
4.FIC肾病抑制剂Ⅱ/Ⅲ期临床积极。Vertex公司潜在“first-in-class”小分子APOL1抑制剂inaxaplin(VX-147)治疗APOL1介导肾病(AMKD)患者的Ⅱ/Ⅲ期临床结果积极。独立的数据监查委员会(IDMC)已评估该项研究Ⅱ期部分的安全性及有效性数据,建议在Ⅲ期阶段部分选择inaxaplin(每日一次45mg)单一剂量;还建议扩展患者招募范围,纳入10至17岁的AMKD青少年患者。此前,该新药已获得FDA授予突破性疗法认定。
5.Equillium公司CD6单抗早期临床积极。Equillium公司CD6单抗itolizumab治疗狼疮性肾炎患者的Ⅰb期临床EQUALIZE结果积极。Itolizumab可选择性靶向CD6-ALCAM信号通路,选择性抑制致病性效应T细胞,同时保留对维持平衡免疫反应至关重要的调节T细胞。第36周时,itolizumab治疗患者尿蛋白肌酐比值(UPCR)较基线降低73%;有37.5%患者达到完全缓解(UPCR≤0.7g/g),有43.8%患者达到部分缓解(UPCR≥50%);且药物耐受性良好。
6.Context公司实体瘤双抗报IND。Context公司CLDN6/CD3双抗CTIM-76向FDA提交了首次人体IND申请,计划开展Ⅰ期剂量递增和扩展研究,评估用于治疗Claudin 6(CLDN6)阳性妇科和睾丸癌患者的安全性、耐受性与初步疗效。CTIM-76结合了高选择性的CLDN6结合臂和CD3结合单链Fv结构域,其Fc被设计为功能性单价,以避免异常T细胞激活并提高安全性。CLDN6是许多实体瘤类型的有效治疗靶点,包括卵巢、子宫内膜、睾丸和胃。
医药热点
1.深圳首个国际联合临床研究所落户中山七院。近日,“伯明翰大学-中山七院联合临床研究所揭牌仪式暨临床研究国际合作论坛”在中山大学附属第七医院举办,中山七院与英国伯明翰大学联合建设的临床研究所正式宣布成立。这是深圳市成立的第一个国际联合临床研究所。中山七院是中山大学设置在深圳市的首家直属附属医院。医院规划总床位4000张。
2.药明生物调整高管职位。药明生物宣布,自2024年3月31日起,周伟昌已退任公司首席技术官以及全球生物制药开发及运营总裁等职务,并调任为公司非执行董事及全球生物制药开发及运营名誉总裁及首席执行官高级顾问以支援公司的发展。调任后,周伟昌将留任董事会战略委员会成员,为公司的决策提供支持。此前,据1月15日药明生物的公告,药明生物欧美CMC管理负责人Sherry Gu将接任周博士职责,担任药明生物CTO及执行副总裁、生物制药开发及生产部负责人。
3.印度CAR-T一针最低21.7万元。近日,《自然》杂志刊登一篇最新研究论文显示,印度生物技术公司ImmunoACT研发出一种经济实惠的CAR-T细胞疗法NexCAR19,其治疗费用仅为全球同类商业产品的十分之一,一次治疗费用只要3-4万美元(约合人民币21.7至28.9万元)。该疗法已于去年10月获得印度药品监管机构批准在印度用于治疗。
评审动态
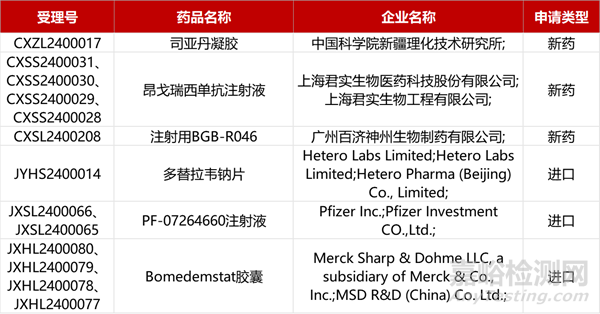
1. CDE新药受理情况(04月02日)
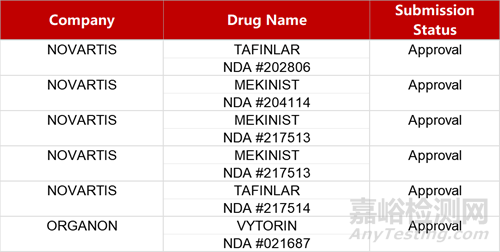
2. FDA新药获批情况(北美03月29日)