欧盟发布两份附录XVI产品指南文件
2023年12月14日,欧盟连续发布了两份有关附录XVI产品的指南,分别是MDCG 2023-5及MDCG 2023-6。这两份指南文件旨在帮助制造商更好地了解附录XVI无医疗预期用途产品分类及等同性证明相关内容。
MDCG 2023-5
无预期医疗用途产品的认定及分类
本指南文件提供了有助于将产品鉴定为MDR附录XVI中所列的无预期医疗用途产品的要素。它还提供了将某些分类规则应用于无预期医疗目的产品的解释和示例。
本指导文件应与MDCG 2021-24关于医疗器械分类的文件一起阅读。
无预期医疗用途产品的分类规则及示例具体如下:
第一组:隐形眼镜
此类别不包括包含工具(如天线或微芯片)的隐形眼镜、作为有源器械的隐形眼镜以及植入眼睛或进入眼睛的其他物品。
短期使用的彩色非矫正隐形眼镜或带有印记的非矫正隐形眼镜,它们是IIa类。如果长期使用,将被归类为IIb类。
第二组:通过侵入性手段植入体内以改变解剖结构的产品
CS适用于旨在通过外科侵入的方式全部或部分引入人体以改变解剖结构的产品。不包括纹身产品、穿孔和通过外科侵入进入人体以固定身体部位的产品。同样,该组的通用规范(CS)不适用于有源植入式器械。
所有植入式器械和长期使用的外科侵入性器械将被归类为IIb类,如皮下植入物、臀部植入物。
如果它们被全部或者大部分吸收,将被归类于III类,如用于隆胸的可吸收缝合线。
如果是乳房植入物或是外科疝补片,则被归类于III类,如乳房植入物,用于隆胸的疝补片。
第三组:用于面部或其他真皮或粘膜填充的产品
该类别包括通过皮下、粘膜下或皮内注射或其他引入进行面部或其他真皮或粘膜填充的物质、物质组合或物品,不包括纹身相关产品。
所有植入式器械和长期使用的外科侵入性器械归类为IIb类,如永久性真皮填充物。其中,可分解的真皮填充物被归类为III类。
第四组:旨在减少、去除或破坏脂肪组织的器械
该类别包括旨在减少、去除或破坏脂肪组织的器械,其中所有非侵入性器械及可重复使用的瞬时使用的外科侵入性器械都被归类为I类,一次性使用的外科侵入式器械被归类为IIa类。
此外,旨在减少、去除或破坏脂肪组织的器械被归类为IIb类,如吸脂器械。
第五组:治疗用高强度电磁辐射发射器械
该类别包括用于人体的高强度电磁辐射(例如红外、可见光和紫外线)发射器械。
其中,仅用于人体脱毛的高强度电磁辐射发射器械重新归类为IIa类,如向人体提供能量、与人体交换能量或提供将被人体吸收的能量的激光和 IPL 器械。
拟用于人体皮肤治疗的高强度电磁辐射发射器械归类为IIb类,包括用于皮肤表面重修、疤痕去除、纹身去除或用于治疗痣、血管瘤、毛细血管扩张和色素沉着的皮肤区域的激光或 IPL 器械。这些器械向人体提供能量、人体交换能量或以潜在危险的方式向人体提供被吸收的能量。
第六组:用于脑刺激的器械
该类别包括应用电流或磁场或电磁场以改变大脑中神经元活动的脑刺激器械,该类器械被归类为III类,如经颅磁刺激或经颅电刺激器械。
原文链接:https://health.ec.europa.eu/system/files/2023-12/mdcg_2023-5_en.pdf
MDCG 2023-6
无预期医疗用途器械等同性证明指南
在指南中,无预期医疗用途器械等同性证明存在三种情况,具体如下:
1、两种无预期医疗用途的器械
在参考等同器械的临床数据时,制造商应根据MDR中制定的标准证明两种无预期医疗用途的器械之间的等同性,其中重点考虑技术、生物学和临床特征等方面。
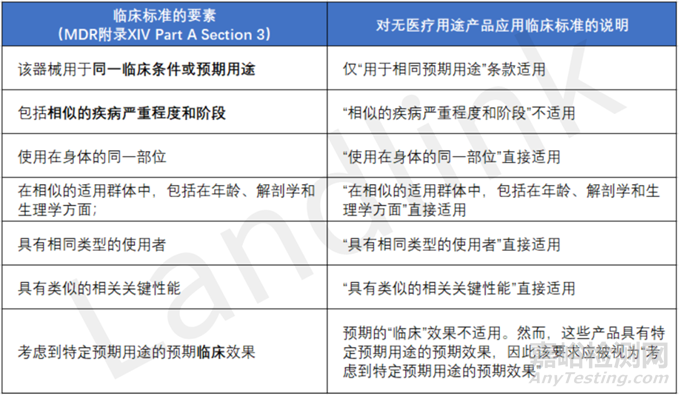
MDR中列出的技术和生物标准可以直接用于比较无预期医疗用途产品的特性,部分临床特征的标准是专门针对医疗用途的。下表阐明了无预期医疗用途产品应如何考虑其特性。
2、无预期医疗用途器械vs类似医疗器械
一般来说,医疗器械和无预期医疗用途的产品之间不可能进行比较,因为并非所有临床特征都能进行比较。特别是"疾病的严重程度和阶段相似 "这一特征对于医疗器械来说是可以定义和获得的,而对于无预期医疗用途的产品来说是无法定义和获得的。因此,无预期医疗用途的器械与有医疗用途的类似器械之间无法完成和建立等同性证明。
3、无预期医疗用途器械vs双用途医疗器械
对于同时具有医疗和无医疗用途的器械(双用途器械),只有无医疗用途相关的一般安全和性能要求的临床数据才能用于无预期医疗用途产品的临床评价。
原文链接:https://health.ec.europa.eu/system/files/2023-12/mdcg_2023-6_en.pdf