今日头条
诺未肝癌DNA核酸药物报IND。诺未科技自研1类生物制品"NWRD06裸质粒DNA注射液"临床试验申请获CDE受理,拟用于GPC3阳性肝细胞癌(HCC)根治术后患者的治疗。NWRD06是一款靶向肝癌特异性抗原GPC3的重组融合质粒DNA药物。临床前研究结果显示,NWRD06单药可显著降低原发性肝癌小鼠模型的肝脏肿瘤数量和肿瘤大小,联合PD-1单抗可进一步增强抗肿瘤药效,而且在动物模型中具有良好的耐受性。
国内药讯
1.安进RANKL单抗在华获批新适应症。安进RANKL靶向单抗普罗力(地舒单抗注射液)获国家药监局批准新适应症,用于治疗骨折高风险的男性骨质疏松症。此前,普罗力已获批用于治疗骨折高风险的绝经后妇女的骨质疏松症。在患有骨质疏松症男性中开展的全球Ⅲ期研究中,普罗力治疗较安慰剂显著提升患者关键部位的骨密度,患者24个月后腰椎与全髋骨密度与基线相比增加8.0%和3.4%,且安全性良好。
2.基石PD-L1单抗肺癌适应症在欧盟报产。基石药业PD-L1舒格利单抗的上市申请获欧洲药品管理局(EMA)受理,联合化疗一线治疗转移性非小细胞肺癌(NSCLC)。去年年底,英国药品监管机构也受理了舒格利单抗相同适应症的上市申请。在Ⅲ期GEMSTONE-302研究中,舒格利单抗联合化疗显著改善患者的无进展生存期和总生存期,研究数据已发表在《柳叶刀·肿瘤学》上。
3.诺华c-Met抑制剂在华报产。诺华5.1类新药卡马替尼(capmatinib,Tabrecta)的上市申请获CDE受理。Capmatinib是一种口服c-Met激酶抑制剂,是首个被FDA批准用于全线治疗METex14跳跃突变转移性非小细胞肺癌(NSCLC)的靶向药物。在Ⅱ期GeoMETry-C研究中,卡马替尼一线治疗经BIRC评估的客观缓解率(ORR)达到53.3%,研究者评估的ORR为60%,疾病控制率(DCR)为86.7%。;在METex14跳突伴脑转移患者中,capmatinib的颅内ORR达到50%,颅内DCR达100%。
4.迈威IL-11单抗获TGA临床批件。迈威生物自研IL-11单抗9MW3811获得澳大利亚治疗用品管理局 (TGA) 批准开展临床试验,拟开发用于多种晚期恶性肿瘤以及纤维化疾病。9MW3811是全球同靶点药物中首个开展临床试验的单抗药物,也是IL-11靶点第一款进入临床阶段的非重组蛋白药物。该新药日前已在ClinicalTrials.gov网站上登记启动首次人体I期临床(NCT05740475)。
5.科伦Nectin-4靶向ADC获批临床。科伦旗下科伦博泰开发的Nectin-4靶向ADC药物注射用SKB410获国家药监局临床许可,拟开发用于晚期实体瘤的治疗。Nectin-4(脊髓灰质炎病毒受体4)是一种I型膜蛋白,通过激活PI3K/AKT途径促进肿瘤细胞增殖、分化、迁移、侵袭等,在尿路上皮癌、膀胱癌、乳腺癌、卵巢癌、胃癌、肝细胞癌和胰腺癌等多种肿瘤细胞中高表达。目前,国内同靶点药物迈威开发的创新药9MW2821研发进展最快,已进入Ⅰ期开发阶段。
国际药讯
1.芦可替尼治疗白癜风获CHMP推荐上市。Incyte公司外用JAK抑制剂芦可替尼乳膏(Opzelura)获欧洲药品管理局(EMA)人用药品委员会(CHMP)推荐批准,用于治疗成人和12岁以上儿童患者非节段性白癜风。在两项Ⅲ期临床中,与安慰剂相比,ruxolitinib治疗组第24周时患者达到面部白癜风症状改善至少75%的比例显著更高(30%vs8%)。2022年7月,该乳膏获得FDA批准,成为首个进入美国市场的白癜风疗法。
2.CD45靶向放射疗法Ⅲ期临床成功。Actinium公司CD45靶向性放射疗法Iomab-B用于提高复发或难治性急性髓系白血病( AML)患者接受骨髓移植(BMT)治疗机会的关键Ⅲ期临床达到主要终点。数据显示,Iomab-B较对照组提高完成BMT的患者比例(100%vs18%);两组患者接受BMT治疗后达到缓解的比例分别为75%和6.3%;与对照组相比,Iomab-B组患者的1年生存率(26.1% vs 13.1%)和中位OS(6.4个月vs 3.2个月)均实现翻倍。Iomab-B总体耐受性良好。
3.礼来Aβ单抗启动一项IIIb期临床。礼来Aβ单抗donanemab在clinicaltrials.gov网站登记注册一项IIIb期临床试验(TRAILBLAZER-ALZ 6),拟评估不同给药方案对早期阿尔茨海默病(AD)成人淀粉样蛋白相关影像学异常-水肿/积液(ARIA-E)频率和严重程度的影响。今年1月,FDA以接受过12个月donanemab持续治疗的患者数据不足(应至少提供100例)为由,拒绝批准该药用于治疗早期症状性AD(包括AD所致的轻度认知障碍以及轻度AD)的加速上市的申请。
4.创新细胞疗法血癌早期临床积极。Orca Bio公司同种异体细胞疗法Orca-T用于治疗急性髓系白血病(AML)、急性淋巴细胞白血病(ALL)、骨髓增生异常综合征(MDS)和其他血液系统恶性肿瘤患者的Ⅰb/Ⅱ期临床12个月治疗数据积极。Orca-T联合BFT(白消安、氟达拉滨和塞替派)方案的患者无复发生存率达到87%,无移植物抗宿主疾病并且无复发的生存率(GRFS)为81%,试验中患者的总生存率达到94%。此前,FDA已授予Orca-T孤儿药资格,用于增强造血干细胞移植手术的细胞定植。
5.欧盟CHMP不推荐默沙东新冠口服药上市。欧洲药品管理局人用药品委员会(CHMP)不建议批准默沙东与Ridgeback公司联合开发的新冠口服药LAGEVRIO(Molnupiravi)上市。CHMP认为没有足够数据能证明Molnupiravir对未补充氧气且伴有进展为重症高风险因素的轻中度新冠患者有临床获益。Molnupiravir是一款口服核苷类似物,也是全球首个获批的口服抗新冠病毒疗法。
6.艾伯维达成约7亿美元眼科基因疗法合作。艾伯维宣布与Capsida公司扩大战略合作,将利用后者新型腺相关病毒(AAV)工程平台和制造能力结合,合作开发和商业化针对眼部疾病的3个基因药物。根据协议,Capsida公司将获得7000万美元的前期付款和股权投资,可能高达5.95亿美元的期权费和研发里程碑付款,以及商业里程碑付款。艾伯维将负责治疗药物的开发和商业化。
医药热点
1.广东补助百名返聘专家每人每年20万。近日,广东省卫健委印发《广东省百名卫生首席专家下基层计划实施方案(2023—2025年)》指出,选聘100名具有二级以上公立医院执业经历、高级职称且符合相关条件的退休医生担任首席专家,下沉到广东省47家中心卫生院全职工作3年,建设1个特色专科,开展1项以上新业务、新技术,“传、帮、带”打造1个专科团队。《方案》明确,在人事关系、现享受的退休待遇不变的情况下,由广东省财政给予每人每年20万元补助。
2.上海首个人类遗传资源管理咨询门诊开设。复旦大学附属中山医院宣布,该院已开设上海首个“人类遗传资源管理咨询门诊”,主要面向研究者,针对人类遗传资源管理的申报、备案过程中的问题进行解答。每周一次的人类遗传资源管理咨询门诊,可更好地服务临床,满足申请人的个性化需求。中山医院同时也开通了“中山医院人类遗传资源管理”微信公众号,随时接受申请咨询。这两项举措均为上海医疗机构的首次探索实践。
3.辉瑞拟收购Seagen。2023年2月27日早间,《华尔街日报》发文称:“辉瑞拟收购Seagen,收购价可能超过300亿美元”。据知情人士透露,辉瑞欲收购Seagen,目前正处在早期谈判阶段。该谈判可能受反垄断法案等多重因素影响,暂不可知最终结果。去年6月,曾有消息透露,默沙东欲以400亿美元的价格收购Seagen,或因收购价格未达成一致,谈判破裂。
评审动态
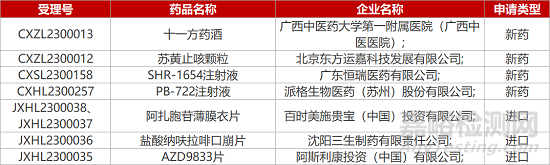
1. CDE新药受理情况(02月27日)
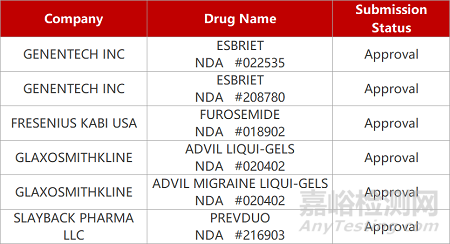
2. FDA新药获批情况(北美02月23日)