您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-06-24 15:31
去年Tendyne获得CE批准,成为全球首款获批上市的二尖瓣置换(TMVR)产品。Tendyne主要适用于那些不适合接受心脏直视手术的高危患者,或者当二尖瓣损伤过大,无法用MitraClip等技术进行二尖瓣修复(TMVr)的患者,Tendyne为以上患者提供了一种急需的、替代性的微创治疗方案来更换损伤的瓣膜。
Tendyne在二尖瓣置换(TMVR)领域是具有跨时代产品,Tendyne开启真正意义上市TMVR时代。今天Tendyne又取得新的进展,获得FDA授予“突破性设备”称号,并预期雅培开展关于Tendyne临床研究,研究对象限制于严重二尖瓣环钙化(MAC)患者。这将为Tendyne在美国上市提供快捷路径。
Tendyne
Tendyne来自于雅培在2015年一次收购,为此雅培花费了2.5亿美金。通过对Tendyne,与雅培已上市的MitraClip形成一个完整的经导管二尖瓣解决方案。
Tendyne是心尖拉绳锚定方式的二尖瓣瓣膜典型代表,其是经心尖方式植入到患者体内。
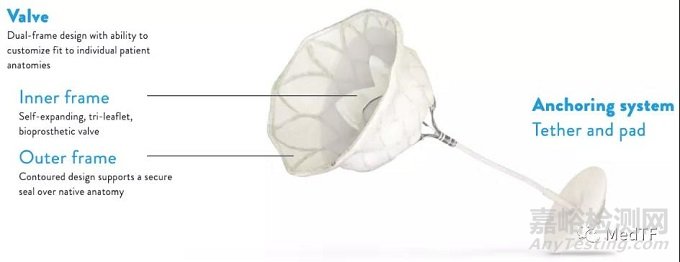
Tendyne由镍钛合金双层D型支架,三叶牛心包瓣膜,可调节拉绳与Pad(心尖固定器)以及密封垫组成。Tendyne 外支架根据二尖瓣瓣环解剖设计成类D型,内支架为圆形,保证有效瓣口的面积始终大于3.2平方厘米。外支架心房侧法兰外翻,用于防止瓣周漏、锚定(在舒张期瓣膜不会向心室移位),拉绳与心尖固定器相连,保证瓣膜不会向心房移位,且心尖固定器有辅助穿刺口止血的效果。
根据雅培提供数据显示:Tendyne在治疗严重二尖瓣返流(3级以上)患者时,显示其优异临床效果:
大多数患者(99%)在30天时MR完全消除,大多数患者在1年和2年时MR持续消除
手术成功率96%
患者的症状和生活质量等临床指标显著改善
不过随着Tendyne样本量增大,其临床效果也在发生着变化,没有之前的惊世骇俗的临床效果。

来源:MedTF


