今日头条
无锡科金细胞疗法获PKD孤儿药资格。科金生物细胞治疗产品CG001获FDA授予孤儿药认定,拟用于治疗丙酮酸激酶缺乏症(PKD)。这是一种由PKLR基因的突变导致的罕见隐性遗传疾病,可导致患者出现慢性溶血性贫血,即红细胞加速破坏。CG001是一款体外基因编辑的细胞疗法,通过科金专利技术平台CPISPR/AAV技术,在体外进行造血干细胞编辑,替换变异的PKLR基因,以达到治愈疾病的目的。
国内药讯
1.信达PCSK-9单抗降脂Ⅲ期临床见刊。信达生物自研PCSK-9抗体托莱西单抗(IBI306)治疗杂合子型家族性高胆固醇血症(HeFH)的中国Ⅲ期研究(CREDIT-2)结果在线发表在期刊BMC Medicine上。与安慰剂组相比,托莱西单抗(150 mg Q2W和450 mg Q4W)均显著降低LDL-C水平,两组患者第12周时LDL-C水平较基线的百分比变化的组间差异为−57.4%和−61.9%,LDL-C水平降低50%以上的患者比例分别达到59.6%和75.0%;IBI306总体安全性良好。
2.迈威铁稳态调节单抗上I期临床。迈威生物铁稳态调节大分子新药9MW3011在中国开展的首次人体 (FIH)I期临床完成首例受试者给药。9MW3011是一款创新靶点单抗药物,特异性结合并上调肝细胞表达铁调素的水平,抑制铁的吸收和释放,以调节体内的铁稳态。该新药拟开发用于治疗β-地中海贫血铁过载和真性红细胞增多症。在美国,9MW3011也获批开展用于真性红细胞增多症患者的临床试验。
3.礼来心血管疾病新药在华获批临床。礼来脂蛋白(a)[Lp(a)]抑制剂1类化药LY3473329片获国家药监局临床试验默示许可,拟开发用于治疗动脉粥样硬化性心血管疾病伴Lp(a)升高的患者。高Lp(a)定义为血浆中Lp(a)水平>125 nmol/L(或约50 mg/dL),是心血管疾病的重要风险因素。根据ClinicalTrials官网,该产品正在Ⅱ期临床评估用于Lp(a)升高且心血管事件风险较高的成年患者的治疗潜力。
4.合源CD19靶向CAR-T在美获批临床。合源生物靶向CD19的CAR-T产品赫基仑赛注射液(CNCT19细胞注射液)获FDA临床许可,拟用于治疗成人复发或难治性B细胞型急性淋巴细胞白血病(r/r B-ALL)。公布于ASH2022年会上的临床数据显示,赫基仑赛注射液的总体缓解率(ORR)达到82.1%,且安全性良好。此前,该新药已获得FDA授予孤儿药资格。
5.百奥赛图抗体平台RenLite授权杨森。百奥赛图宣布与强生旗下杨森就其专有抗体药物RenLite®平台签订非独家授权协议。百奥赛图RenMice平台是基于SUPCE基因编辑技术开发的,包括RenMab、RenLite和RenNano全人源转基因小鼠平台,通过大片段原位替换人源抗体基因序列,保留小鼠Fc区域序列,保证全人抗体的产生和免疫系统发育正常。根据协议,杨森将利用RenLite®平台、针对不限数量药物靶点,开发、生产和商业化可用于任何用途的全人共轻链抗体和其他生物制品。
6.丽珠医药引进一款抑酸新药。丽珠医药宣布与Onconic公司就后者临床后期创新钾离子竞争性酸阻滞剂(P-CAB)zastaprazan签署独占许可授权协议,丽珠医药将获得zastaprazan的大中华区授权。zastaprazan具有起效快、抑酸效果持久等特点,正在韩国开展Ⅲ期临床评估用于治疗糜烂性食管炎的效果。根据协议,Onconic将获得1500万美元首付款,共计不超过1.1250亿美元开发和销售里程碑潜在付款,以及产品的销售提成。
国际药讯
1.FDA发布AMD基因治疗产品指南草案。近日,FDA 发布一份涉及湿性老年黄斑变性(wet AMD)药物开发的指南草案,对试验设计、纳入标准和疗效终点等方面给出指导意见。对于试验设计,FDA建议进行随机、平行组、双盲试验。出于安全性考虑,FDA建议至少有400例患者接受实验性治疗,并至少有300例患者接受为期9个月的随访;以及该试验应包括50岁以上的患者,并且至少应进行一项至少两年的安全性对照试验。
2.首款Rett综合征新药获FDA批准上市。Acadia公司开发的新型IGF-1氨基末端三肽类似物Daybue(trofinetide)获FDA批准上市,成为首款Rett综合征治疗药物,用于成人和2岁以上儿童患者。Trofinetide通过减少神经炎症和支持突触功能来治疗Rett综合征的核心症状。Rett综合征是一种罕见遗传性神经发育障碍,由一种叫做MECP2.3的基因的X染色体突变引起,通常发生在女童身上。
3.Qtorin雷帕霉素Ⅱ期试验积极。Palvella公司在研药品Qtorin雷帕霉素在治疗微囊性淋巴管畸形患者的Ⅱ期临床获积极结果。与基线相比,Qtorin雷帕霉素治疗显著改善患者包括病变高度、渗漏和出血等多项重要疾病负担,受试者达到“大幅度改善(Much Improved)”或“极大幅度改善(Very Much Improved)的比例为100%,药物的耐受性良好,无药物相关严重不良事件,在体循环中亦未观察到雷帕霉素。
4.Vertex糖尿病干细胞疗法获批临床。Vertex公司第二款同种异体干细胞的全分化胰岛细胞疗法VX-264获FDA批准开展Ⅰ/Ⅱ临床试验,拟用于1型糖尿病(T1D)的治疗。VX-264包装在Vertex开发的独有免疫保护医疗器械中,通过手术植入患者体内,在保护细胞不受免疫排斥的同时,释放细胞生成的胰岛素。此前,该公司同类产品VX-880用于治疗T1D的Ⅰ/Ⅱ期临床已获得概念验证积极结果。
5.新型同种异体细胞疗法上Ⅰ期临床。Creative Medical公司宣布与Syneos Health公司就其针对1型糖尿病的同种异体细胞疗法CELZ-201开展Ⅰ/Ⅱ临床试验达成合作协议。Syneos Health是一家全集成生物制药解决方案机构,已建立去中心化的临床试验中心网络,旨在推动“数字医疗技术解决方案”。CELZ-201可通用供体细胞的分泌因子来重新编程患者自身的免疫细胞。该新药已在今年2月获得FDA临床许可。
6.默沙东布局EBV纳米颗粒疫苗。OPKO Health旗下公司ModeX Therapeutics与默沙东就其靶向爱泼斯坦-巴尔病毒(EBV)的临床前纳米颗粒候选疫苗MDX-2201达成独家许可和合作协议。MDX-2201能够表达多达24个拷贝的重组抗原,以增强病毒关键组分的呈递;多靶点途径的设计旨在抑制B细胞和上皮细胞的感染。根据协议,OPKO将获得5000万美元的预付款,高达约8.7亿美元的开发和商业化里程碑后期付款。默沙东将负责产品的临床开发和商业化。
医药热点
1.马晓伟连任新一届国家卫健委主任。3月12日上午,十四届全国人大一次会议第五次全体会议表决通过:由马晓伟继续担任国家卫生健康委员会主任。马晓伟自2018年3月担任国家卫健委主任以来,致力于推进医疗卫生健康事业高速发展:积极落实分级诊疗;推进县医院能力提升“千县工程” ;并针对实现公立医院“三个转变、三个提高”、构建高质量发展的新体系、破除制约高质量发展的体制机制障碍等方面,提出一系列指示要求。
2.四川率先开展口腔牙冠竞价挂网。3月10日,四川省医保局发布《关于开展口腔牙冠竞价挂网工作的通知》。《通知》明确,由四川省医保局率先在全国组织开展口腔牙冠竞价挂网。本次竞价挂网产品为单牙种植使用的全瓷牙冠产品,材质主要成分为氧化锆,包含白锆、彩锆(含单色彩锆和分层彩锆)。四川省所有开展口腔种植牙服务的公立医疗机构均应参加。
3.柳叶刀:二甲双胍可预防新冠后遗症。明尼苏达大学的研究人员在《柳叶刀》预印本平台发表:Outpatient Treatment of COVID-19 and the Development of Long COVID Over 10 Months:A Multi-Center,Quadruple-Blind,Parallel Group Randomized Phase 3 Trial 的论文。这项大规模随机对照临床试验显示, 在新冠感染早期使用二甲双胍治疗,能够将长期新冠发生率降低42% ,如果在出现症状4天内使用二甲双胍,能够将长期新冠发生率降低63%。
评审动态
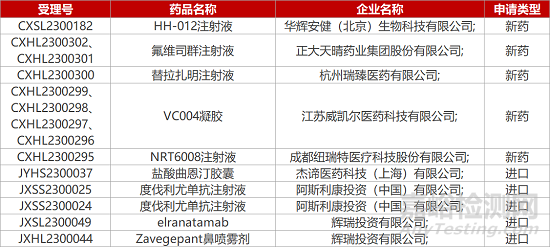
1. CDE新药受理情况(03月13日)
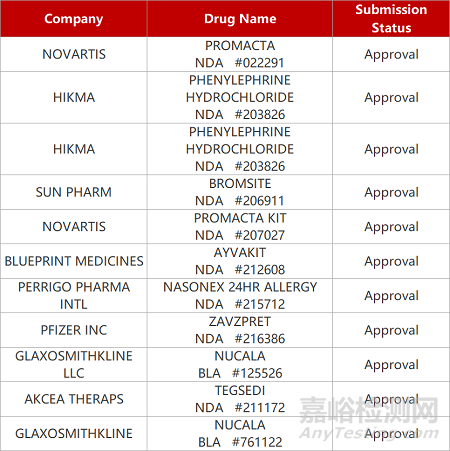
2. FDA新药获批情况(北美03月09日)