您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-07-21 09:53
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.百济神州PD-1新适应症拟优先审评。百济神州PD-1替雷利珠单抗针对MSI-H/dMMR实体瘤适应症的上市申请获CDE拟纳入优先审评。据悉,这是替雷利珠单抗申报上市的第7项适应症。在一项Ⅱ期临床(NCT03736889)中,中位随访时间为11.78个月时,IRC评估的ORR在所有肿瘤类型(单侧p<0.0001)中为45.9%(n=34/74;95% CI 34.3,57.9);疾病控制率为71.6%;替雷利珠单抗总体耐受性良好,未发现新的安全性信号。
2.北海康成新药CAN106获批临床。诺爱药业CAN106注射液获国家药监局临床试验默示许可,拟用于治疗阵发性睡眠性血红蛋白尿症(PNH)。CAN106是北海康成和药明生物及Privus Biologics建立战略合作关系后,共同开发进入临床阶段的一款补体C5抑制剂。除了PNH,CAN106还被开发用于治疗其他与补体失调相关的多种遗传性疾病。该新药去年12月在新加坡获批临床,目前正在进行I期安全性试验。
3.恒瑞两款1类新药获批临床。恒瑞旗下盛迪医药研发的注射用甲苯磺酸瑞马唑仑和注射用HRS3797获国家药监局临床试验默示许可。注射用甲苯磺酸瑞马唑仑是一种短效的GABA受体激动剂,该产品用于胃镜、结肠镜检查镇静的适应症已获批上市,用于支气管镜诊疗镇静、全身麻醉的适应症已完成临床试验并已进入申报生产阶段。HRS3797是一种超短效非去极化肌松药,拟用于全身麻醉诱导期气管插管及维持术中骨骼肌松弛,目前,国内外尚未有同类产品获批上市。
4.荣昌生物ADC新品种报IND。荣昌生物Claudin 18.2 ADC注射用RC118的临床试验申请获CDE受理。Claudin 18(CLDN18)是一种由CLDN 18基因编码的蛋白质,可以控制层细胞之间的分子流动。CLDN 18.2蛋白是一种CD20样分化蛋白,在胃癌等多种肿瘤组织中高度表达,而在正常组织中几乎没有表达。RC118是荣昌生物申报的第4款ADC,也是国内申报临床的第3款Claudin 18.2 ADC。
5.典晶生物引进珐博进眼科品种。典晶生物宣布与珐博进达成许可协议,获得珐博进拟用于治疗角膜致盲患者的生物合成角膜进行开发和商业化的全球独占许可权。这款生物合成角膜产品源自重组III型人胶原蛋白,目前正处于临床研发阶段。典晶生物成立于2020年,由礼来亚洲基金与张金忠博士、胡珍泽博士共同创办,致力于开发新型眼科产品。据悉,此项合作首付款和里程碑付款高达1.08亿美元。
国际药讯
1.新冠鸡尾酒疗法获批日本上市。日本厚生劳动省(MHLW)批准罗氏与再生元联合开发的抗体疗法Ronapreve(casirivimab和imdevimab)上市,用于通过静脉输注治疗轻中度COVID-19患者。在一项全球Ⅲ期临床REGN-COV 2067中,Ronapreve可使COVID-19高风险非住院患者的住院或死亡减少70%,症状持续时间缩短4天。在美国,Ronapreve已获FDA紧急使用授权,用于治疗病毒检测阳性、且进展为重度COVID-19风险较高的轻中度COVID-19患者。
2.A型血友病基因疗法在欧盟进入审查。欧洲药管局受理BioMarin制药基因疗法valoctocogene roxaparvovec(valrox,BMN270)用于治疗重度A型血友病成人患者的营销授权申请,CHMP的意见预计在2022年上半年公布。valrox是一种AAV基因疗法,旨在通过单次输注,向A型血友病患者体内递送凝血因子VIII功能基因,恢复VIII的产生,从而消除或减少静脉VIII输注需求。该疗法此前已获FDA授予的再生医学先进疗法认定和突破性疗法认定。
3.免疫检查点三联疗法上临床。Compugen抗PVRIG抗体COM701与百时美施贵宝PD-1抑制剂Opdivo(nivolumab)和抗TIGIT抗体BMS-986207构成的三联疗法,在晚期实体瘤患者中的Ⅰ/Ⅱ期剂量递增试验中完成首例患者给药。临床前实验结果显示,在对靶向PD-1免疫疗法耐药的患者中,癌细胞中较高的PVRL2水平可能是关键的生物标志物;而COM701与抗PD-1抗体联用能刺激T细胞产生协同作用,这类组合具有进一步增强针对肿瘤的免疫应答的潜力。
4.创新心肌肌球蛋白抑制剂Ⅱ期临床积极。Cytokinetics公司新型口服小分子心肌肌球蛋白抑制剂CK-274治疗梗阻性肥厚型心肌病(oHCM)的Ⅱ期临床REDWOOD-HCM获积极结果。与安慰剂相比,CK-274治疗组10周后患者的平均静息LVOT-G(左心室流出道压差),和使用咽鼓管充气检查法后的平均LVOT-G,均较基线显示出统计学意义的显著降低,CK-274组两队列达到治疗目标的患者比例分别为78.6%和92.9%,而安慰剂组仅为7.7%;临床中未出现因左心室射血分数(LVEF)降低而导致的治疗中断或中止。箕星药业拥有该新药大中华区研发权益。
5.FDA批准脊髓电刺激系统。Nevro公司开发的10 kHZ脊髓刺激(SCS)“Senza”系统获FDA批准上市,用于治疗疼痛性糖尿病神经病变(PDN)引起的慢性疼痛。这是FDA批准的首款以PDN为适应症的脊髓刺激系统。该公司计划近期将推出与PDN治疗相关的“HFX”的方案,包括Senza脊髓刺激系统,和治疗慢性疼痛的支持服务。目前获得的临床试验数据表明,相比传统医疗管理方案,HFX能够使PDN患者的疼痛平均缓解76%。
6.Frontier公司拟开发下一代KRAS抑制剂。致力于开发靶向“不可成药”靶点的精准疗法公司Frontier Medicines宣布完成8850万美元的B轮融资。此轮融资将用于推进该公司一款靶向KRAS G12C突变体的抑制剂。该新药能够同时抑制激活状态和失活状态的KRAS G12C突变体,具有双重抑制功能的药物可能比只靶向KRAS G12C突变体失活状态的药物具有更好的抗癌活性。
医药热点
1.“长期新冠”症状达200多种。《柳叶刀》子刊《EClinical Medicine》日前发表的一项最新研究显示,经历“长期新冠”的患者累计报告了200多种症状,涵盖人体10个器官系统。这10个器官系统分别为:全身性系统;神经精神病系统(子分类);心血管/循环系统;皮肤/外皮系统;皮肤相关的消化系统;肺部/呼吸系统;头、耳、眼、鼻、喉/头眼耳鼻喉系统;生殖/泌尿/内分泌系统;免疫系统;肌肉和骨骼系统。
2.暨南大学附属常德医院揭牌。7月16日下午,暨南大学附属常德医院正式揭牌成立,标志着常德市第一人民医院与暨南大学正式建立医疗协作关系。常德第一人民医院与暨南大学强强联合,共同致力于建设一流的区域医疗中心、一流的医疗人才培养基地,也开启了协同发展模式,铸就了服务百姓、造福一方的事业基础。
3.法国一医疗公司首次售出人工心脏。当地时间7月19日,法国医疗技术公司Carmat表示,自2008年该公司成立以来,第一次售出一颗人工心脏,用于植入1例等待移植的意大利患者。据悉,手术是由意大利那不勒斯Azienda Ospedaliera dei Colli医院的心外科医生Ciro Maiello领导的团队完成,该医院是意大利人工心脏领域最具经验的中心之一。
审评动向
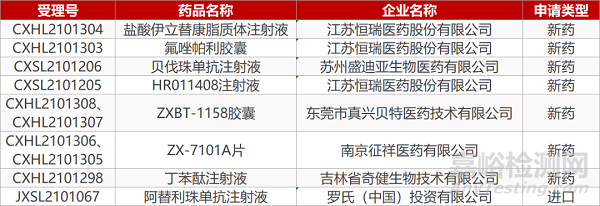


来源:药研发


