您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2021-03-16 07:56
为方便广大医疗器械生产企业的产品注册申报,本文整理了二、三类医疗器械的首次注册、延续注册、变更事项及创新审批的办理流程。供大家参考。
01、相关法规的要求
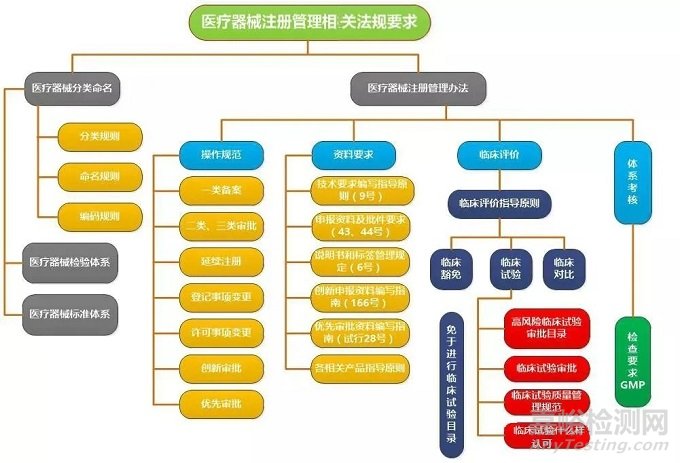
注:不同的产品依据相关的标准、指导原则、法规要求进行。
02、二类医疗器械的注册流程
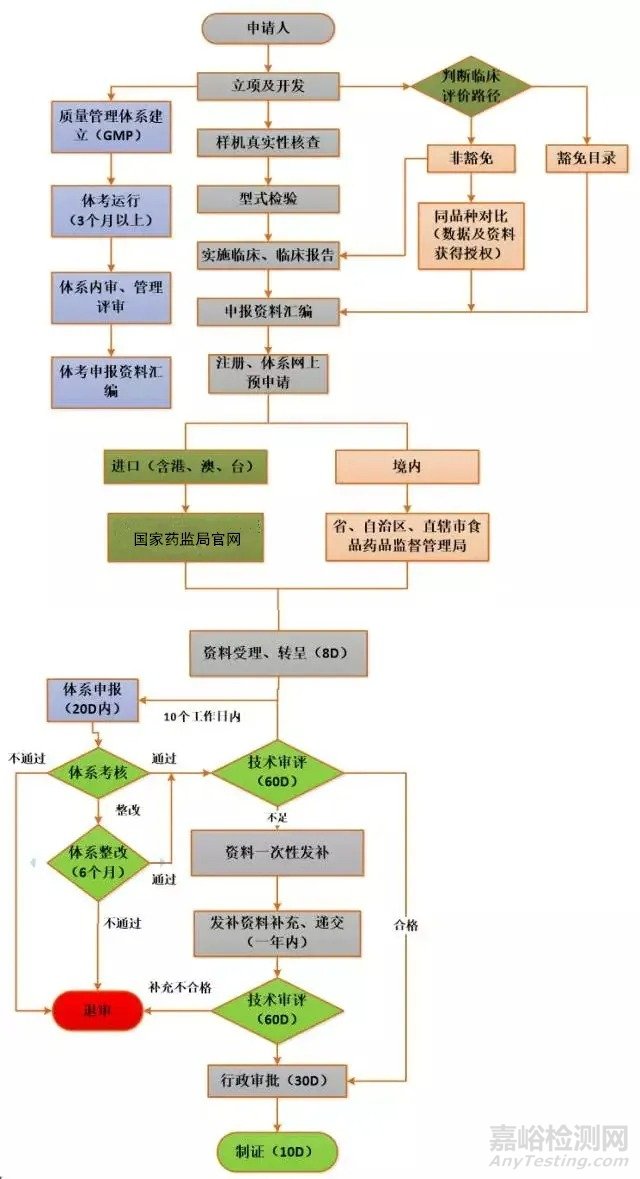
周期(含审批)
不含临床试验约需18个月;含临床试验约需18-36个月及以上。详情如下。
1、从产品立项到完成检测预计使用4-7个月。
2、如产品需做临床试验则需耗时6-12个月,具体视产品而定。
3、申报注册全过程需8个月(158个工作日,每月按20个工作日,不计节假日)。此处未将整改、资料发布等不确定因素的耗时计入。
03、三类医疗器械的注册流程
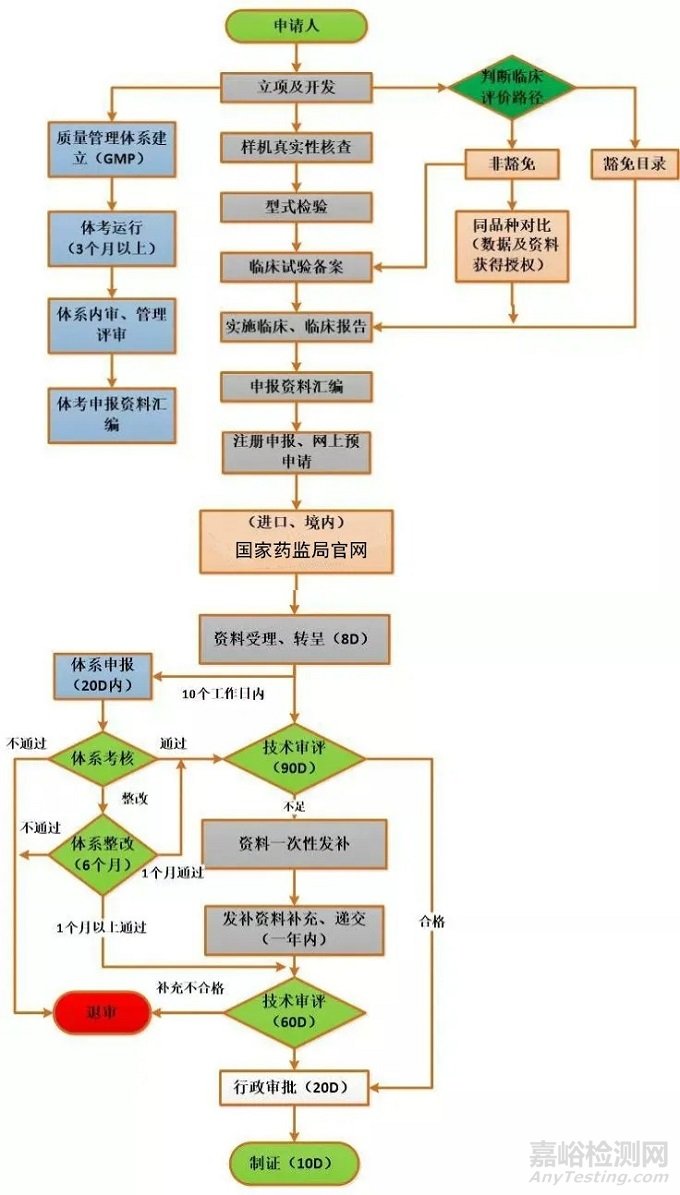
周期(含审批)
不含临床试验约需18个月;含临床试验约需18-36个月及以上。详情如下。
1、从产品立项到完成检测预计使用4-7个月。
2、如产品需做临床试验则需耗时6-12个月,具体视产品而定。
3、申报注册全过程需8个月(约158个工作日,每月按20个工作日,不计节假日)。此处未将整改、资料发布等不确定因素的耗时计入。
04、延续注册的流程
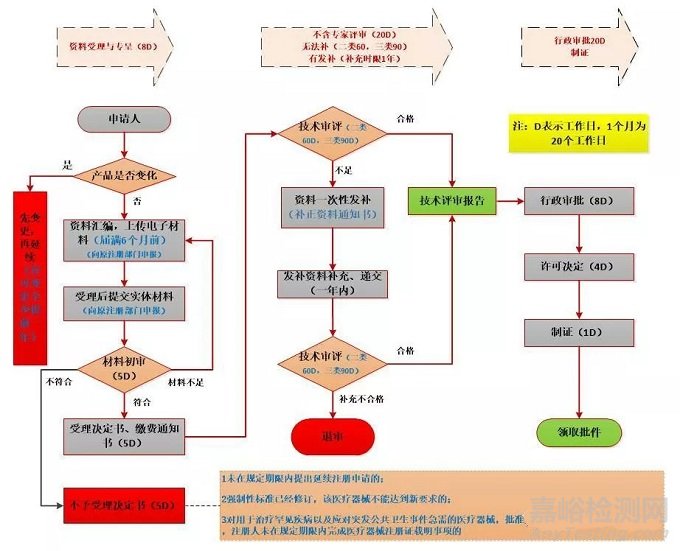
05、注册办理的流程
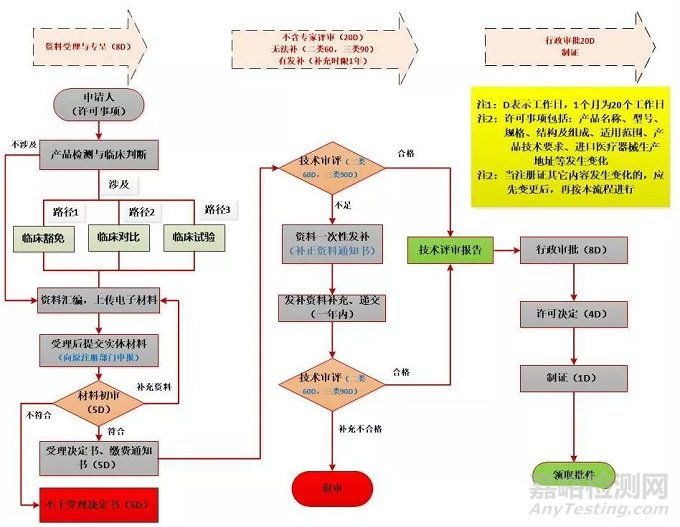
06、生产许可事项的办理流程
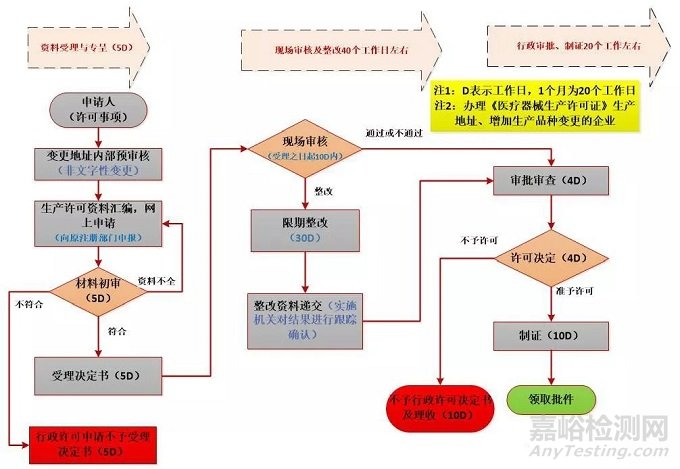
07、登记事项的办理流程
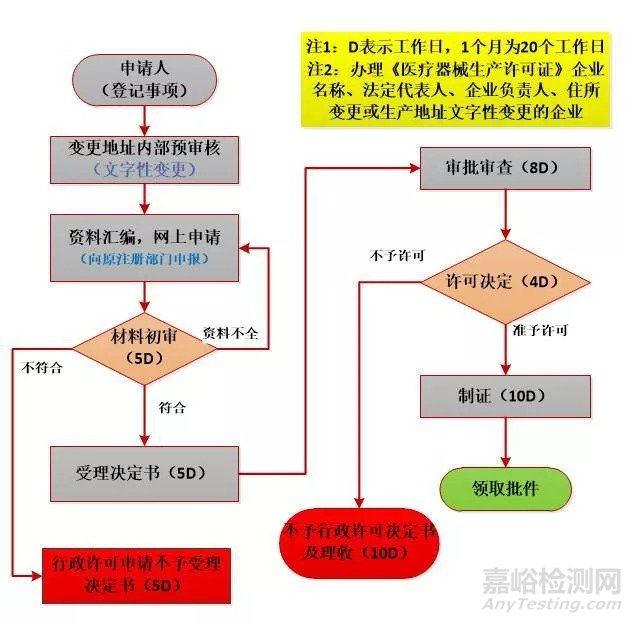
08、注册资料的说明
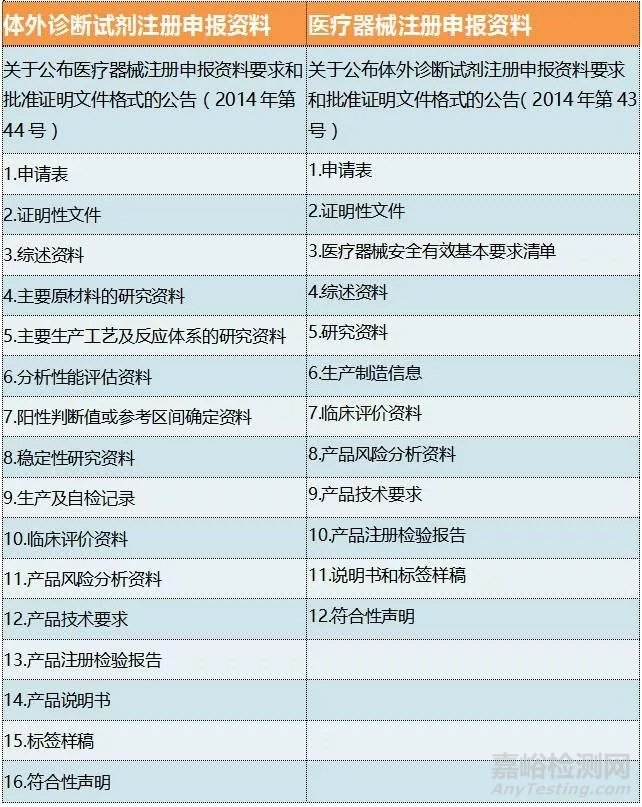
09、分类界定的流程
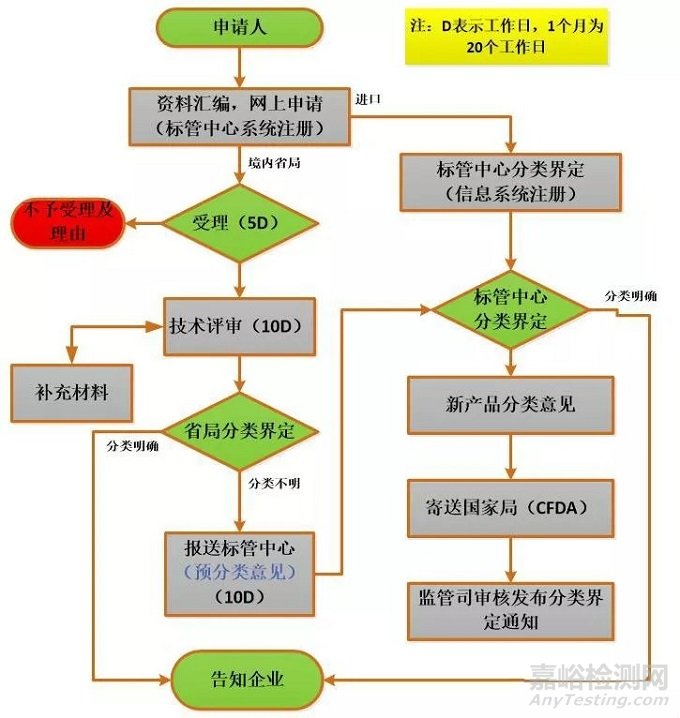
收费:免费。
周期:20-60个工作日及以上。
10、创新审批的流程
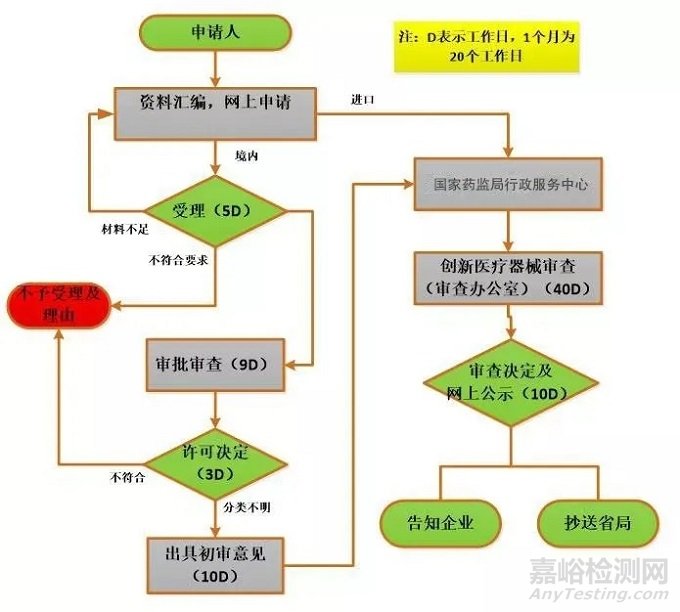
收费:免费。
周期:省药监局审批约需35个工作日;国家药监局审批约需50个工作日。

来源:Internet


