您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2019-09-04 09:09
「本文共:15条资讯,阅读时长约:3分钟 」
今日头条
上海泽生慢性心衰新药获FDA快速通道认定。上海泽生自主研发的具全新靶点与机制的注射用重组人纽兰格林获FDA快速通道资格认定。重组人纽兰格林是一种神经调节蛋白Neuregulin-1β2α的重组多肽片段,正在开发供慢性收缩性心力衰竭患者治疗使用的注射剂。现有临床证据显示,重组人纽兰格林能直接作用于受损的心肌细胞,修复心肌结构,有望改善患者心脏功能、逆转心室重构,提高运动能力及生活质量,并最终实现降低目标患者全因死亡率及再入院率的目的。该药在中国已纳入优先审评程序,目前处于审批阶段。
国内药讯
1.贝达药业盐酸恩沙替尼注册临床数据更新。贝达药业发布公告,该公司新一代 ALK 抑制剂盐酸恩沙替尼(X-396),在治疗克唑替尼耐药的间变性淋巴瘤激酶(ALK)阳性非小细胞肺癌患者的关键性Ⅱ期研究中表现出持续的治疗效果,经独立评审委员会对截至 2019 年5月底的最新数据进行评估,在疗效性方面,恩沙替尼整体ORR为52.6%,疾病控制率为87.8%,中位PFS为11.2个月,颅内ORR为71.4%,颅内病灶控制率达95.2%。该药此前已获纳入优先审评程序,目前,该公司正在递交补充材料,配合CDE的进一步审评工作。
2.拜耳氯化镭[223Ra]注射液拟纳入优先审评。拜耳抗癌药氯化镭[223Ra]注射液上市申请拟纳入优先审评公示名单。氯化镭[223Ra]注射液是全球首个α-粒子辐射放射性治疗药物,于2013年获FDA批准用于已发生骨转移的去势抵抗性前列腺癌患者的治疗,商品名为Xofigo。一项关键Ⅲ期临床ALSYMPCA研究数据显示,与安慰剂联合最佳支持治疗(BSoC)相比,该药联合BSoC使患者总生存期延长3.6个月( 11.3 vs14.9个月),并使死亡风险降低30%;Xofigo治疗组患者首次出现症状性骨骼事件的时间往后推迟(9.8 vs 15.6个月)。
3.石药集团HER2/CD3双特异抗体在美获批临床。石药集团非全资附属公司友芝友生物自主研发的注射用重组抗HER2/CD3人源化双特异性抗体(M802)获FDA临床批件。M802是一款针对乳腺癌、胃癌等恶性疾病的双抗药物,在临床前药理药效研究中,M802已被验证可有效激活T细胞,增加CD3阳性细胞对HER2阳性细胞的识别、结合和免疫杀伤能力,抑制HER2介导的下游信号分子MAKT及AKT的磷酸化,对HER2阳性肿瘤细胞的增殖有显著的抑制作用,并具有ADCC和CDC作用。M802目前正在中国开展临床试验。
4.信达生物IBI303 Ⅲ期关键研究结果发表。信达生物宣布由清华大学医学院徐沪济教授牵头的针对中国国产生物类似药Ⅲ期临床研究成果刊登在《柳叶刀•风湿病学》上,并获杂志封面推介。该研究是阿达木单抗生物类似药和原研药在活动性强直性脊柱炎患者中的大型头对头Ⅲ期临床研究,结果显示:第24周ASAS20应答有效率在IBI303组和阿达木单抗组中分别为75.0%和72.5%,临床等效性成立;此外,研究也达到包括第12周时的ASAS20有效率、第24周ASAS40、ASAS部分应答和ASAS5/6应答率等次要终点。
5. 信立泰拟对MA公司增资。信立泰全资子公司诺泰国际将以722.29万美元参与M.A. MED ALLIANCE SA公司新一轮普通股发行的认购。本次增资完成后,诺泰国际将持有MA公司约16.54%的股份。MA公司专注于高端心血管介入医疗器械的研发、生产,其核心产品雷帕霉素药物洗脱球囊Selution™在全球范围内拥有自主知识产权,拟用于治疗冠脉疾病或外周动脉疾病等。预计2020年该产品将获“外周血管适应症”、“冠脉疾病适应症”2个适应症的欧盟CE认证。信立泰去年已以1000万美元获得Selution™相关知识产权、技术信息等在中国大陆地区的独家许可使用权。
国际药讯
1.小野制药BTK抑制剂申请日本上市。小野制药开发的口服布鲁顿酪氨酸激酶(BTK)抑制剂tirabrutinib hydrochloride(ONO-4059,tirabrutinib)在日本提交上市申请,用于治疗复发、难治原发性中枢神经系统淋巴瘤(PCNSL)患者。此次申请基于一项多中心、开放标签、非对照I/II期研究(ONO-4059-02)的结果。该研究共入组44例复发、难治性PCNSL患者,研究中tirabrutinib每日口服一次。该药今年8月已获日本厚生劳动省(MHLW)授予治疗PCNSL的孤儿药资格。
2.阿斯利康公布达格列净详细Ⅲ期结果。在欧洲心脏病学会年会上,阿斯利康SGLT2抑制剂Farxiga(dapagliflozin,达格列净)公布Ⅲ期临床DAPA-HF的详细结果。DAPA-HF是首个研究SGLT2抑制剂与心衰造成的死亡和疾病加重风险的Ⅲ期临床。射血分数下降心衰患者(包含非2型糖尿病患者)在接受标准疗法以外,接受达格列净或安慰剂的治疗。数据显示,达格列净将患者的心衰加重事件和心血管死亡风险降低26%(HR=0.74,95%CI:0.65,0.85,p=0.00001),包括将心衰加重风险下降30%,将心血管死亡风险下降18%;在非2型糖尿病患者中达格列净将心衰风险降低27%,与2型糖尿病患者相当。
3.罗氏流感新药Xofluza 两项Ⅲ期临床结果积极。罗氏在OPTIONS X 2019会议上展示其内切核酸酶抑制剂Xofluza两项III期临床的积极数据。在III期临床BLOCKSTONE研究中,试验者在接触家庭感染成员后,使用Xofluza(baloxavir marboxil)进行预防性治疗,与安慰剂相比,患流感的风险显著降低86%;Xofluza治疗组的不良事件总体发生率为22.2%,安慰剂为20.5%,试验过程中没有发生严重不良事件。另一项III期临床研究MINISTONE-2也达主要终点,Xofluza的疗效与奥司他韦的疗效相当。与奥司他韦相比,单剂量Xofluza将流感病毒从儿童患者(未满12周岁既往健康的流感患者)体内排出的时间缩短两天多。
4.长效PCSK9抑制剂inclisiran公布III期临床ORION-11研究数据。The Medicines Company公司在2019年欧洲心脏病学会年会上公布其长效PCSK9抑制剂inclisiran III期临床ORION-11研究的全部数据。患有动脉粥样硬化心血管疾病或使用他汀类疗法仍不能控制LDL-C水平的患者每年只需接受inclisiran两次皮下注射,结果显示:在第510天,安慰剂调整后的平均LDL-C水平降低为54%;第90天至第540天,安慰剂调整后的时间-平均LDL-C水平降低为50%,2个数据均具统计学意义。inclisiran降低LDL-C的疗效与现有的PCSK9单抗药物相似。预计2019年底在美国、2020年初在欧洲提交其上市申请。
5.阿斯利康创新药Fasenna获孤儿药资格。阿斯利康创新药物Fasenna获FAD授予孤儿药资格,用于治疗嗜酸性食道炎(EoE)。Fasenra是一种单克隆抗体,可直接与嗜酸性粒细胞上的IL-5受体结合,并促使自然杀伤细胞(NK)通过细胞凋亡诱导嗜酸性粒细胞快速死亡。该药已于2017年11月获FDA批准上市,用于12岁及以上重度嗜酸性粒细胞哮喘患者的附加维持治疗。近两年来,FDA先后授予Fasenra治疗嗜酸性肉芽肿性多血管炎(EGPA)和嗜酸性粒细胞增多症(HES)的孤儿药资格。除EoE外,阿斯利康还在探索Fasenra对鼻息肉病和慢性阻塞性肺病的疗效。
6.Polpharma Biologics宣布全球商业化那他珠单抗。Polpharma Biologics S.A.与Sandoz AG公司就那他珠单抗生物仿制药达成全球商业化协议。该仿制药由Polpharma Biologics公司开发,目前处于Ⅲ期临床阶段,用于治疗复发缓解型多发性硬化症。Polpharma Biologics是一家专注于开发和制造生物仿制药和新型生物药的制药公司,该公司与Polpharma Biologics Group旗下的其他关联公司一起,提供从细胞系开发到商业产品供应的全面一体化生物制品服务。根据协议,Polpharma Biologics将负责开发、制造和供应该仿制药,获批后,Sandoz AG将通过独家全球许可,将该药物商业化并在所有市场销售。
医药热点
1.同济医院:国际首部系统论述乙型肝炎重症化全英文专著全球发行。同济医院感染科宁琴教授担任独立主编,世界著名的Springer出版社与华中科技大学出版社联合出版的国际首部论述乙型肝炎重症化的全英文版专著Acute Exacerbation of Chronic Hepatitis(共两卷)线上线下全球同步发行。该专著是我国专家首次将乙型肝炎重症化的中国观点、中国理论、中国实践推向世界的全英文学术著作。为临床医师和科研人员提供了最新的技术和最先进的治疗策略,为其他终末期肝病治疗提供了有价值的参考。
2.上海启动首批健康村镇试点。作为贯彻落实《健康上海行动》的第一项举措,上海市爱卫办近日召开健康村镇试点建设启动会,为首批136个试点单位授牌。到2020年,上海计划建立健全健康镇(街道)、村(居)建设管理机制,建成20个健康镇(街道)、100个健康村(居)委会,为深入推进上海健康乡村建设工作提供可借鉴的范本。目前,上海市爱卫办已与复旦大学公共卫生学院签订合作协议,由复旦大学公共卫生学院为全市健康村镇建设提供技术指导。
3.日本实施全球首例iPS细胞角膜移植手术。来自日本大阪大学西田幸二教授的研究团队完成了全球首例利用诱导多能干细胞(iPS细胞)培养出的角膜组织进行移植的临床手术。接受移植的是一名患有重度“角膜上皮干细胞衰竭症”的女性。研究团队利用京都大学iPS细胞研究所储备的iPS细胞培养出角膜细胞,制作成厚度约0.05毫米的膜片状组织,并移植到患者眼中。患者术后视力有所改善,目前已出院。研究团队表示,将用一年时间跟踪观察移植的安全性和效果。
【人福医药】(1)控股子公司宜昌人福收到FDA关于萘普生钠片的批准文号。(2)控股子公司宜昌人福收到国家药监局核准签发的盐酸羟吗啡酮片的《临床试验通知书》。
审评动向
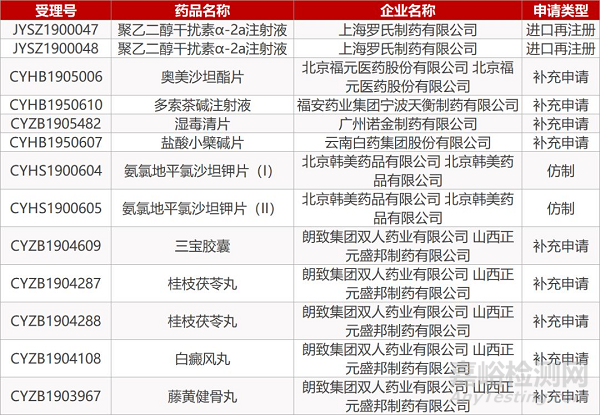
1. CDE最新受理情况(09月03日)
2. FDA最新获批情况(北美09月02日)
暂无

来源:药研发


