您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-08-11 15:41
近日,北京先瑞达医疗科技有限公司(简称“先瑞达”)宣布其自主研发的西罗莫司药物涂层冠脉球囊扩张导管——AcoArt Canna®成功获国家药品监督管理局(NMPA)批准上市(国械注准20253031486)。
继AcoArt Camellia®冠脉紫杉醇涂层球囊成功上市后,AcoArt Canna®的推出标志着先瑞达在冠脉DCB领域完成西罗莫司+紫杉醇双技术平台布局,进一步巩固了公司在药物涂层技术方面的全球领先地位,并为公司在冠脉介入领域开疆拓土打下坚实基础。

# 研究背景
冠状动脉疾病(CAD)是全球致死率最高的疾病之一,其中冠脉分叉病变占据了相当一部分比例。根据多项研究数据,冠脉分叉病变约占PCI(经皮冠状动脉介入治疗)治疗病变总数的15-20%。这一病变的复杂性和不确定性导致了临床治疗中的许多挑战,尤其是在进行药物治疗时。
分叉病变的形态多变,包括血管角度、斑块分布以及血管直径等因素,常使得传统的冠脉介入治疗方法效果有限,甚至可能增加治疗失败的风险。
因此,如何简化治疗方案、提高疗效和安全性、减少药物依赖性成为了当前临床治疗中的重要问题。
药物涂层冠脉球囊(DCB)作为一种“介入无植入”的治疗方式,被视为治疗分叉病变的潜力解决方案,尤其在避免支架植入的情况下,它的疗效和安全性得到了广泛关注。
DCB方面包括药物类型如紫杉醇、雷帕霉素及二者的混合物;涂层工艺如微晶涂层、缓释涂层、纳米涂层;球囊设计如与斑块更贴合的易形球囊、通过微孔灌注药物的灌注球囊、结合切割、震波、超声等功能的融合球囊技术等。
“介入无植入”理念是一种新兴的冠心病介入治疗理念,其核心是在开通和修复病变血管的同时,避免永久性植入器械留存体内,从而使血管最大限度地恢复到原始的健康状态。这一理念的出现主要是为了解决传统金属支架植入后可能引发的远期问题,如支架内再狭窄、慢性炎症反应、血管弹性受限等。
据EuroPCR 2025大会专家预测,未来介入无植入治疗方案比例将有望达到75%,其中60%为DCB,15%为BRS。
# 产品介绍
AcoArt Canna®是先瑞达推出的公司首款西罗莫司药物涂层冠脉球囊扩张导管,它是针对分叉病变的一项创新产品,代表了先进的药物涂层技术。这款产品将用于治疗血管直径≥2.0mm且≤4.0mm的原发冠状动脉分叉病变狭窄,进一步拓展了先瑞达在冠脉介入领域的技术实力,并标志着公司在全球药物涂层技术方面的领先地位。
该产品的最大亮点之一是采用了先进的西罗莫司药物涂层技术。西罗莫司作为一种免疫抑制剂,具有显著的抗内膜增生作用,可以有效防止支架植入后血管再狭窄的发生。
与传统的紫杉醇药物涂层相比,西罗莫司的组织吸收速率较低,组织留存更少,这一特性使得药物涂层的研发具有更高的技术难度。
然而,AcoArt Canna®通过亲脂性载药基质的创新设计,成功实现了西罗莫司药物的高效、缓释地递送到靶血管组织,确保药物在治疗过程中能够持续发挥作用。通过这一技术创新,AcoArt Canna®能够有效减少药物在输送过程中的损失,同时提升药物在目标部位的留存率,从而达到理想的临床疗效。
此外,AcoArt Canna®的载药基质可被人体完全代谢,不仅提高了药物的生物相容性,也增强了其在临床应用中的安全性。
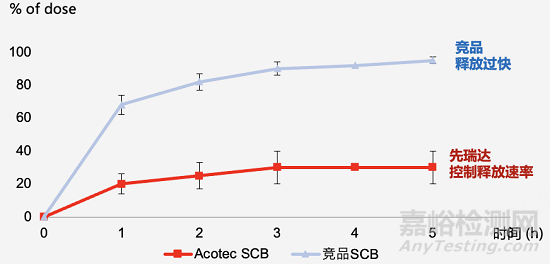
▲体外测试:先瑞达西罗莫司药物涂层的药物释放速率慢于竞品
# 临床试验结果
临床试验中,先瑞达AcoArt Canna® DCB作为试验组产品,垠艺生物的轻舟®紫杉醇药物涂层球囊作为对照组产品。垠艺生物的轻舟®药物洗脱球囊是国际首个适用于原发冠脉分叉病变的产品,也是国内首个取得注册证的产品。
临床试验共入组了230名患者,1:1进入试验组和对照组。主要临床终点指标为术后9个月时血管造影显示的靶病变分支血管直径狭窄率(DS, %):试验组数据为30.52%,对照组数据为33.46%,试验组数据优于对照组,两组差异无统计学意义,非劣假设成立。
而从临床安全性试验数据上看,随访期内,全因死亡与心源性死亡发生率两组间的差异无统计学意义(P>0.05),心肌梗死及靶血管相关心肌梗死发生率两组间的差异也无统计学意义(P>0.05),进一步证明了先瑞达AcoArt Canna®西罗莫司冠脉DCB的安全性。

# 药物涂层球囊市场概况
裸金属支架(BMS)的出现在一定程度上解决了球囊扩张后可能会面临的血管壁夹层、血管急性闭塞和血管弹性回缩等问题,但却带来了另一个严峻的挑战,即支架内再狭窄。金属支架对血管内膜的持续性刺激,可导致血管内膜增生过度,引起支架内再狭窄(ISR),发生率可达30%。
药物涂层球囊扩张术使药物作用于血管内壁,维持血管通畅效果更佳且不留异物在血管内,在血管内再狭窄ISR、小血管、分叉病变有明显优势,原发病变的扩展也不断探索验证。
随着近年来“介入无植入”理念的推广,药物涂层球囊使用量快速增长。根据弗若斯特沙利文预测数据,药物涂层球囊首次在中国获批用于冠状动脉疾病的治疗后,使用量从 2016 年的 7500 个大幅增长至 2021 年的 29.0 万个。预计 2025 年市场规模将进一步攀升至 100.0 万个,2030 年预计将达到 204.2 万个。
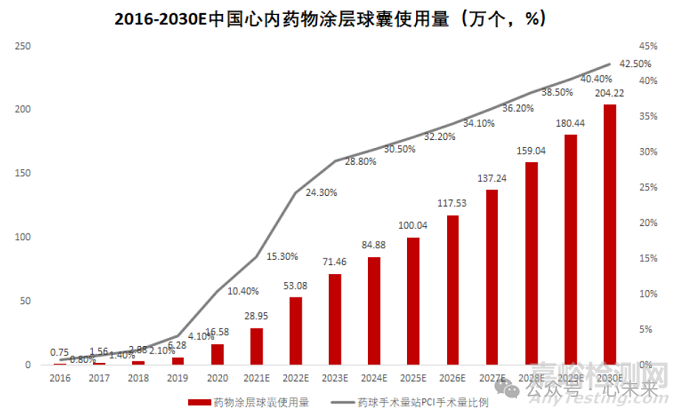
▲源于弗若斯特沙利文
根据弗若斯特沙利文预测数据,国内冠脉药物涂层球囊的市场规模从 2016 年的 1.35 亿元大幅增长至 2021 年的 20.09 亿元,预计 2025 年市场规模将进一步攀升至 43.86 亿元,2030 年预计将达到 59.33 亿元。
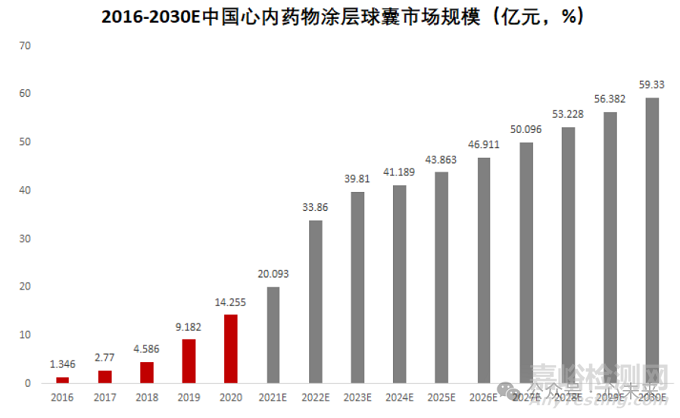
▲源于弗若斯特沙利文
冠脉药物涂层球囊是高端第三类医疗器械,产品具有高精密技术,进入壁垒较高的特点。我国药物球囊行业发展起步较晚,发展时间较短,国内市场由数家公司主导,仍有较大的进步空间。
德国贝朗的 SeQuent Please 是我国最早上市的药物涂层球囊,其适应症为冠状动脉支架内再狭窄治疗。垠艺生物的轻舟®药物洗脱球囊于 2017 年获原国家食品药品监督管理总局(CFDA)优先审批上市,是国际首个适用于原发冠脉分叉病变的产品,也是国内首个取得注册证的产品。
随着临床应用研究逐步开展,参与者陆续取得冠脉药物球囊产品注册证,如上海申淇、乐普医疗、凯德诺(远大医药)、赢生医疗、巴泰医疗、鼎科医疗。未来随着更多竞争对手和竞品进入市场,市场竞争将加剧,但竞品的进入也将进一步加强行业的国内市场教育,促进产品市场渗透率提高。
其中,垠艺生物的轻舟®药物洗脱球囊具有出色的通过性及输送性、优异的药物涂层品质,已在多家知名心血管医院及国内逾千家医院进行临床应用,上市后销量增长较快,打破了德国贝朗的市场垄断。

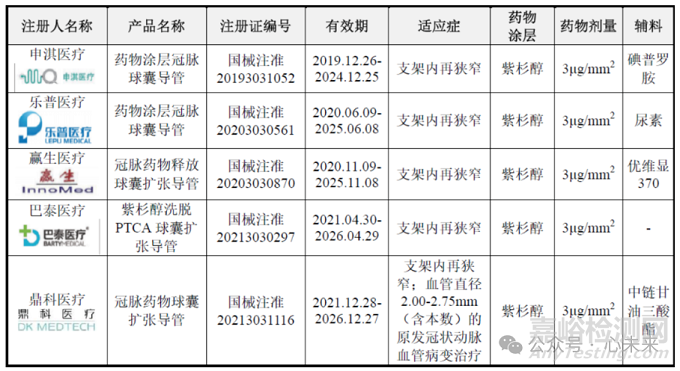
▲冠脉药物球囊竞品信息对比(源于垠艺生物招股说明书)
申淇医疗是国内第二家获证的DCB企业,其研发的淇济®swide®药物涂层冠脉球囊导管使用紫杉醇+碘普罗胺的药物组合,拥有创新超声喷涂技术,致密性更好,而且可在病变处停留长达28天。该产品于2019年在我国获批上市,适用于冠状动脉ISR的治疗。
鼎科医疗与美敦力合作研发的Dissolve™冠脉药物球囊于2021年12月在我国获批上市,球囊表面涂有紫杉醇,载体为中链甘油三酸脂,用于冠状动脉ISR和原发小血管病变的治疗。该球囊的三段式输送可以更好的保障药物充分转移且延缓稀释,优化的输送杆可保证力的传导、平滑过渡的导丝导入口可提高跟踪性。
除了上述企业外,还有浙江乾合畅脉医疗科技有限公司的紫杉醇药物涂层冠状动脉球囊扩张导管(2023年获批,用于分叉病变)、瑞维特医疗研发的药物涂层PTCA球囊扩张导管(2023年获批,用于小血管病变)、恒壹医疗冠脉药物涂层球囊扩张导管(2023年获批,用于ISR、分叉病变)等均已获批上市。
DCB技术作为行业新星,在多项临床数据结果上的表现与老牌选手药物洗脱支架无明显差异,而且再狭窄率,药物洗脱效率,药物传输效率,聚合物残留,无植入支架,晚期血栓风险方面表现优异。该赛道本土企业的加入也极大地改变了市场格局,如申淇医疗、乐普医疗和垠艺生物等在市场中的占比已经反超进口产品。在价格和政策环境的支持下,本土企业有望在未来的竞争中占据更大的市场份额。

来源:心未来


