导语:本文为总结性学习,参考申高老师《医疗美容激光产品注册常见问题解析》培训、强脉冲光治疗设备注册审查指导原则(2023年修订版)、半导体激光脱毛机注册技术指导原则、激光治疗设备同品种临床评价注册审查指导原则、CMDE共性问题等,探讨技术评审流程、注册资料要求及医疗美容激光产品注册申报过程中的常见问题,以为诸君在研发过程中提供点滴参考。
写在前面的话
随着时间的推移,我们国家的人民生活品质不断攀升,对美的渴望也逐步加深。得益于自媒体和网络的迅速发展,我们现在可以轻松地获取各类医疗美容信息。无论走到哪里,街头地铁站到处都是医疗美容的广告。我曾在互联网上看到一张图片,许多广告都会采用类似的对比手法。那么,大家对这种产品有何感想呢?实际上,我们甚至可以足不出户,在网上订购脱毛等服务。多年前,人们可能会认为只有明星才会涉足医疗美容领域,但现在,医疗美容已经普及到几乎每个人都能轻松接受的程度。
第一部分 医疗美容的应用
首先,激光设备被广泛用于改善皮肤外观,这是其应用最广泛的部分。这包括但不限于治疗皱纹、改善血管状况、去除色素斑点、淡化疤痕,以及解决皮肤敏感和痤疮等问题。多数产品都专注于这一领域,旨在帮助用户提升皮肤外观的美观度。光子嫩肤介绍可点击图片参考器审中心漫画全面介绍。
其次,激光技术也用于毛发管理,具有促进毛发生长和抑制脱发的双重效果。这使得激光产品在脱毛和生发市场上有着广泛的应用。激光脱毛介绍可点击图片参考器审中心漫画全面介绍。
最后,激光设备还被用于脂肪处理,包括体表和体内的操作。这一应用范围涵盖了从减少脂肪堆积到雕塑身体曲线等多种医疗美容服务。
以上三个方面共同构成了激光设备在美容领域的全面应用,展示了激光技术在改善人类外观方面的多样性和有效性。
第二部分 相关的指导原则
可见光谱治疗仪注册技术审查指导原则
强脉冲光治疗设备注册审查指导原则(2023年修订版)
半导体激光脱毛机注册技术指导原则
激光治疗设备同品种临床评价注册审查指导原则
以上指导原则可在微信公众号内回复 激光美容 获得。
第三部分 注册申报资料的要求
在121号文中有详细的规定关于注册资料的撰写,这里不一一列举,主要介绍一些特别的点。
3.1 综述资料
综述资料主要包括四大内容:工作原理、结构组成、产品的主要功能以及适用范围。
(1)工作原理非常关键。激光器的种类繁多,包括固体激光器、气体激光器、半导体激光器等。
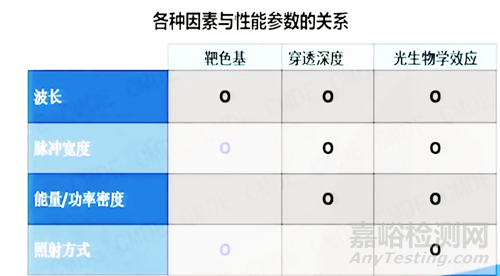
(2)在申报时需要详细描述内置激光器的类型和作用机理,主要描述激光与生物组织相互作用的机理,例如激光的穿透深度和热效应等。
(3)结构组成主要描述设备的结构,包括激光器结构、病人装置、手柄等。如果有可能,那么希望大家提供一些区别于其他产品特征、综述资料的要求和形式,大家可以参考场外提供的例子。
(4)产品的主要功能分为三部分:第一部分是提供输出模式,这部分指激光器输出的是连续或脉冲。脉冲包括几种模式,如自由振荡模式、外部服务模式或其他分段脉冲模式。重复键的功能,例如手柄的作用,扫描技术是否可行。第三个是软件功能,大部分设备可能利用软件控制输出后的图形和扫描方式。
如果有可能,那么希望大家提供一些区别于其他产品的特征。综述资料的要求和形式,大家可以《强脉冲光治疗设备注册审查指导原则》。
接下来,介绍一些例。在《强脉冲光治疗设备注册审查指导原则》中的例子中都有体现。应说明设备的光源种类、形成光脉冲的原理,以及滤除光谱采用的方法。
强脉冲光是一种非激光的光源,它是由单个或多脉冲序列组成的非相干光,具有频谱范围宽、能量密度高的特点。可利用滤光片或采用镀膜的方式滤除不期望出射的光谱。 例如,强脉冲光设备的光源是氙灯,其基本工作原理是触发器对氙气施加高电压触发氙气电离,通过储能电容在相对较长时间的充电后,在极短的时间内放电,引起灯管内氙气雪崩式电离,氙气以高强度光辐射的形式将所充电能转化并释放,这个放电过程即是一个光脉冲。采用导光晶体上镀膜的方法滤除光谱,560治疗头导光晶体上所镀膜层可滤除短于560nm的波段,保留波长范围在560nm~1200nm之间的光谱。
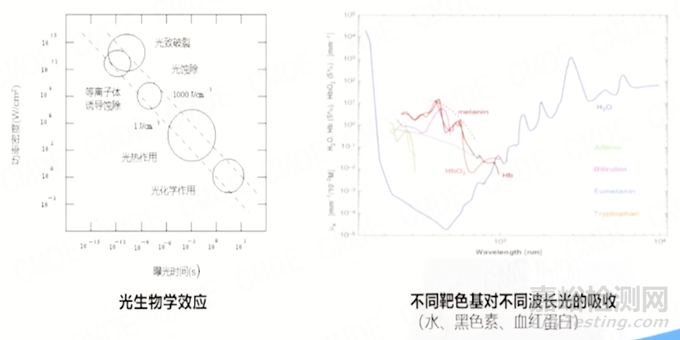
以上内容基本回答了光有什么特性以及是如何产生的问题。关于作用机理,我们看下这两张图。
这两张图可以在各个文献和教科书均可查阅。主要涉及两个问题,第一个是光的生物学效应,器审中心通常会发补光生物学效应,他们指的是左边的图。不同光的生物学效应与功率密度的发光时间密切相关,关于光化学作用还是光热作用以及光热过滤程度,在制作资料时需要进行初步判断。第二个是不同靶色基对不同波长光合的吸收。在医疗美容应用上,主要有三个不同靶色基,如黑色素、氧合血红蛋白、水。尤其是中国大部分黄种人。黑色素基大部分都是吸收的,因此需要考虑黑色素微波的阻挡和吸收,可以看到不同波长对不同发射器有不同的技术效果。
血管壁的主要结构是上皮与蛋白,呈白色,对光吸收较少。但其内流动的血液,即血红蛋白具有颜色。血红蛋白在480 nm有最大吸收峰,在540 nm和577 nm有两个次高峰,在940 nm附近还存在一个更低的吸收峰。特定波段的IPL,可以被血红蛋白强吸收。当光波脉宽与治疗血管的热弛豫时间适配时,就会通过能量转化、聚集,产生温升,并使热能主要集中在血管内及其邻近组织。当温度升高达到一定程度,就可造成毛细血管内皮与管壁蛋白收缩、变性、凝固甚至坏死,毛细血管腔闭锁,并逐渐被纤维组织替代,最终实现治疗病变血管的目的。
《强脉冲光治疗设备注册审查指导原则》强脉冲光在血管病变上的作用机理
眼部、全身因素、药物、环境、饮食等多重因素均可导致睑板腺终末导管阻塞和(或)睑酯分泌异常,从而引起泪膜稳定性下降和眼表炎性反应、眼部刺激症状和损伤,并导致干眼恶性循环。 IPL通过选择性光热作用封闭睑缘异常扩张的毛细血管,可减少炎性介质的分泌。热效应可以融解睑板腺睑脂、疏通睑板腺导管,恢复并改善睑脂排出能力;可减少蠕形螨,阻止炎症的级联反应,减少眼睑皮肤痤疮丙酸杆菌等微生物负荷等。同时,IPL还可上调抗炎因子在局部组织的表达、下调促炎因子在组织的表达,抑制基质金属蛋白酶的活化,促进睑缘微环境的平衡。从而达到治疗睑板腺功能障碍相关性干眼的目的。
《强脉冲光治疗设备注册审查指导原则》强脉冲光在治疗睑板腺功能障碍相关性干眼的作用机理
对于同类或前代产品的比较:希望大家能详细描述,提高数据模型各项参数的比较必须非常有限,说明产品性能参数与同类产品存在差异。这里不要求大家一定要涵盖技术要求那么细致,希望大家至少提供几个方面的比较:一是结构组成对比;二是图片性能参数对比;三是波长脉宽、能量波宽大小;四是四是操作方式对比;五是设备和形式在一起时如何操作。建议以列表的方式表述,比较的项目应至少包括产品名称、型号规格、工作原理、作用机理、治疗头滤光方式、终端输出脉冲光波长范围、脉冲能量及能量密度、脉冲宽度、关键组件、预期用途等。包括申请人已经上市同类产品或其他企业已经上市的同类产品。
3.2非临床研究资料
(1)性能研究:
非临床研究主要的发补集中在性能研究,常见的发补问题包括:
(a)注重从机理方面说明能量、脉宽、重复频率等性能指标设定的原因及依据(理论):性能指标的确定并非仅仅参考行标或产品,这样显然不行。因为需要告诉具体指标设定的原因、理论根据、是否进行过实验以及同类产品的指标,所以这需要大家具体说明。
(b)提供激光输出各模式(连续、脉冲等)波形图;
(c)详述产品调节能量的方式,是调节脉宽还是提高功率:产品调节能量的方式是调节脉宽还是提高功率?有些脉冲产品在调节能量时本身就发生了变化,例如从3焦到5焦,对于肤质或者不了解此产品的人而言会有变化,能量从3焦变到5焦。更深层次的是我们需要了解调节脉宽的方式。你是指将脉宽调得更长,导致整个脉冲能量变大还是真正提高了功率?因为提高功率与效率相关,提高脉宽会增加加热时间,所以这两个最终产生的作用会不同。
在性能研究中,好需要提交量效关系,以说明设置参数的安全性、有效性和合理性。同时,还要考虑能量安全,例如能量不会对正常组织造成不可接受的伤害。在提交资料时,可以包含动物实验资料或实验室资料,但无论提交何种资料,希望大家都能考虑这两方面。不仅要关注产品机理、设计合理性和有效性,还要明确在使用于其他非正常组织时是否安全。
以色素为例,这个产品已经相当成熟。在资料准备时,可以通过模型实验,如果有很多色素,经过色素吸收后,申报波长对色素去除效果较高,可以进行离体组织实验。例如,在动物皮肤里嵌入色素颗粒,再进行相关实验。如果波长比较新,可能会涉及实验。对于成熟产品,通常只需模型实验或立体组织实验就足够。对于较新产品,功率较大,建议大家进行动物实验研究。
此外,还需关注不同剂量下的使用效果,希望大家提供研究资料证明最大剂量的安全性。关于是否设置对照,通常建议大家设置对照。在重新比对时,对照会更加客观。
(2)生物学评价
生物学评价要求对成品中与患者之间或间接基础材料的生物学项目进行评价,主要有两个方面:一是通过涂抹冷凝胶。之前有些产品涂抹冷凝胶后几乎不接触型,但实际上可能是间接接触。因此,即使包含涂抹凝胶的产品,仍需开展研究。另外,一些残留灭菌产品需在灭菌实验后进行正确试验,请大家关注。
第四部分 技术评审流程图
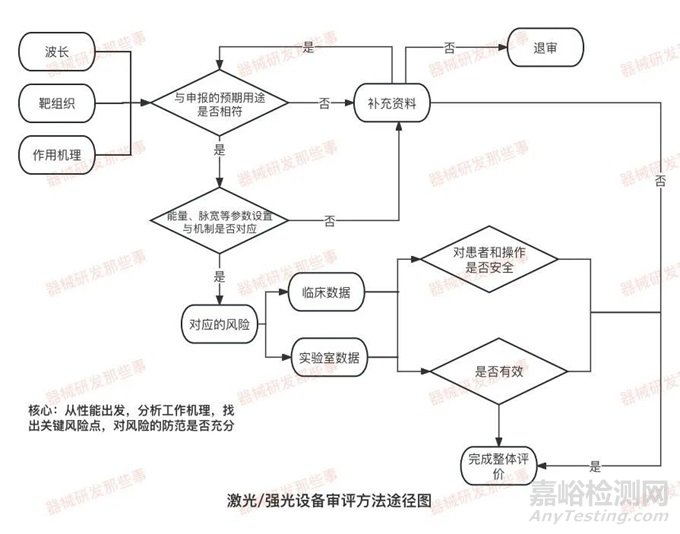
这里提供一份激光/强光设备技术审评的方法流程图,正如之前提到的机理与波长密切相关。在撰写资料时,需要思考是否与申报预期用途相同,还是系统参数设置与机制对应?审评员会从性能参数出发,在拿到资料后,查看参数是否与资料中描述的工作机制相对应,并找出风险点,判断提交资料中对风险防范是否充分,是否通过验证。建议申请人和注册人员在制作资料时明确工作机制作用,这需要花费一定时间积累。关于性能参数设置,需依据产品设计输出是否满足输入要求,提交资料是否充分验证。
第五部分 常见问题
(1)激光治疗仪用于脱毛时为降低皮肤表面温度会使用冷喷剂,对于冷喷功能有何要求?进行性能、安全及电磁兼容检验时,是否需考虑冷喷功能?
申请人应当依据冷喷功能的使用方式、功能设计、是否可设置开关等,自行明确与冷喷功能相关性能指标(如:持续时间、间隔时间、冷却效果等),并提供相关指标及试验方法的确定依据。性能及安全检测时需考虑冷喷功能,并配合冷喷剂进行测试;电磁兼容检验应考虑开启冷喷功能对产品的影响,并选择最不利情形进行测试。
(2)二氧化碳激光治疗仪采用了新的设计结构,用于新的临床应用部位,是否需要进行动物实验?动物实验是否需要设对照组?
动物实验主要为产品设计定型提供相应的证据支持,为医疗器械能否进入临床研究阶段提供依据,实现对临床受试者的保护。若产品采用新的作用机理、工作原理、结构设计、应用方法(如手术操作)、改进某方面性能等,申请人应针对产品创新点相关风险进行评估,并对风险控制措施有效性进行验证和/或确认,参照风险管理判定原则确认是否开展动物实验。
若拟申报的二氧化碳激光治疗仪采用了新的结构设计、改进了性能,或采用了新的功能(如点阵扫描)、用于新的临床用途,如台架性能试验研究不足以判定其基本安全性时,建议在临床试验之前开展动物实验。
动物试验不要求必须设置对照组。
(3)同品种对比对比哪些项目?
具体可参考《激光治疗设备同品种临床评价注册审查指导原则》。这里简单介绍下支持性证据,通过论述差异性不对产品安全有效性产生不利影响时,根据结果选择离体组织试验和动物试验。
(4)说明书的相关说明
由于这类产品可以在医疗机构或家庭使用,因此针对在医疗机构使用的需要在说明书注明:“经由培训的专业医生使用”;在家庭使用的,需要说明书中注明:“在医生指导下使用”。