您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2023-09-06 09:34
肠道水疗机用于医疗机构治疗时将液体灌注到患者肠道内,同时通过排液管将液体引流到体外实现对肠道的清洗所使用的设备,不含液体。一些肠道水疗机也集成了给药治疗功能。
根据《医疗器械分类目录》,分类编码为09-08-05,管理类别为Ⅱ类。
一、肠道水疗机的结构组成与工作原理
1、工作原理
肠道水疗机通过应用程序控制泵、电磁阀,同时利用温度、流量、压力传感器采集数据和反馈控制,并配合使用直肠管,从而实现向人体的肠腔内灌注液体、排出废液的功能。
2、结构组成
该产品通常由主机、加热装置、控制系统、液箱(液袋)、泵、治疗机管路(含注液管、排液管)等组成。
2.1加热装置:该部分用于液体加热。应明确加热方式,如加热盘、加热棒、加热板或发热片等。明确加热元器件的电压、电流、功率及安全防护措施。
2.2控制系统:通过压力、流量、温度传感器采集数据,监测、反馈控制泵等装置,配套使用直肠管经直肠导入,实现向人体的肠腔内灌注液体、排出废液功能。该部分实现对治疗过程的液位、时间、压力、流量、温度、报警等指标的控制、显示、输出,应明确具体的控制部件、控制方式、控制参数。
2.3泵:用于将液箱(液袋)内的液体直接输送到患者肠道内。应明确泵的种类及相应参数。
2.4治疗机管路:用于液箱、给水泵或药泵与直肠管(或相关肠道灌排导管)之间的连接,辅助实现结肠灌注与排泄功能。应明确管路的具体形式、材料及生物相容性。
应用软件:产品结构组成中包含软件,且软件属于关键部件,应增加软件功能的描述举例。
产品结构图及实物图示例如图1-4。
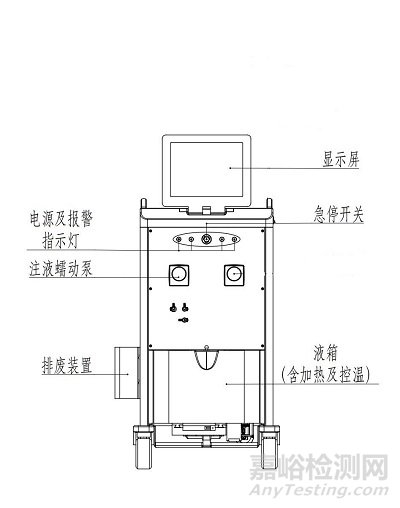
图1 肠道水疗机结构图示例

图2 推车式肠道水疗机示意图
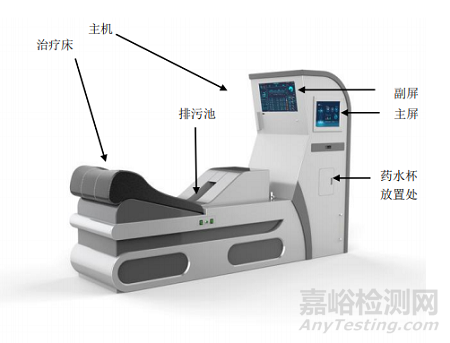
图3 床式肠道水疗机示意图


图4 便携式肠道水疗机示意图
二、肠道水疗机的主要风险
依据GB/T 42062附录E(见表1)列举了肠道水疗机产品有关的可能危害示例的不完全清单,以帮助判定与肠道水疗机产品有关的危害。企业还应根据自身产品特点确定其他可能危害。针对产品的各项风险,企业应采取控制措施,确保风险降到可接受的程度。
表1 肠道水疗机主要危害
|
可能的危害 |
可能的原因 |
造成的后果 |
|
|---|---|---|---|
|
能量危害 |
电磁能 |
设备受到电磁干扰;设备产生电磁能 |
设备运行异常或不能工作;影响操作者健康或其他设备使用 |
|
漏电流 |
电击 |
操作者受到电击伤害 |
|
|
热能 |
设备加热功能失常 |
液体温度超温或过低,伤害患者。影响治疗效果 |
|
|
机械能 |
压力测量不准确 |
灌注压力过高导致肠腔穿孔,甚至死亡;压力过低,影响治疗效果 |
|
|
生物学和化学危害 |
微生物污染 |
治疗机管路、液箱及贮药装置中的药液长期储存,有超标微生物进入人体 |
导致患者感染 |
|
生物相容性 |
与患者人体接触部分的原材料有毒有害 |
对患者产生毒性或刺激 |
|
|
化学残留 |
清洁或消毒残留物超标 |
对患者肠粘膜产生刺激或危害 |
|
|
信息 危害 |
标记 |
标记缺少或不正确,标记的位置不正确,不能永久贴牢和清楚易认等 |
设备信息不明确;错误操作,影响治疗效果 |
|
说明书 |
说明书未对消毒等维护信息作出详细说明;说明书未对故障排查作详细说明;说明书未对合理可预见的误用进行警告 |
非预期使用;设备运行异常或不能工作 |
|
|
操作 危害 |
使用 错误 |
未按照说明书中操作方法使用;在申请人规定的使用环境条件外使用产品;液箱、治疗机管路等未按说明书要求及时清洗消毒 |
设备运行异常或不能工作;产品寿命降低;影响治疗效果;造成患者作用部位损伤 |
三、肠道水疗机性能研究实验要求
1、主要技术指标
不同的肠道水疗机其参数根据设计要求会有所区别。下面列出此类产品可能涉及的重要性能参数,开发人可根据自身产品的技术特点制定性能指标的具体要求。若产品具有其他部件或功能,应符合相应国家标准和行业标准要求。
液箱(液袋)容积;
液体控温范围;
泵注液速度;
灌注量及灌注误差;
灌注压力及误差;
排泄压力及误差;
治疗时间;
液路系统密封性;
水处理装置(若有);
噪声;
连续工作时间。
直肠管:如为自制产品,应参考YY 0488考虑抗弯曲性、拉伸性能、缩径、空气泄露等相关要求。如为外购产品,应购买已取得医疗器械注册证或备案凭证的产品。
报警:考虑报警的适用性,结合产品的设计,出现超温、超压、供电短时中断等风险时处理方式。
其他:产品具有的其他特定功能,应参考相应标准制定相应的性能,如床体的要求、急停功能等。应用软件应按照《医疗器械软件注册审查指导原则》的要求,明确软件的功能、使用限制、接口、访问控制、运行环境(若适用)、性能效率(若适用)等。
2、安全性能
电气安全应符合GB 9706.1、YY 9706.108的要求。
电磁兼容应符合YY 9706.102(YY 0505)的要求。
3、产品性能研究
开发人需要开展产品性能研究,明确产品技术要求。需明确适用的标准或方法。关于适用标准中的不适用条款,需明确原因。
开发人需结合产品应用模式、运行模式、产品配置等,开展相应的测试验证。
明确液体的输送路径和工作原理,明确可以提供加热方式。明确速度、灌注和排泄压力、控温范围及精度的设定依据。若含有水处理装置,应明确水质相关要求。若含有直肠管,应详细描述尺寸、材质等。若含有床体,应明确是否可调,床体尺寸、锁止能力、承载能力等参数。
4、生物相容性研究
生物相容性评价根据GB/T 16886.1标准进行,应明确产品所用材料及其与人体接触的性质。生物相容性评价研究应明确实施或豁免生物学试验的理由,并对现有数据或试验结果进行评价。如实施生物学试验,应按照GB/T 16886.1标准开展相关研究,试验项目至少应包含细胞毒性、致敏、刺激或皮内反应。
5、清洗消毒灭菌工艺研究
产品使用中,明确重复使用部件(如治疗机管路)推荐的清洁和消毒工艺(方法和参数)、工艺确定的依据并开展相关验证。
如消毒使用的方法容易出现残留,应开展研究明确残留物信息及采取的处理方法。
6、稳定性研究
可参考《有源医疗器械使用期限技术审查指导原则》要求,开展产品使用期限的研究。对于可更换/有限次重复使用的医疗器械(如治疗机管路),应单独分析或开展使用次数验证。
应开展产品的包装及包装完整性研究,并参照GB/T 14710开展产品环境试验的研究。开发人应结合声称的储运条件开展包装和环境试验研究,并论述研究设置的合理性。应在开发人所声称的储运条件下进行性能测试,证明运输和环境测试后产品能够保持其完整性和功能性。
7、软件研究
开发人依据《医疗器械软件注册审查指导原则》,开展软件研究。软件研究需要覆盖全部软件组件。通常肠道水疗机的软件安全性级别为中等。
产品若涉及医疗器械网络安全,开发人可以参照《医疗器械网络安全注册审查指导原则》开展网络安全研究。
8、其他
肠道水疗机属于列入《免于临床评价医疗器械目录》中的产品,开发人需当按照《列入免于临床评价医疗器械目录产品对比说明技术指导原则》,从基本原理、结构组成、性能、安全性、适用范围等方面,证明产品的安全有效性。产品与对比产品存在差异的,还应开展差异部分对安全有效性影响的分析研究。
表2 肠道水疗机免于临床评价描述
|
09-08-05 |
肠道水疗机 |
通常由主机、温度控制装置、压力(流量)控制系统、液箱、蠕动泵、注液管、排液管等组成。治疗时将液体灌注到肠道内,同时通过排液管将液体引流到体外。在医疗机构用于对结肠的清洗。 |
Ⅱ |

来源:嘉峪检测网


