您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-04-26 12:52
[摘要]目的:以该产品国外参比制剂为参考,研究盐酸小檗碱片的最佳处方工艺,运用紫外-可见分光光度法建立合适的体外溶出测定方法,评价自制品与国外参比制剂溶出曲线行为的相似性。方法:通过正交试验法筛选辅料的用量从而确定最佳处方工艺,并制备出盐酸小檗碱片;分别考察自制试验制剂盐酸小檗碱片和参比制剂体外溶出行为,并采用f2相似因子法来评价这两产品的相似性。结果:自制样品和参比制剂的相似因子 f2均大于50或15分钟溶出量大于85 %。结论:在这4种介质中,自制试验制剂与国外参比制剂溶出曲线的溶出行为相似,说明受试制剂的处方工艺合理,可为盐酸小檗碱片的质量一致性评价提供参考。
药品的质量和疗效与国人的健康息息相关,我国属于仿制药大国。仿制药一致性评价可以使仿制药在质量和疗效方面与原研药品一致,并取代在临床中的原研药品,确保人民用药的安全和有效,可以节约医疗费用,同时对提高我国医药行业的整体发展都具有极大意义。故仿制药的一致性评价是国家药品监督管理局自2013年以来的一项重要工作。在校药学专业的大大学学生寻生寻找开找开展仿展仿制药制药一致一致性评性评价的价的研究研究切入切入点点,,进进行科行科研研活活动的尝试和探索,锻炼学生的专业技能和实验操作技巧,提高对药物理化性质的认知,在巩固理论、实验技术的同时激发创新精神,培养对药学专业严谨的态度和学习热情。
盐酸小檗碱片是临床用于肠道感染、腹泻的抗菌药,也是止泻药类非处方药品。盐酸小檗碱俗称黄连素,为毛莨科植物黄连根茎中所含的一种主要生物碱,可由黄连、黄柏或三棵针中提取。本品口服后在胃肠道吸收迅速而完全,对痢疾杆菌、大肠杆菌引起的肠道感染非常有效,针对性强,副作用小,可以减少其他化学合成类抗生素的使用,从而减少细菌耐药性的产生。[1]《中国药典》2020年版将其收载为抗菌药,本研究采用经验证的溶出曲线测试方法,以相似因子f2为考察标准,对自制制剂进行了不同溶出介质的研究来测定评估内在质量差异。
1材料和方法
1.1 仪器
LEE104E104E//0022电电子分子分析天析天平平((梅特梅特勒勒--托利托利多仪多仪器上器上海有海有限公限公司),DHG-9123A恒温鼓风干燥箱(上海一恒科技有限公司), YK-160摇摆颗粒机(上海绿翊制药机械有限公司),FL-5沸腾制粒机(上海华发制药机械成套发展公司),ZP-9A旋转式压片机(山东潍坊北方制药机械有限公司),BG-5H高效包衣锅(浙江江南制药机械有限公司),ZB-1D智能崩解仪(上海精拓仪器有限公司),CS-2脆碎度测试仪(上海精拓仪器有限公司), ZRS-8G智能药物溶出仪(天津市新天光分析仪器技术有限公司),N4S紫外可见分光光度计(北京普析通用仪器有限责任公司),XPE205电子分析天平(梅特勒-托利多国际贸易(上海)有限公司),Agilent 1260高效液相色谱仪(美国安捷伦公司)。
1.2 试药和试
试验试剂:盐酸小檗碱(四川协力制药股份有限公司)、一水乳糖(上海华茂药业有限公司)、玉米淀粉(海盐六和药业有限公司公司))、、磷酸磷酸氢钙氢钙((湖湖州展望药州展望药业有限公业有限公司司))、、硬脂硬脂酸镁酸镁((海海盐六盐六和药业有限公司)、盐酸小檗碱片(大峰堂药品工业株式会社,规格:100mg),盐酸小檗碱片(自制,规格:100mg),盐酸小檗碱对照品(批号 110713-202015,中国食品药品检定研究院),盐酸、乙腈、三乙胺为色谱纯,1-庚烷磺酸钠、磷酸二氢钾等均为分析纯。
1.3 累积溶出度测定
根据国内外盐酸小檗碱制剂溶出曲线的测定方法,以及完整的方法学研究结果,确定溶出曲线测试条件:按照中国药典2020年版四部溶出度与释放度测定法第一法(0931)[2],采用0.1 mol/L盐酸溶液、pH 4.0醋酸盐溶液、pH6.8 磷酸盐溶液和水四种介质,进行溶出度试验,按照f 2相似因子法或15 min 溶出量应均大于85%进行判定。
1.4 UV 测定
参照紫外-可见分光光度法(通则 0401)[3-4],在263nm的波长处测定吸光度,按标准曲线计算盐酸小檗碱释放量。
1.5 处方和工艺筛选
1.5.1 原料药的药理化特性确认
本品为口服固体制剂,湿法制粒工艺中涉及到高温高湿条件,对可能影响制剂质量的原药特性进行确认,结合相关试验对本品溶解度、pKa、粒度分布等进行确认。
1.5.2 辅料选择
参考参比制剂说明书[5]、原辅料相容性试验及公司实际生产经验,确定采用稀释剂一水乳糖、稀释剂磷酸氢钙、稀释剂淀粉、崩解剂羧甲淀粉钠、粘合剂淀粉浆为主要辅料,并以参比制剂的溶出曲线作为评价指标晶型处方工艺筛选与考察。
1.5.3 制粒正交试验设计法
制粒工艺采用国内较为常用的一步法制粒工艺,即在沸腾干燥机中完成喷浆制粒和颗粒干燥的工艺。由于盐酸小檗碱水溶性较差,口服给药不易吸收,在处方用量摸索阶段,为确保片剂崩解速度和颗粒压片的流动性,需进行稀释剂、崩解剂、粘合剂用量的三者关系的考察。具体操作按照正交设计要求,拟定相应处方用量,采用一步制粒工艺进行制粒,获得合适的干颗粒,进行压片。
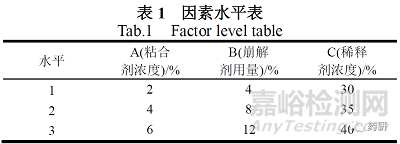
1.5.4 压片工艺
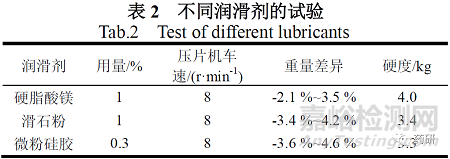
在盐酸小檗碱片成型工艺研究过程中,对目前常用的润滑剂如硬脂酸镁、滑石粉和微粉硅分别进行了相关指标的考察。选用不同润滑剂进行压片工艺研究,考察其对压片速度、硬度和重量差异的影响。见表2。
按照筛选优化的处方量将主药和辅料过100目筛,于沸腾干燥机中混合均匀后,以适量的4%淀粉浆作为粘合剂喷浆,在60.0 ℃下制粒并干燥,取出整粒,加1%硬脂酸镁,混合均匀后,用冲模为6.0mm浅凹冲的旋转式压片机制成约0.17g的素片。
1.5.5 片剂包衣工艺研究
盐酸小檗碱片因自身的溶解性差,在制粒时就有明显的成形困难,压片时因可压片也不强,所以如果压力调节不当,就会造成素片裂片、卷边和脆碎度不合格等现象。同时,为了和原研制剂尽可能保持一致。故在素片压制结束后,需要进行包衣。本研究采用市场上常见的薄膜包衣工艺。
薄膜包衣材料与溶剂的选择。将本品制成薄膜包衣片,按2020年版《中华人民共和国药典》中的相关规定,盐酸小檗碱片的崩解时限为30min,以薄膜包衣后不影响片重差异和崩解时限为重要考察指标。基于上述两个主要制剂通则的检查因素,选择羟丙甲纤维素为包衣主要成分,在长期试验中发现,如果选用较高浓度乙醇为溶剂,即不利于试验安全也对包衣材料羟丙甲纤维素的溶解度不佳,有时还导致包衣薄膜表面粗糙等。薄膜衣液的溶剂为30%乙醇溶液,薄膜衣材为羟丙甲纤维素,薄膜衣浓度控制在15.6%。
片剂包衣操作。①包衣操作。预热过程:将盐酸小檗碱片片芯倒入高效包衣锅内,设定转速6.0r/min,进风温度设置40.0~45.0℃,设定进风风速2000~2800r/min,锅内负压设置为-2.0Pa,开始预热,包衣锅内温度控制在38.0℃,开始喷浆。②成膜过程。设定转速6.0~7.0r/min,进风温度为48.0~55.0℃,保持包衣锅温度30.0~33.0℃,保持进风风速2000~2800r/min,进行包衣,总时长控制在1.5~2.0h。
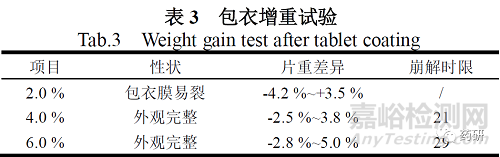
为确定本品最佳包衣增重范围,考察样品的性状、片重差异和崩解时限的变化情况。试验结果显示,包衣增重2.0%的样品,片剂包衣膜易不完整、有开裂,性状不合格;增重4.0%的样品性状、片重差异、崩解时限合格;增重6.0%的样品性状合格,片重差异也合格但崩解时限有延长表现。综合上述情况,确定包衣增重量为素片的4%,见表3。
2结果
2.1 处方和工艺筛选
2.1.1 原料药的理化特性确认
盐酸小檗碱BCS分类为Ⅱ类或Ⅳ类,其pKa为11.50,在水中略溶解,在pH1.0~8.0 范围内其溶解度为0.14~3.5mg/mL,具pH值依赖性。按最大规格100mg计算,属于低溶解性药物。基于相关试验及特性,盐酸小檗碱原料药需微粉化处理。
2.1.2 辅料选择
水乳糖、磷酸氢钙和玉米淀粉在本品中用作稀释剂可保证片剂的可压性;羧甲淀粉钠作为崩解剂利用其吸水膨胀力,瓦解片剂颗粒间的结合力;淀粉浆作为国内制剂常用的粘合剂,可避免因粘合性过大所致的崩解缓慢的情况。硬脂酸镁作为助流剂使用,其用量控制在1.0%左右,在满足颗粒流动性的同时,避免影响产品的溶出速率。
2.1.3 制粒正交试验
为确保片剂崩解速度和颗粒压片的流动性,需进行稀释剂、崩解剂、粘合剂用量的三者关系的考察。具体操作按照正交设计要求,拟定相应处方用量,采用一步制粒工艺进行制粒,获得合适的干颗粒,进行压片和溶出曲线测试。
按照正交试验设计表称取原辅料,制成片剂后考察在0.1mol/L盐酸溶液中的溶出行为,以原研制剂的溶出度为参比,对样品进行溶出行为的相似因子f2计算。正交试验结果进行直观分析与方差分析,结果见表4、表5。结果R 值越大,该因素的影响越大,由表3、可知,三因素的影响强度为B>A>C。
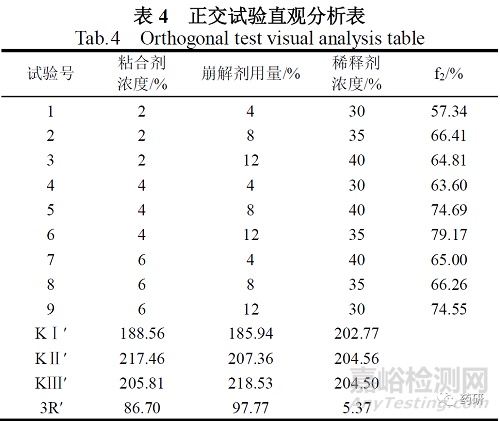
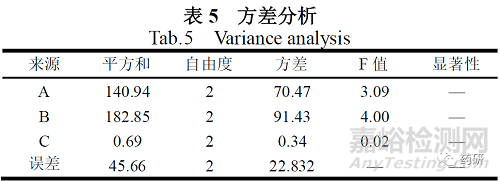
综合上述试验结果,确定最佳用量考察为A2B3C2,即淀粉浆浓度4%、羧甲淀粉钠用量12%、一水乳糖35%。确定的新工艺采用一步制粒法,进行制备三批样品( 批号为YX101001、YX101002、YX101003),依据拟定的质量标准要求,对原处方工艺和新处方工艺质量评价结果见下表6:
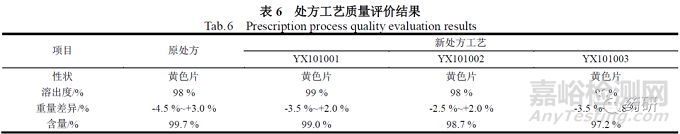
2.2 自制制剂和参比制剂的溶出曲线比较
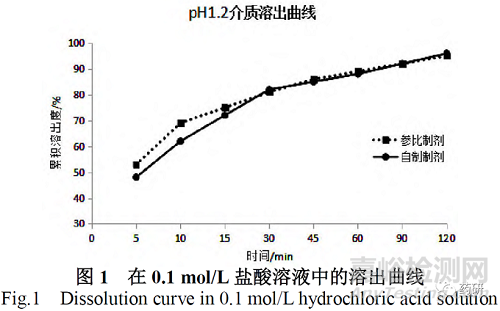
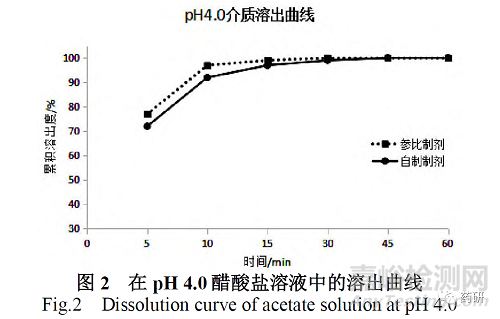
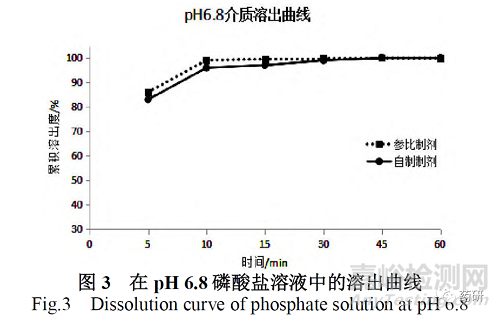
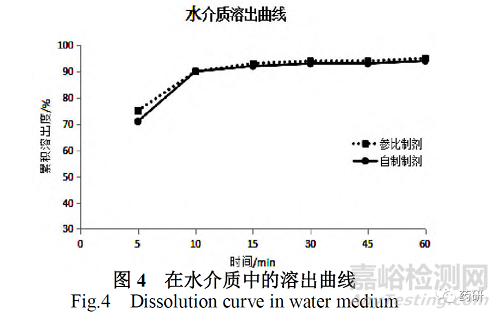
根据国内外盐酸小檗碱制剂溶出曲线的测定方法[9-11],以及完整的方法学研究结果,确定溶出曲线测试条件:按照中国药典2020年版四部溶出度与释放度测定法第一法(0931)[11],采用0.1mol/L 盐酸溶液、pH4.0醋酸盐溶液、pH6.8磷酸盐溶液和水四种介质,进行溶出度试验(见图1,图2,图3、图4),其中pH4.0醋酸盐溶液、pH6.8磷酸盐溶液和水三种介质,按照15 min 溶出量均大于85%,0.1mol/L 盐酸溶液采用f2相似因子大于50。根据CDE发布的《普通口服固体制剂溶出度试验技术指导原则》要求,判定自制制剂和参比制剂体外溶出行为相似。
3讨论
由于盐酸小檗碱属于难溶性药物,原料必须经过微粉化处理,增加药物的比表面积,增大药物的溶出速率。但经试验证明,仅通过微粉化增加溶出速率仍不理想。在制剂处方工艺摸索过程中,采用增加吸水膨胀力强的崩解剂大大改善了产品的溶出量,优化后的处方和制备工艺,从根本上改变了原处方工艺产品的溶出行为,使自制制剂与国外参比制剂溶出曲线溶出行为相似,说明受试制剂的处方工艺合理,可为盐酸小檗碱片的质量一致性评价提供参考。

来源:Internet


