您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-03-04 09:13
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
印度太阳药业抗癌药获得国内优先审评。太阳药业引进品种磷酸索尼德吉胶囊的新药上市申请获CDE拟纳入优先审评,适用于手术或放疗后复发的局部晚期基底细胞癌(BCC)的成年患者,或不宜手术或放疗的患者。磷酸索尼德吉(sonidegib phosphate,Odomzo)是诺华研发的一种口服选择性SMO抑制剂,已于2015年获FDA批准上述适应症。太阳药业拥有该药的全球权益。
国内药讯
1.智飞新冠疫苗在乌兹别克斯坦获紧急使用授权。中科院微生所与智飞龙科马生物共同研发的重组新冠病毒疫苗(CHO 细胞)在乌兹别克斯坦国获紧急使用授权。去年12月,该疫苗在这一国家启动了Ⅲ期试验,来自近7000名志愿者参与的临床研究结果显示,这款疫苗安全有效。乌兹别克斯坦卫生部2日报告新增新冠确诊病例35例,累计确诊79961例,累计死亡622例,累计治愈78513例。
2.三个用于治疗新冠肺炎的中药颗粒制剂获批上市。3月2日,国家药监局通过特别审批程序应急批准了中国中医科学院中医临床基础医学研究所的清肺排毒颗粒、广东一方制药的化湿败毒颗粒、山东步长制药的宣肺败毒颗粒上市。这三个中药颗粒制剂是新冠疫情爆发以来,在武汉抗疫临床一线众多院士专家筛选出有效方药清肺排毒汤、化湿败毒方、宣肺败毒方的成果转化,也是首次按照《中药注册分类及申报资料要求》(2020年第68号)“3.2类 其他来源于古代经典名方的中药复方制剂”审评审批的品种。
3.艾力斯甲磺酸伏美替尼获批上市。艾力斯医药第三代EGFR-TKI甲磺酸伏美替尼获NMPA批准上市,用于治疗EGFR T790M突变阳性的局部晚期或转移性非小细胞肺癌(NSCLC)。在一项IIb期ALSC003 研究中,伏美替尼在既往接受一/二代EGFR TKI治疗后进展或初治T790M突变NSCLC中的ORR达到73.6%,预估6周和12周DCR率为87.3%和82.3%,中位PFS为7.6个月,中位OS和 DoR均未达到。截止目前,国内已有3款第三代EGFR-TKI获批上市。
4.辉瑞BRAF抑制剂获批中国临床。辉瑞BRAF抑制剂encorafenib硬胶囊获CDE一项临床试验默示许可,拟开发治疗结直肠癌。encorafenib是辉瑞通过114亿美元收购Array Biopharma所得,该药已获FDA批准治疗携带BRAF V600E突变的转移性结直肠癌成人患者。在一项Ⅲ期临床BEACON CRC中,encorafenib联合西妥昔单抗在这类患者中的中位总生存期为8.4个月,高于对照组的5.4个月;此外,联合疗法组患者的客观缓解率为20%,而对照组只有2%。
5.贝达药业PI3Kα抑制剂获批临床。贝达药业1类新药BPI-21668片获CDE临床试验默认许可,拟开发用于晚期实体瘤(如乳腺癌、非小细胞肺癌、胃食管癌、卵巢癌等)的治疗。BPI-21668是一种新型口服小分子PI3Kα抑制剂,目前国内尚无同类品种获批上市。全球范围内只有2款PI3Kα选择性抑制剂获批上市,分别为拜耳的copanlisib和诺华的alpelisib。alpelisib首个获批用于乳腺癌治疗的药物,2020年全球销售额达3.2亿美元。
6.再鼎2020年财报:尼拉帕利收入2.2亿元。3月1日,再鼎公布2020年财务业绩报告。全年收入为4900万美元,较2019年增长277%;2020年研发费用开支为2.227亿美元,较2019年增长56.6%;产品销售方面,核心产品则乐(尼拉帕利)报告期内销售收入为3210万美元,爱普盾(肿瘤电场治疗仪)销售收入为1640万美元。
国际药讯
1. 阿斯利康新冠疫苗真实世界数据首次公布。英国公共卫生部首次公布了阿斯利康和牛津大学联合开发的新冠疫苗ChAdOx1(AZD1222)真实世界的预防效力数据。来自今年1月4日后70岁以上老年群体的数据显示,接种一剂疫苗14天后,患上COVID-19的风险开始降低;接种35天后,疫苗的保护效力达到73%。由于随访时间较短,尚未有足够的数据显示ChAdOx1的保护效力是否达到平台期,以及一次接种的保护效力持续的时间。
2.诺华司库奇尤单抗获欧盟批准标签更新。欧洲药品管理局人用医药产品委员会(CHMP)批准诺华抗炎药司库奇尤单抗(Cosentyx)II类标签变更,纳入来自同类首个MAXIMISE试验的银屑病关节炎(PsA)轴向表现数据。有轴向表现的PsA患者,疾病负担更高,疼痛、疲劳、晨僵、身体功能受损、附着点计数增加和炎症标记物水平更高。目前,Cosentyx已获批的适应症为:斑块型银屑病、银屑病关节炎、强直性脊柱炎、放射学阴性中轴型脊柱关节炎(nr-axSpA)。2020年,Cosentyx销售额达39.95亿美元,位居诺华产品销售榜首。
3.辉瑞长效生长激素申报欧盟上市。OPKO公司/辉瑞长效人生长激素somatrogon的营销授权申请(MAA)获欧洲药品管理局(EMA)受理,用于每周注射一次治疗生长激素缺乏症(GHD)儿科患者。欧盟委员会预计将在2022年作出审查决定。在一项全球Ⅲ期试验中,与每日注射一次Genotropin相比,每周注射一次somatrogon在年身高生长速度(height velocity)方面疗效具有可比性。somatrogon目前也正在接受FDA的审查,PDUFA目标日期为2021年10月。
4.安进公布双抗药物Ⅲ期临床总结报告。安进CD19/CD3双抗Blincyto(blinatumomab)治疗首次复发的高危B细胞前体急性淋巴细胞白血病(B-ALL)儿童患者的Ⅲ期临床结果在《美国医学会杂志》上发布。与巩固化疗相比,Blincyto显著延长患者的无事件生存期。在中位随访时间为22.4个月时,两组维持无事件生存的患者比例分别为69%和43%。此外,接受Blincyto治疗后,基线时最小残余病(MRD)阳性患者中93%达到MRD阴性缓解,化疗组这一数值为24%。
5.创新精准疗法公司FogPharma完成C轮融资。FogPharma宣布完成数额为1.07亿美元的C轮融资。FogPharma公司专有Helicon多肽药物开发平台整合了定向进化、螺旋超稳定化学、人工智能、基于结构的药物发现等技术,能够迅速针对此前无法成药的靶点开发出多肽候选药物。募集的资金将用于推进潜在“first-in-class” β-连环蛋白(β-catenin)拮抗剂进入临床开发阶段,并且促进其Helicon技术平台开发一系列靶向“不可成药“靶点的候选药物。
6.基因编辑公司eGenesis完成C轮融资。由麻省理工学院(MIT)的George Church教授和杨璐菡博士联合创建的eGenesis公司宣布,已完成1.25亿美元的C轮融资。eGenesis公司旨在通过对猪的器官进行基因编辑,以使其满足安全成功移植到人体内的要求,以解决全球器官短缺问题。获得资金将用于促进该公司在肾脏和胰岛细胞移植方面的主打研发项目进入人类概念验证研究,以及其基因编辑平台的持续开发和扩展GMP生产规模。
医药热点
1.上海新规:医闹失信者或被限制招为公务员。3月1日,国内首部专门保护医护人员权益的省级政府规章——《上海市医疗卫生人员权益保障办法》正式实施。该《办法》从职业和社会权益保障、执业环境保障、涉医失信行为的联合惩戒等多个章节,较为全面地提出了保护医疗卫生人员的措施。在联合惩戒方面,对于重度失信者,行政机关还可以在一定期限内限制其使用医保就医,限制招录为公务员或者事业单位工作人员。
2.教育部撤销4所高校临床医学七年制专业。3月1日,教育部官网发布《教育部关于公布2020年度普通高等学校本科专业备案和审批结果的通知》,宣布撤销518个高校本科专业。其中,南开大学临床医学七年制、山东大学齐鲁医学院临床医学七年制和口腔医学七年制、中南大学湘雅医学院临床医学七年制和广西医科大学临床医学七年制均被撤销。
3.北京新冠疫苗累计接种突破500万人。北京市通报,自今年1月1日全面启动9类重点人群新冠疫苗接种,截至3月2日14时,全市累计接种765万剂次,累计接种达500万人,其中264万人完成两个剂次接种。北京市将推进下一阶段疫苗接种工作,围绕感染高风险人群、维持社会基本运行人群、基本生活物资供应保障关键岗位人群及服务业和劳动密集型行业从业人员等疾病传播风险较高人群接种疫苗,实现重点人员“应接尽接”。
4.中国医疗器械行业年均增长率20%。德勤3月1日发布《中国医疗器械行业:企业如何在日趋激烈的市场竞争中蓬勃发展?》白皮书。根据白皮书,中国医疗器械2020年市场规模预估为8000亿元人民币,比2015年的市场规模翻倍;自2015年以来,该行业保持年均20%左右的增长,近几年的增速超越GDP的增速;中国医疗器械对外贸易每年增速为10%,超过了全球医疗器械贸易的平均增长速度。
审评动向
1. CDE新药受理情况(03月03日)
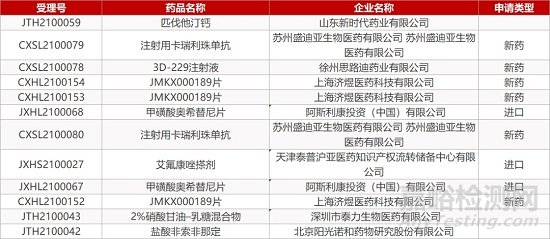
2. FDA新药获批情况(北美03月1日)
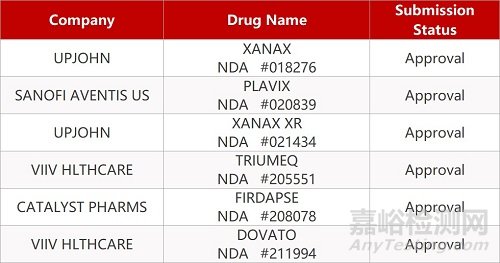
股市资讯
【艾力斯】公司近日从国家药监局网站查询获悉,公司提交的伏美替尼药品注册申请办理状态已变更为“审批完毕-待制证”阶段,并已取得药品批准文号。伏美替尼是目前公司的核心产品,主要用于表皮生长因子受体(EGFR)敏感突变、EGFR T790M耐药突变的晚期非小细胞肺癌治疗。
【中国医药】公司子公司科益药业近日收到国家药监局核准签发的盐酸伐昔洛韦片《药品补充申请批准通知书》,该药品主要用于治疗带状疱疹,适用于治疗单纯疱疹病毒感染、预防(抑制)单纯疱疹病毒感染的复发。
【君实生物】公司子公司TopAlliance近日向FDA滚动提交了特瑞普利单抗用于治疗复发或转移性鼻咽癌的生物制品许可申请。

来源:药研发


