前言
有水就有生命,有水就有生化反应,水也是引起产品降解从而导致保质期缩短的主要因素之一;
冷冻干燥是一个在很低的温度下通过升华和解吸附的方式去除产品中水分的过程;
残余水分和顶空残氧量是两个促进产品降解的常见因素,会引起产品的稳定性变化从而导致产品保质期不足;
冷冻干燥可以很好的同时解决这两个问题;
药物分子在冻干状态下保持稳定的机理是:形成了具有低分子流动性和低反应活性的高粘度无定形玻璃态;
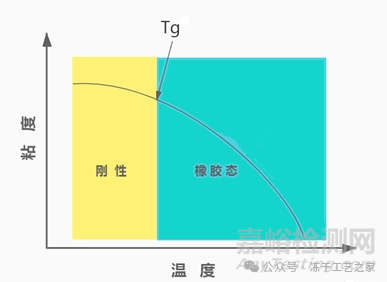
玻璃态/无定形态的临界点是玻璃转化温度(Tg):将冻干产品暴露在高于其玻璃转化温度(Tg)的温度下,粘稠的玻璃态将转化为粘稠度较低的 "橡胶 "态(如图一),其热容量、分子流动性和反应性都会增加,从而稳定性降低;
图一:Tg、粘度、温度之间的关系图
冻干产品的温度超过 Tg 值还会有反玻璃化的风险:即某些可结晶的辅料会发生结晶,从而进一步影响产品的稳定性;
冻干产品的 Tg 值的确定对设计加速稳定性研究非常重要。因为在高于 Tg 值的温度下生成的加速稳定性数据无法预测在较低储存温度下产品的行为,也不能由此来估计产品的保质期;
建议在至少低于产品Tg 10℃的条件下,进行产品的稳定性研究。
* Chang 等人报告说,当 IL-2 的储存温度高于其 Tg 值时,其脱氨率和聚集率更高;
Strickley等人报道,随着储存温度的升高:接近或超过Tg值时,胰岛素的聚集速率会增加,即使在玻璃状态下也会发生脱酰胺;
其他研究小组报告显示,Tg对酶活性的稳定性没有太大影响。
冻干粉饼的水分含量和Tg又有什么关系呢?
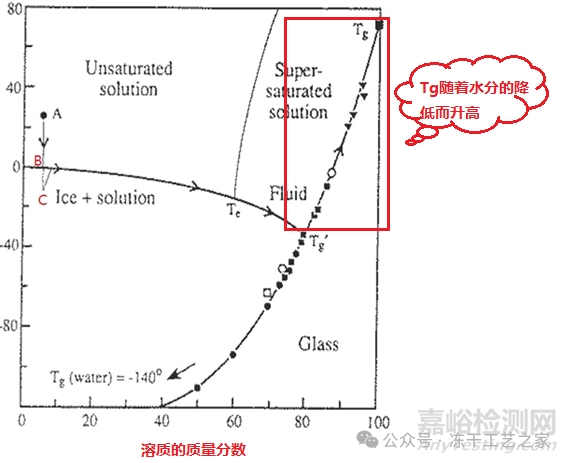
冻干粉饼的Tg随着其水分含量的升高而降低:大概水分每增加1%,则产品的Tg降低10℃(此数据仅为一个大概的数据,用户帮助大家理解Tg和粉饼水分之间的关系)
图二红色框内部分也表达了两者之间的关系:
图二:冷冻干燥过程中的相图
为了提高产品存储的稳定性,需要将冻干后产品的水分降到一个很低的数值;
对于每个产品来说,降低到多低的数值:小于<2%、1%,还是3%?根据产品分子的不同,这个标准都会不同;
很多同学私信问我:冻干产品是否有一个统一的水分标准,是否是越低越好,还有同学说他们产品水分必须要达到0.5%以下才能保持稳定性如何才能做到?
但很遗憾,这些问题都没有办法用一句话来回答,并不存在统一的标准答案;
对于每一种冻干产品:都需要通过系统的水分研究来评估残余水分含量对产品质量属性的影响。这项研究的结果将为产品残余水分标准的设计提供依据。
有两种方法可以用于研究冻干产品的最终水分标准,本篇文章将会详细介绍这两种研究方法。
方法 一:水分吸附等温线
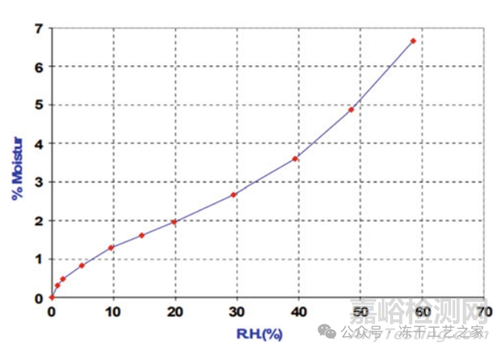
为配方/产品最初建立的吸湿等温线如图 3 所示;
水分吸附等温线将水活性(αw)与相应的冻干材料联系起来,每种材料和温度对应的等温线都是唯一的;
图三:25 °C 时蛋白质配方的吸附等温线
吸湿等温线通常使用吸附微天平以重力法获得;
要获得吸湿等温线,需要将初始干燥的样品置于相对湿度(RH)不断增加的环境中,通常最高可达 70% RH;
在每个水活度水平上,连续测量样品的重量,直到观察到平衡为止。
理论上,当样品的重量随时间保持不变时,平衡就建立了。不过,在实践中,当样品重量在预定时间内的变化足够小时,就可以认为样品处于平衡状态。
在较高的相对湿度下,配方中的某些成分/辅料可能会结晶,这一点可从水分的解吸中看出来;
某些辅料的结晶可通过偏光显微镜来确定,如图 4 所示,回收的样品会出现双折射;
通过粉末X射线衍射可以确认结晶。
图四:偏光显微镜观察从吸附微天平上回收的样品,显示某些配方成分结晶 成分结晶可通过粉末 X 射线 衍射
水分平衡
一旦建立了吸附等温线,就可以通过两种方法来研究在不影响产品稳定性的情况下,产品中可以残留的最大水分含量;
一种方法是在不同的相对湿度下平衡冻干的蛋糕,以获得不同水平的残余水分含量;
不同的相对湿度可通过不同浓度的 NaOH 溶液(见表一)来实现;
|
NaOH 溶液测得 |
R.H (%) |
预期含水量 |
测量的含水量 |
|
水分含量(%) |
|
(%) |
|
|
(%) |
|
|
浓度(摩尔) |
_ |
_ |
干燥 |
卡尔费休滴定法 |
|
|
|
失重法 |
|
23.05 |
11 |
13 |
1.7 |
1.7 |
|
14.96 |
25 |
2.4 |
3,1 |
2,8 |
|
12.53 |
35 |
3.2 |
3.8 |
3.5 |
|
10.64 |
45 |
4.3 |
4.9 |
4.8 |
表一:氢氧化钠盐浓度可实现不同的湿度
或使用不同盐类的饱和溶液来提供不同的相对湿度,如表二 所示;
|
盐溶液 |
Control |
LiCI |
LiI |
MgCI2 |
Mg(NO3)2 |
|
% 相对湿度 (RH) |
N/A |
11 |
18 |
33 |
53 |
|
% 西林瓶中样品水分 |
0.6 |
1.2 |
1.6 |
2,7 |
4.2 |
表二:环境相对湿度VS样品水分
样品在这些溶液中在真空条件下平衡一夜, 过夜平衡后的样品含水是用干燥失重法法和卡尔费休滴定法测量,结果见表一。
这些不同的残余含水量的样品在加速(37 °C)条件下放置3 个月;
在建议的储存条件下(2°C 至 8°C)放置 2-3 年;
根据这些数据,确定冻干产品的最终残余水份指标,并在最终产品的放行实验中执行;
样品准备
▪ 将装有饱和盐溶液的培养皿连同湿度计一起放入干燥器或手套箱中,让其过夜平衡;
▪ 如果使用手套/干燥箱,则用氮气吹扫干燥箱,直到相对湿度低于盐溶液的预期水平;
▪ 将西林瓶放入干燥箱或手套箱中,在箱内或干燥箱中打开胶塞并关闭干燥箱门;
▪ 在 t = 0、t = 24 小时和 t = 48 小时时取出样品瓶,用卡尔费休法测定水分含量。
卡尔费休水分分析法
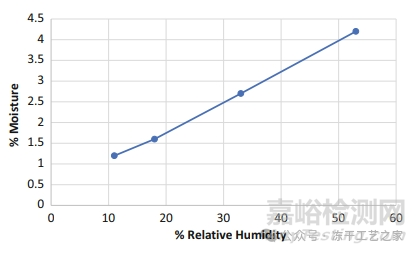
表 二 和图 五 总结了卡尔费休法测量的暴露于不同相对湿度百分比后的含水量;
图 五 平均残余水分值与相对湿度百分比的关系
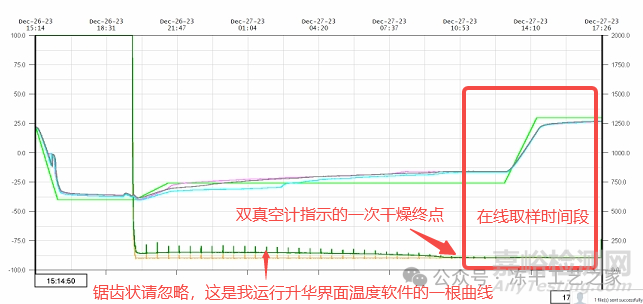
方法 二:冻干机在线取样法
在冻干工艺运行过程中,不断地取出样品;
在这种方法中,当一次干燥达到终点的时候(当皮拉尼压力计与电容压力计(CM)的压力趋于一致时),从不同位置用冻干机配备的在线取样装置取出西林瓶;
图六:在线取样时间段标示图
一次干燥到二次干燥升温的斜坡阶段,二次干燥温度保持阶段每隔1-3小时,用在线取样装置从冻干机中取出西林瓶并在取样之后压塞;
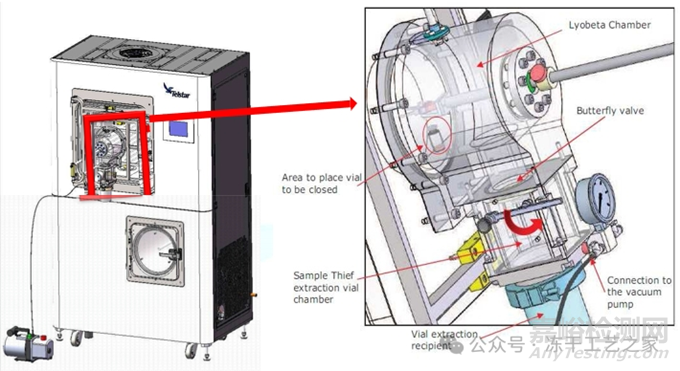
图七:冻干机上在线取样装置工作示意图
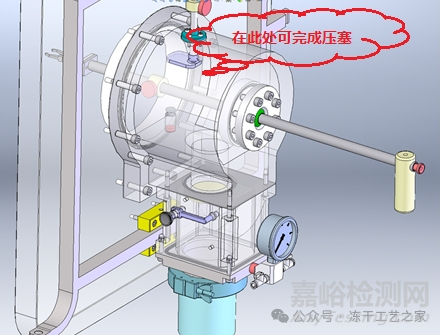
图八:取样后进行压盖示意图
图九:在线取样装置实物图
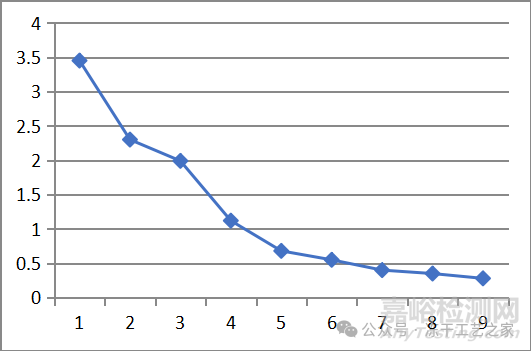
一次干燥结束后,一次干燥到二次干燥的升温阶段,二次干燥的温度保持阶段,样品中的残余水分不断减少,如图十:
图十:在线取样样品水分变化示意图
(初始水分根据产品的不同而不同,我示范的这个数据初始水分偏低不少)
不同时间段取出的样品,残余水份也都不同;
这些不同的残余含水量的样品在加速(37 °C)条件下放置3 个月;
在建议的储存条件下(2°C 至 8°C)放置 2-3 年;
根据这些数据,确定冻干产品的最终残余水份指标,并在最终产品的放行实验中执行;
注释:
产品装量规格
▪ 在选择西林瓶胶塞和最终产品的装量规格时必须谨慎;
▪ 需要注意当装量减小或西林瓶和瓶塞尺寸增大时,在 2 年保质期内有可能出现冻干粉饼水份超标的情况;
▪ 西林瓶和胶塞的尺寸增大时,在 2 年保质期内残余水份超标的风险就会大大增加;
▪ 当粉饼质量减少时,残余水份超过在2年保质期内超标的风险也会大大增加如表三;
|
特征 |
产品A |
产品B |
|
产品水分限度 |
2% |
|
蛋糕重量 |
500mg |
50mg |
|
胶塞重量 |
2.5gm |
|
胶塞水分 |
0.2% = 5 mg |
|
潜在产品水分 |
1% |
10% |
表三 减少灌装干物质质量导致水分指标不合格的风险说明
*胶塞水分迁移是影响产品水分的一个重要因素,此篇主要讲冻干产品水分指标的确定方法,胶塞水分迁移的原理和解决方案以后再单独开一篇来讲吧。
最后的话
冻干产品的最终水分没有一个统一的标准;
每个产品用一套确定水分标准的研究方法来确定一个这个产品需要符合的水分放行标准;
在实践中,我们看见有些产品的水分合格标准是低于2%、有些是低于1%,有些将3%作为放行标准也完全没问题。关键是你对于这个问题进行过系统的研究,有足够的数据作为支持;
实践中大家的水分标准常常是从同类产品的标准“借鉴“来的,有些同学因为这个问题收到了来自监管部门的“挑战”;
如果在制定标准的过程中,遵循科学的方法,积累了足够的数据,这个“挑战”可能更可以是一个证明我们研究过程严谨的“机会”;
参考文献:
1.Feroz Jameel Design of Moisture Specification Studies for Lyophilized Product
2. Pikal MJ. Mechanisms of protein stabilization during freeze drying and storage: the relative importance of thermodynamic stabilization and glassy state relaxation dynamics. In: Rey L, May J, editors. Freeze drying/lyophilization of pharmaceutical freeze drying 1831d biological products. Marcel, Dekker, Inc.; 1993. 2. Carpenter JR,
3. Pikal MJ, Rigsbee D, Roy ML, Galreath D, Kovach KJ, Wang W, Carpenter JF, Cicerone MT. Solid state chemistry of proteins: II. The correlation of storage stability of freeze-dried human growth hormone (hGH) with structure and dynamics in the glassy solid. J Pharm Sci. 2008;97(12):5106–21.
4. Chang BS, Beauvais RM, Dong AC, Carpenter JF. Physical factors affecting the storage stability of freeze-dried interleukin-1 receptor antagonist—glass transition and protein conformation. Arch Biochem Biophys. 1996;331:249–58.
5. Mazzobre MF, Buera MD, Chirife J. Glass transition and thermal stability of lactase in low-moisture amorphous polymeric matrices. Biotechnol Prog. 1997;13:195–9