今日头条
正大天晴PI3Kα/δ双重抑制剂报产。正大天晴1类化药TQ-B3525片的上市申请获CDE受理,推测适应症为既往至少二线治疗失败的复发/难治滤泡性淋巴瘤(FL)。TQ-B3525是一款新型PI3Kα/δ双重抑制剂,它既可以克服单独抑制PI3Kδ亚基时引起的PI3Kα亚基活性上调导致的耐药问题,同时较之PI3K泛抑制剂又显著降低了毒副作用。目前,该新药正在国内开展多项临床研究,适应症包括FL、套细胞淋巴瘤和弥漫性大B细胞淋巴瘤等。
国内药讯
1.珐博进HIF抑制剂肿瘤贫血III期临床成功。珐博进与阿斯利康联合开发的口服HIF-PH抑制剂罗沙司他(roxadustat)用于正在接受化疗的非髓系恶性肿瘤患者治疗贫血的中国III期临床达到主要研究终点。与重组人促红素α (SEPO®)相比,罗沙司他治疗组患者第9-13周平均Hb水平较基线的平均变化达到非劣效性标准。罗沙司他的不良事件概况与先前的研究结果基本一致,两家公司计划尽快提交该新药的补充新药申请。
2.唯源立康HSV基因药物DEB临床积极。北京唯源立康宣布其基于专有I型单纯疱疹病毒(HSV-1)载体平台开发的基因药物WG1025凝胶制剂,在研究者发起、针对营养不良型表皮松解症(DEB)治疗的临床研究中获积极结果。WG1025含有两个拷贝全长COL7A1基因的复制缺陷型HSV-1载体,可以在皮肤细胞持续表达功能性VII型胶原蛋白并促进创口愈合。数据显示WG1025局部给药后创口完全愈合时间为5-10天,中位时间为7.5天;药物总体耐受性良好。
3.恒瑞两款自免病新药获批临床。恒瑞医药两款1类生物制品(注射用SHR-2001和SHR-1654注射液)分别获得国家药监局临床试验默示许可。SHR-2001是一款抗体-细胞因子融合蛋白,拟开发用于治疗系统性红斑狼疮(SLE)等自身免疫性疾病;SHR-1654也是恒瑞医药自主研发,临床皮下注射给药,拟开发用于治疗类风湿关节炎。
4.华东医药三靶点降糖药中国报IND。华东医药旗下道尔生物1类生物制品“注射用DR10624”的临床试验申请获CDE受理。DR10624是一款潜在“first-in-class”同时靶向GLP-1R、GCGR和FGF21R的的长效(临床拟每周使用一次)三靶点激动剂,潜在的适应症为糖尿病、肥胖症、非酒精性脂肪性肝病(NAFLD)、非酒精性脂肪性肝炎(NASH)等。今年4月,该新药已在新西兰获批开展Ⅰ期临床试验。
5.安斯泰来KRAS G12D降解剂中国报IND。安斯泰来1类化药ASP3082注射液的临床试验申请获CDE受理。ASP3082是一款高效选择性KRAS G12D蛋白降解剂(PROTAC),能够有效降解KRAS G12D蛋白,对细胞外信号调节激酶磷酸化及其下游基因具有显著的抑制作用。在携带KRAS G12D突变的多种异种移植小鼠模型中,ASP3082已显现出广泛的抗肿瘤活性;而且安全性良好。
国际药讯
1.艾伯维JAK抑制剂获批治疗克罗恩病。FDA批准艾伯维口服JAK抑制剂Rinvoq(upadacitinib,乌帕替尼)新适应症,用于治疗对一种或多种TNF阻断剂反应不足或不耐受的中重度活动性克罗恩病(CD)成人患者。在两项诱导研究(U-EXCEED和U-EXCEL)以及维持研究U-ENDURE中,Rinvoq治疗组患者达到临床缓解与内镜缓解的比例显著更多。这是upadacitinib在风湿病学、皮肤病学和胃肠病学领域获得FDA批准的第7个适应症。
2.度普利尤单抗COPD临床研究见刊NEJM。赛诺菲与再生元联合开发的IL-4/IL-13抑制剂度普利尤单抗(dupilumab,Dupixent)治疗慢性阻塞性肺疾病(COPD)的Ⅲ期临床(BOREAS)积极结果发表在《新英格兰医学杂志》(NEJM)上。与安慰剂相比,度普利尤单抗联合三联疗法治疗52周后显著减少30%的疾病恶化;患者12周和52周时肺功能较基线分别改善160mL(vs77mL,p<0.0001)和153mL(vs70mL,p=0.0003);药物的安全性结果与已知研究一致。
3.诺和诺德长效胰岛素临床见刊柳叶刀子刊。诺和诺德每周1次胰岛素Icodec用于治疗2型糖尿病的Ⅲa期ONWARDS 2试验26周治疗结果发表在The Lancet Diabetes & Endocrinology期刊上。与每日一次德谷胰岛素治疗相比,每周一次icodec治疗具有非劣效性(p<0.0001)和优效性(p=0.0028),两组患者糖化血红蛋白(HbA1c)水平分别较基线降低0.97%和0.68%。icodec组患者体重平均增加1.40kg(vs减少0.30kg)。研究中未发现与icodec相关的新的安全性问题。
4.武田新型ADAMTS13重组蛋白获优先审评。武田ADAMTS13酶替代疗法TAK-755治疗先天性血栓性血小板减少性紫癜(cTTP)的生物制品许可申请(BLA)获FDA受理,并获授予优先审评资格。在Ⅲ期临床中,与基于血浆的疗法相比,TAK-755降低血小板减少事件的发生率60%(95% CI,30%-70%);与治疗相关的不良事件发生率也显著更底(8.9%与47.7%)。如果获批,它将成为首款针对cTTP的ADAMTS13酶替代疗法。
5.丙酸血症mRNA疗法早期临床积极。Moderna公司基于脂质纳米颗粒(LNP)递送技术开发的mRNA疗法mRNA-3927在ASGCT2023年会上公布治疗罕见病丙酸血症的I/II期临床(NCT04159103)积极结果。mRNA-3927旨在编码PCCA和PCCB亚基蛋白以恢复肝脏中功能性PCC酶活性。数据显示,1岁及以上丙酸血症患者共有16例患者在5个剂量组中接受mRNA-3927治疗后,患者的MDEs(代谢失衡事件)症状获得减轻或消失;药物总体耐受性良好。
6.奥贝胆酸治疗NASH未获FDA支持。FDA胃肠药物咨询委员会不推荐加速批准Intercept公司FXR激动剂奥贝胆酸(OCA)上市,用于治疗非酒精性脂肪性肝炎(NASH)引起的肝硬化前期伴有肝纤维化患者。专家们认为,奥贝胆酸在Ⅲ期临床(REGENERATE)中使用了替代终点,肝脏组织学的改善(22.4%vs9.6%,p<0.0001)只是2个主要终点之一,而且奥贝胆酸还有引起药物性肝损伤的风险。目前,这项试验正在进行中,以收集另一个主要终点全因死亡率和肝脏相关临床数据。
医药热点
1.熬夜致癌的原因被发现。近日,华盛顿州立大学的研究人员在" Journal of Pineal Research "期刊上发表的一项最新研究成果显示,夜班工作引起的昼夜节律紊乱可以改变肿瘤相关基因的表达,从而使一种基因更容易受到导致癌症的DNA损伤的影响。华盛顿州立大学睡眠与表现研究中心主任表示:“夜班工人面临着巨大的健康差异,从代谢和心血管疾病的风险增加到精神疾病和癌症。现在是时候为这些夜班工人找到诊断和治疗解决方案”。
2.广东省骨科疾病临床医学研究中心启动。5月20日,中山大学附属第八医院举行基础研究与临床转化研讨会,广东省骨科疾病临床医学研究中心正式启动。未来,该院将充分发挥省级临床医学研究中心的引领作用,加快构建具有粤港澳大湾区特色的骨科疾病防治体系,搭建国际一流的临床研究公共服务平台,为广东省科技攻关提供平台支持。
3.全国已组建家庭医生团队超42万个。19日,是第13个“世界家庭医生日”,主题是“签而有约 共享健康”。我国从2016年开始全面推行家庭医生签约服务,截至目前,全国已组建超过42万个家庭医生团队,为签约居民,特别是慢病患者、老年人等重点人群提供医疗卫生服务。国家卫健委要求,到2035年,家庭医生签约服务覆盖率将达到75%以上,基本实现家庭全覆盖。
评审动态
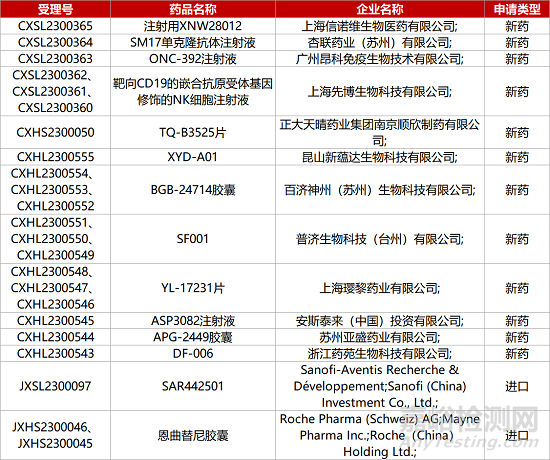
1. CDE新药受理情况(05月22日)
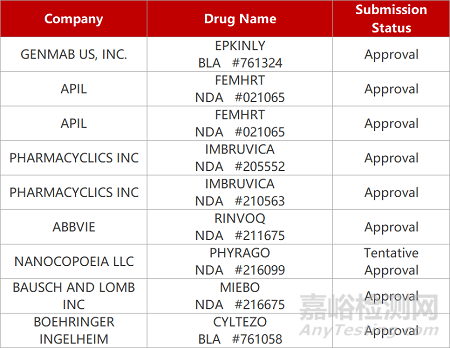
2. FDA新药获批情况(北美05月19日)