今日头条
济民可信小分子免疫激动剂获批临床。济民可信1类化药JMKX000197注射液获国家药监局临床默示许可,拟开发用于治疗恶性胸腔积液。JMKX000197是一款小分子免疫激动剂,可以诱导多种细胞因子的释放,引起炎症反应的同时可以激活体内的巨噬细胞,树突状细胞以及杀伤性T细胞,从而多种机制协调来达到治疗疾病的效果。
国内药讯
1.正大天晴PD-L1单抗启动肺癌Ⅲ期临床。正大天晴PD-L1单抗TQB2450登记启动一项Ⅲ期临床,拟评估TQB2450联合紫杉醇加卡铂后序贯TQB2450联合盐酸安罗替尼胶囊对比替雷利珠单抗联合紫杉醇加卡铂一线治疗晚期鳞状非小细胞肺癌的有效性和安全性。中国医学科学院肿瘤医院主任医师石远凯博士为该试验的主要研究者。此前,TQB2450已被CDE纳入突破性治疗品种,适应症为非微卫星高度不稳定(非MSI-H)或非DNA错配修复缺陷(非dMMR)的复发性或转移性子宫内膜癌。
2.基石PD-L1单抗食管鳞癌III期临床积极。基石药业宣布PD-L1舒格利单抗注射液(择捷美)联合化疗一线治疗无法手术切除的局部晚期、复发或转移性食管鳞癌的III期临床(GEMSTONE-304)达到主要研究终点。与安慰剂联合化疗相比,择捷美®联合化疗显著改善BICR评估的无进展生存期(PFS)和总生存期(OS),而且联合治疗未发现新的安全性信号。该公司计划近期向国家药监局递交其上市申请。
3.众生新冠口服药完成III期研究患者入组。众生药业宣布其口服抗新冠3CL蛋白酶抑制剂RAY1216片用于治疗轻型和普通型新冠病毒感染患者的III期临床已完成全部1360例患者入组。在一项研究者发起的RAY1216用于治疗新冠感染患者的剂量探索性研究中,RAY1216单药组或联合利托那韦组均较安慰剂组显著降低新冠病毒RNA载量和缩短病毒核酸转阴时间,并且药物的总体耐受性良好。
4.科兴新冠口服药完成II期研究患者入组。科兴生物新冠病毒聚合酶(RdRp)抑制剂SHEN26胶囊用于治疗轻型和普通型新冠病毒感染患者的II期临床完成全部受试者入组。这是一项随机、双盲、安慰剂对照的临床研究,主要终点指标为SARS-CoV-2病毒RNA水平(RT-PCR检测)相对于基线的变化值。在已完成的I期临床试验中,SHEN26胶囊显示出良好的耐受性和安全性。
5.迈威铁稳态调节单抗获批贫血临床。迈威生物1类新药9MW3011注射液获国家药监局批准两项临床试验默示许可,拟用于治疗β-地中海贫血铁过载和真性红细胞增多症。9MW3011是一款创新靶点单抗药物,特异性结合,上调肝细胞表达铁调素的水平,抑制铁的吸收和释放,降低血清铁水平,从而调节体内的铁稳态。今年11月,该新药已在美国获批开展用于真性红细胞增多症患者的临床试验。
6.百暨基因CLL-1靶向CAR-T获批新临床。广州百暨基因自主研发的“自体抗CLL-1嵌合抗原受体T细胞注射液”(BG1805)获国家药监局临床默示许可,拟开发用于治疗复发难治性急性髓系白血病(R/R AML)。BG1805是该公司拥有核心专利技术、靶向CLL1的CAR-T疗法,已先后获得FDA和EMA授予的孤儿药资格。公布在2021ASCO年会上的初步疗效数据显示,BG1805在R/R AML患者中达到81.8%的ORR,总疾病控制率(DCR)高达90.9%。
7.辉瑞双激酶抑制剂获批白癜风临床。辉瑞JAK3/TEC抑制剂Ritlecitinib胶囊(利特昔替尼)获国家药监局临床试验默示许可,拟用于12岁及以上适合接受系统性治疗的非节段型白癜风患者。这是继斑秃、溃疡性结肠炎后,利特昔替尼在国内获批临床的第3项适应症。2022年11月,CDE已将利特昔替尼用于适合接受系统性治疗的12岁以上斑秃患者的上市申请纳入优先审评。
国际药讯
1.2023年有望获批的十大潜在重磅疗法。日前,Evaluate发布一份报告,预测2023年有望获批的10款创新疗法。这10款潜在重磅疗法分别为:治疗阿尔茨海默病(AD)引发的轻度认知障碍的Aβ抗体lecanemab(卫材/渤健)、用于治疗杜氏肌营养不良的基因疗法SRP-9001(Sarepta/罗氏)、Pegcetacoplan(Apellis公司)、Donanemab(礼来)、RSVPreF3 OA(GSK)、Epcoritamab(艾伯维/Genmab)、Zuranolone(渤健/Sage)、Mirikizumab(礼来)、Eetrasimod(辉瑞)、Sotatercept(默沙东)。
2.辉瑞血友病B基因疗法Ⅲ期临床积极。辉瑞基因疗法Fidanacogene Elaparvovec治疗中重度至重度血友病B成年男性患者的Ⅲ期临床(BENEGENE-2)结果积极。数据显示,Fidanacogene Elaparvovec单次给药达到了主要研究终点,所有患者的年平均出血率(ABR)从预处理期的4.43降至1.3(降低71%,p<0.0001);年化输注率也降低92%(p<0.0001);药物整体的耐受性良好。此前,该新药已获FDA的突破性再生医学高级疗法和孤儿药认定。
3.Opus Genetics收购两种眼科基因疗法。基因治疗药物公司Opus Genetics宣布与Iveric Bio公司就后者两款临床前阶段的遗传性视网膜疾病 (IRD) 基因治疗候选产品达成合作和许可协议。Opus拟开发新型基因治疗药物以治疗bestrophin-1 (BEST1)相关的遗传性视网膜疾病和视紫红质介导的常染色体显性视网膜色素变性(RHO-adRP)。根据协议,Iveric将获得50万美元的预付款,开发和监管等里程碑潜在付款,以及产品的销售分成。
4.干细胞疗法治疗新冠后遗症临床积极。近期,美国报道一项脐带充质干细胞治疗危重型COVID-19相关呼吸窘迫综合征(ARDS) 患者的随机、对照、双盲研究积极结果。24例危重型患者2次干细胞输注后,患者炎症指标改善,复查时氧合指数升高至301 mmHg,胸部CT提示双肺病灶较前吸收,患者呼吸道症状改善;并缩短治疗时间,显著改善患者存活率。干细胞显示出修复新冠患者脏器损伤的治疗潜力。
医药热点
1.北京协和发布新冠感染基层诊疗方案建议。北京协和医院针对目前缺乏循证医学证据的关键临床等问题、结合北京协和医院一线经验,就新冠病毒感染患者诊疗编写了基层版诊疗方案建议。该建议采用基层工作中经常使用的“评估—分类—处理”模式推荐基层新型冠状病毒感染(以下简称新冠)诊疗的流程。对于重症患者,要求基层应紧急处理后协助联系转运通道尽快转诊。
2.广东发热门诊有了电子地图。广东省卫健委发布发热门诊(诊室)电子地图,居民登录“粤健通”微信小程序“发热门诊查询”后,将自动排列出距离自己最近的发热门诊(诊室)。居民选定就诊的发热门诊(诊室)后,点击“到这去”,即可导航前往,操作方便,居民能够快速找到最近的发热门诊(诊室)问诊。
3.江宁军博士将加入恒瑞医药。据悉,原基石药业CEO江宁军博士将加入恒瑞医药,担任副总经理、首席战略官,负责临床研究和商务拓展工作。由孙飘扬、张连山和江宁军组成恒瑞医药战略决策小组,全面负责恒瑞医药的战略和研发决策。加入恒瑞医药后,江宁军直接汇报于恒瑞医药董事长孙飘扬。目前,恒瑞医药尚未对此消息进行官方回应/证实。
评审动态
1. CDE新药受理情况(01月03日)
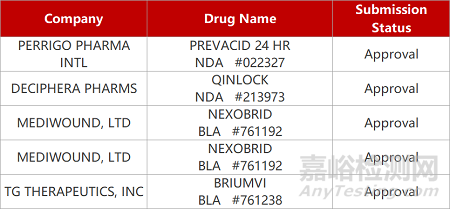
2. FDA新药获批情况(北美12月29日)