近期,宾夕法尼亚州立大学程寰宇﹑杨健教授和电子科技大学林媛教授在科爱出版创办的期刊 Bioactive Materials 上联合发表综述文章:用于伤口愈合与治疗智能敷料的最新进展。伤口实时监测与治疗是伤口愈合的关键,这推动着伤口敷料往智能化和多功能化方向发展。该文详细总结了闭环智能伤口敷料的材料设计﹑结构设计与实时监测单元的最新研究进展,并指出可延展传感器以及无线通讯技术在伤口监测与药物管理的重要作用以及智能伤口敷料的传感治疗多功能集成的设计与加工上挑战。
1、研究内容简介
术后伤口恢复和免疫缺陷造成的慢性伤口溃烂是临床医学上的难点,且患者比例逐年上升。通过使用伤口敷料固定伤口切面﹑抵抗细菌感染﹑施加生长因子﹑诱导免疫系统有序反应是加速伤口愈合的主要手段。传统的伤口敷料研究关注敷料本身的机械性能,包括黏性和内聚力,自然界中广泛存在的生物黏附现象从材料和结构两方面为伤口敷料设计提供了极大灵感。近期提出的水凝胶由于其良好的生物兼容性﹑优异的药物输运性以及外场可控交联方式,在伤口敷料方向展现了巨大的应用前景。最新研究表明光﹑电﹑机械刺激和它们之间的协同刺激都可以促进生长因子分泌和组织再生,极大地加快伤口愈合。除了伤口治疗,将柔性传感器集成在敷料中对伤口进行实时检测和评估也是闭环智能伤口敷料的重要功能。伤口传感数据通过先进的无线技术与终端设备进行交互,促发药物管理系统进行智能化药物释放,保证伤口有效愈合。该文章从材料﹑结构以及系统三个方面介绍了敷料,传感器以及无线技术在闭环智能伤口敷料的最新研究进展进行了详细综述 (图1)。
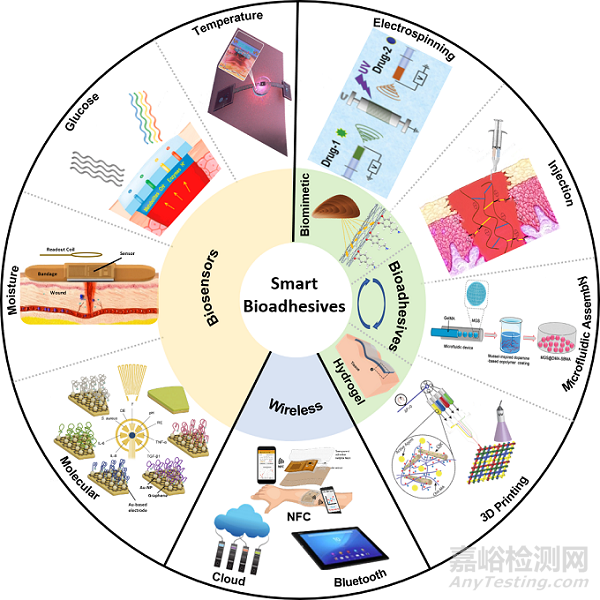
图1:智能伤口敷料技术总结
一、免疫调节水凝胶敷料
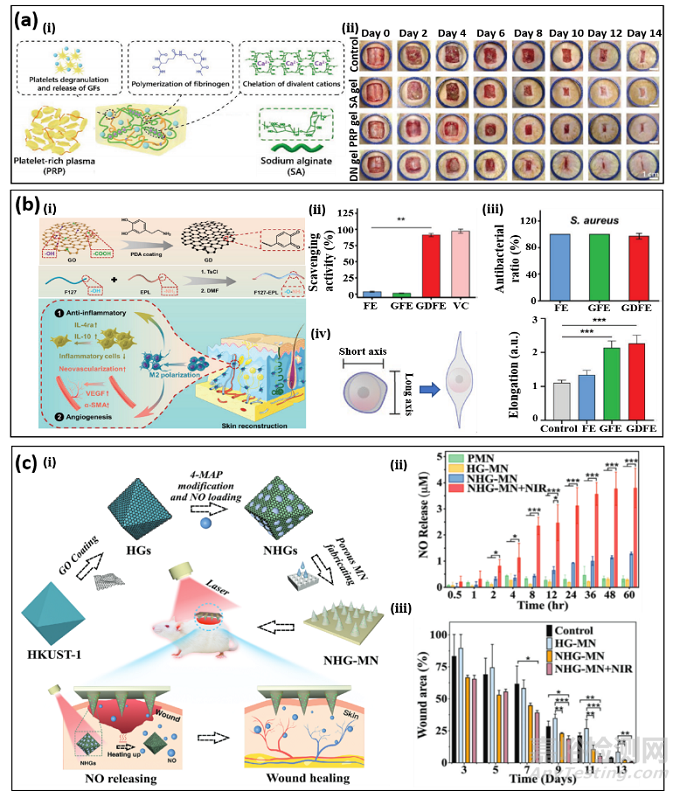
伤口愈合是一个有序的先天性与特异性免疫反应参与过程,包含了凝血﹑炎症﹑修复与成熟四个阶段。先天性免疫系统在炎症期检测到异体信号,然后特异性免疫系统开始清理病原体。参与免疫反应的细胞与组织之间的协同工作依靠一套可靠的信号系统,包括生长因子﹑细胞因子﹑趋化因子等。信号交流紊乱会引起免疫反应失效,从而导致伤口无法愈合,甚至是截肢或者死亡。例如,伤口愈合过程中细胞因子和活性氧的过度表达会导致促炎性到促再生阶段过渡的延时,导致伤口溃烂。考虑到伤口愈合是一个复杂生理过程,相比于直接药物管理,通过特定的物理化学刺激促发人体自身免疫反应是治疗伤口感染或发炎更有效的方式(图2)。水凝胶因为其可控的化学组分﹑机械性能﹑交联促发机制﹑药物加载和释放方式,是一种优良的伤口敷料。前期研究发现,一些特定水凝胶本身化学成分具有免疫调节功能,比如玻尿酸和壳聚糖水凝胶。另外,通过对水凝胶进行表面修饰或者掺杂也可以达到免疫调节的作用。例如,对F127水凝胶掺杂多巴胺修饰氧化石墨烯和ε-聚赖氨酸可以同时取得抗菌和免疫调节的作用。该水凝胶可以通过多巴胺到多巴醌的氧化反应有效降低氧化自由基的浓度,进而促进巨噬细胞向M2表型细胞极化,加速糖尿病患者伤口愈合。一种基于血浆含有多种生物活性分子,具有天然的免疫调节功能。通过在血浆中引入海藻酸钠形成双网络水凝胶结构,可以有效解决血浆机械强度低和生物活性因子释放过快等问题,从而加速伤口愈合。一氧化氮是重要的神经递质和免疫反应的生物信号分子,在伤口由发炎过渡到修复阶段担当着重要作用,如何在伤口处持续地释放一氧化氮气体成为了研究的难点问题。多孔的MOF颗粒是优良的一氧化氮气体载体,通过对颗粒外表面行进氧化石墨烯修饰然后加载在聚乙二醇水凝胶的交联网络中,可以实现红外光控制的一氧化氮可持续释放,进而调节免疫系统加快伤口愈合。
图2:免疫调节水凝胶. (a)基于血浆与海藻酸钠双网络水凝胶;(b)F127水凝胶掺杂多巴胺修饰氧化石墨烯和ε-聚赖氨酸同时具有抗菌和免疫调节的作用;(c)MOF颗粒修饰聚乙二醇水凝通过可持续释放一氧化氮气体调节伤口愈合免疫反应
二、柔性生物传感器
慢性伤口恢复是一个动态且漫长的过程,患者需要经常去医院做伤口诊断和治疗,比如清理伤口和更换敷料,而且伤口评估主要依靠医生的经验和主观判断,往往导致错误判断。通过柔性生物传感器对伤口状态进行科学的﹑实时的诊断和评估已经成为了伤口管理的新趋势,其中监测指标包括pH值﹑温度﹑湿度﹑尿酸﹑葡萄糖与氧气浓度等。pH值主要影响炎症反应﹑胶原蛋白形成与血管再生等过程。对于急性伤口,pH值在4到6之间,可以有效阻止细菌增殖。由于免疫系统紊乱,慢性伤口的pH值在7到9之间波动,很容易导致细菌入侵和伤口感染。温度对参与伤口愈合过程的各种酶的反应活性,伤口局部血流和淋巴细胞迁移具有重要影响,因为被认为是伤口愈合过程中最具参考意义。研究表明,伤口温度低于33 °C会降低纤维母细胞﹑中性粒细胞以及上皮细胞的活性,不利于伤口愈合。人体无法分泌尿酸代谢酶,而某些细菌可以直接进行尿酸代谢,因为伤口渗出物较低的尿酸含量可能预示着伤口感染。较高的葡萄糖浓度会阻碍毛细血管的新生,进而导致组织坏死。伤口处充足的氧气浓度可以刺激白细胞进入伤口区域﹑抵抗细菌感染﹑加快局部新陈代谢,促进组织再生。
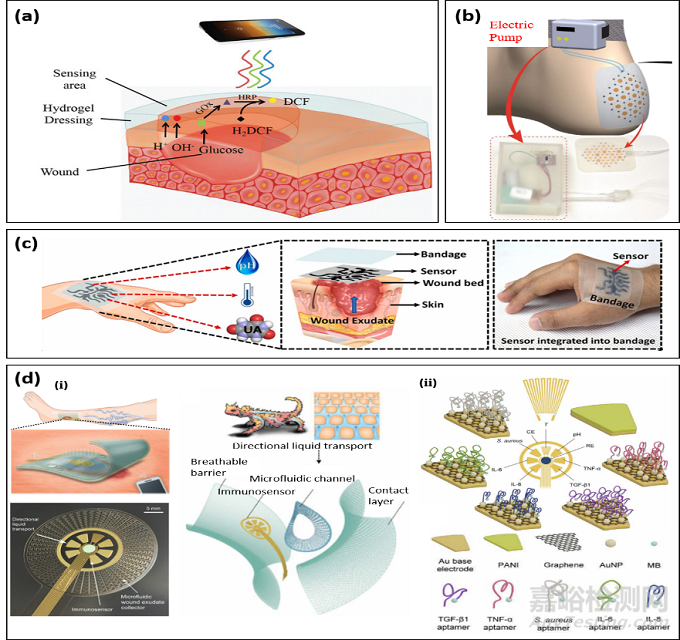
针对这些关键伤口指标,一系列新颖的多功能柔性传感器被提出并且在展现出巨大的应用前景(图3)。基于酸碱指示剂和荧光效应,一种多功能水凝胶可以同时监测伤口处pH和葡萄糖浓度值。一种纸基微流管道的贴片可以通过微流泵往伤口处定向输送氧气,有效提高氧气浓度高达25-50%,加快伤口愈合速度;基于荧光效应,钌化合物可以准确检测5-26 ppm的氧气浓度范围。纳米材料具有优异的电化学性能,被广泛应用生物传感。基于激光诱导石墨烯和MXene的复合材料可以同时检测伤口处的pH值和尿酸浓度,并且线性度高达0.99。此外,该复合材料的电阻温度系数在25-50 °C范围内为0.09% ˚C-1并具有很高的线性温度响应性能(~0.99)。最近,一种专门针对慢性伤口检测的智能贴引起了学界的关注,它集成了微流控芯片﹑免疫炎症因子(包含tumor necrosis factor–α (TNF-α), interleukin-6 (IL-6), IL-8, transforming growth factor–β1)﹑细菌﹑温度传感以及无线传输模块。受鲨鱼牙齿的启发,该微流通道可以有效地收集微量伤口渗出液并将其输运到检测区域。通过对电化学传感器工作电极进行金纳米颗粒与石墨烯修饰,接着引入适配体,炎症因子以及细菌浓度通过方波伏安法标定和测量。
图3:用于伤口监测的柔性生物传感器. (a)基于酸碱指示剂和荧光反应监测伤口pH值与葡萄糖浓度;(b)钌化合物的荧光反应检测伤口处氧含量;(c)基于激光诱导石墨烯和MXene复合材料的柔性pH,温度与尿酸传感器;(d)针对慢性伤口炎症检测的适配体电化学传感器
三、多功能或闭环伤口敷料
集成诊断和治疗功能的智能伤口敷料具有广阔的应用前景。通过柔性传感器实时、原位地监测伤口生理指标并及时释放药物可以大大降低置换敷料带来的痛苦,减少伤口感染和发炎的风险(图4)。用氨基苯硼酸(ABA)嫁接金纳米颗粒修饰的纤维素敷料不仅具有优良的抗菌性,而且可以根据荧光强度判断敷料上纳米药物残余,从而及时进行敷料更换。由于伤口渗出物及其微量,对它进行有效的收集是准确检测伤口状况的关键,利用特殊结构设计的微流管道是解决这一难题的有效途径。由于毛细力的作用,伤口渗出液会自发地被收集到光子晶体检测区域,乳酸和钙防卫蛋白等伤口标记分子可以通过荧光反应进行标定。当相关指标异常时,加载在多孔微针的生长因子会主动释放,从而加快伤口愈合。另一方面,无线技术可以极大地减小智能伤口敷料的尺寸和增加其功能多样性,包括非接触式检测﹑远程监控与药物管理。例如,导电纤维作为伤口缝线与插值电极构成LC振荡电路,可以通过共振频率的偏移和幅值变化来远程监测内部伤口泄露与缝线断裂。集成温度传感器﹑LED﹑药物加载水凝胶以及近场耦合通信的智能闭环伤口敷料可以实时监测伤口温度﹑评估伤口感染程度﹑传输传感数据﹑接收远程药物管理命令。实时传感数据与药物管理命令的通过近场传输相互交互可以有效的避免治疗不及时和药物乱用带来的严重后果。基于蓝牙无线传输的智能水凝胶伤口敷料具有更远的工作距离,伤口处的异常温度上升触发UV-LED开启,抑制细菌生长。
图4:集成生物检测、治疗与无线数据传输的智能伤口敷料。(a)基于金纳米颗粒药物的抗菌伤口敷料及其纳米药物残留自检测机制;(b)集成微流管道和多孔水凝胶微针进行有效伤口渗出液收集与生长因子释放;(c)导电纤维伤口缝线与插指电极构成的LC震荡电路对内部伤口泄露与缝线断裂进行监测;(d)基于无线近场传输的闭环智能伤口敷料实现伤口温度﹑pH﹑尿酸的检测以及抗菌药物的释放;(e)基于蓝牙无线传输的闭环智能伤口敷料实时监测伤口温度异常并远程开启UV-LED进行杀菌