首先了解一下设计输出的定义:根据设计输入,完成某一项或多项设计活动而得到的可交付的设计成果。
设计成果可以是文字性的资料,可以是图纸性资料,也可以是实物等等。
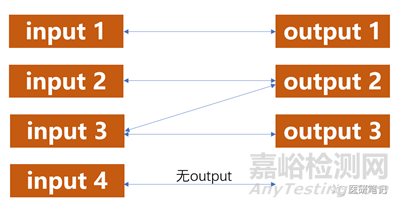
从定义上可以获得:设计过程也必须具有可追溯性,即每一个设计输出,必须可追溯至一个或几个设计输入。或者几个设计输出,可追溯到一个设计输入。
项目结束时,建议大家对每一个输出的成果进行追溯,在设计输入的资料里,都应该找到相对应的条款。
但是并不是每一个设计输入都会有设计输出,就是我之前是说的,设计输入尽可能全面,做到宁多毋缺。
一个完整合格的设计输出必须具备2个基本功能:
1) 为产品实现提供信息:如采购规范、成品规范、生产程序、检验和测试程序、说明书或维修手册、标签和包装等。
2) 被用于验证器械是否满足规范、并确认器械是否满足市场营销、法规监管、客户需求以及预期用途。
设计输出的资料是审评过程中重点审查的内容,每一项的输出都会影响产品的安全性和有效性。
项目结束时,大家可以核对下面的问题清单,自查自己的设计输出是否完整。
1) 是否能准确告诉他人,项目的产品是什么?
2) 这个产品是由什么材料制成的,及材料的要求是什么?
3) 是如何正确生产这个产品的?
4) 是在什么环境下生产的?
5) 生产过程需要哪些工装、设备?
6) 检验过程需要什么设备、仪器?
7) 质量验收的标准是什么?
8) 如何测试质量水平?
9) 产品的风险是如何管理的?
10) 如何使用这个产品,或者如何安装、维护这个产品?
本篇以一个三类无源医疗器械为例,提供了一个模版,供大家参考。