您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-01-13 11:46
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
首个国产CD20单抗报NDA。博锐生物与海正生物自主研发的1类创新型CD20单抗泽贝妥单抗(HS006,安瑞昔)的上市申请获CDE受理,用于治疗CD20阳性弥漫大B细胞性淋巴瘤(DLBCL)初治患者。在III期临床中,HS006联合CHOP方案治疗DLBCL初治患者在ORR上非劣效于R-CHOP,且在治疗结束时CR率显著更高;1年PFS和OS呈现出显著优于美罗华组的趋势。安瑞昔也是首个申报上市的国产CD20新药。
国内药讯
1.贝达多靶点激酶抑制剂报NDA。贝达药业1类新药伏罗尼布片的上市申请获CDE受理。根据贝达药业官网信息,推测伏罗尼布(CM082,vorolanib)是具有全新化学结构的新一代多靶点激酶抑制剂,申报的适应症可能为:与依维莫司联合用于治疗晚期肾癌患者。目前,该产品正在Ⅱa期临床中用于治疗慢性年龄相关性黄斑病变,在Ⅱ/Ⅲ期研究CONCEPT中评估与依维莫司联合治疗晚期肾癌的潜力。
2.三生制药米诺地尔泡沫剂报产。三生制药5%米诺地尔泡沫剂的上市申请获CDE受理。这是三生制药在米诺地尔酊(蔓迪)基础上开发的新一代防脱生发产品,拟用于治疗雄激素性脱发。该药处方体系不含有丙二醇,可减少过敏瘙痒的发生率;而且泡沫剂密度小,较其它外用制剂(酊剂、搽剂、外用溶液、喷雾剂)更易分布于表皮,利于涂沫后药物分散且均匀。
3.恒瑞「海曲泊帕乙醇胺」获FDA临床许可。恒瑞医药口服小分子非肽类TPO-R激动剂海曲泊帕乙醇胺片获FDA批准,即将在美国开展用于化疗所致血小板减少症(方案编号:HR-TPO-CIT-301)的Ⅲ期临床。海曲泊帕乙醇胺通过激活TPO-R介导的STAT和MAPK信号转导通路,促进血小板生成。该新药已在中国获批上市,用于既往对糖皮质激素、免疫球蛋白等治疗反应不佳的慢性原发免疫性血小板减少症(ITP),以及用于对免疫抑制治疗疗效不佳的重型再生障碍性贫血,商品名为恒曲。
4.君实TIGIT单抗2.9亿美元出海。君实生物宣布,Coherus已启动行使TIGIT单抗JS006在美国和加拿大的许可选择权的程序。同时,Coherus将向君实生物支付3500万美元首付款,最高达2.55亿美元的开发、申报和销售里程碑付款,以及产品销售净额18%的销售分成。JS006是君实生物自主研发的抗TIGIT单抗注射液,可特异性阻断TIGIT-PVR抑制通路,刺激杀伤性免疫细胞活化,分泌肿瘤杀伤性因子,与抗PD-1/PD-L1抗体可发挥协同抗肿瘤作用。
5.Sana、驯鹿和信达达成合作协议。Sana Biotechnology、驯鹿医疗与信达生物就经临床验证的BCMA CAR达成战略合作和非独家许可协议。BCMA CAR是驯鹿医疗与信达合作开发的BCMA CAR-T产品(CT103A/IBI326)中的关键成分。根据协议,Sana将获得BCMA CAR的非独家商业权利,应用于Sana特定的体内基因治疗和体外低免疫细胞治疗产品开发。驯鹿/信达将获得首付款、和最多6个产品、约2.04亿美元的潜在开发、注册里程碑付款和销售分成。
国际药讯
1.KRAS G12C抑制剂在美报NDA。Mirati公司宣布其KRAS G12C抑制剂adagrasib已向FDA递交新药上市申请,用于二线治疗携带KRAS G12C突变的非小细胞肺癌(NSCLC)患者。一项Ⅱ期临床数据显示,在携带KRAS G12C的意向治疗人群分析中,adagrasib达到43%的客观缓解率(ORR)和80%的疾病控制率(DCR)。Adagrasib具有长达24小时的半衰期和血脑屏障渗透性特点,此前已获FDA授予突破性疗法认定。
2.Bicycle两款PDC抗肿瘤临床积极。英国专注于双环肽技术的生物技术公司Bicycle 公布了两款PDC产品(BT8009和BT5528)的I/II期临床试验数据,二者均表现出良好的抗肿瘤活性。PDC是一种新型偶联药物,由多肽、细胞毒素和连接体三个部分组成,是肿瘤靶向药研究热点。但是,PDC的安全性存在非常大的争议,此前全球首款上市的PDC药物Pepaxtp因“不明原因的死亡风险增加”而遭FDA撤市。
3.辉瑞布局抗癌双抗。辉瑞宣布与Dren Bio公司将合作开发双特异性抗体疗法。Dren Bio开发的双特异性抗体,将肿瘤细胞与髓系细胞连接起来,产生强大而安全的免疫刺激、靶向吞噬作用和肿瘤新抗原的交叉呈递,潜在地促进持久的临床反应。根据协议,Dren Bio将获得2500万美元的预付款,总额超过10亿美元的开发、监管和商业里程碑潜在付款,以及产品的销售分成。
4.安进联手Arrakis 开发RNA降解疗法。安进与Arrakis Therapeutics达成一项研究合作,利用Arrakis开发的端到端RNA靶向小分子(rSM)药物发现平台,针对安进指定的难以成药靶标,合作开发创新靶向降解RNA的候选小分子。根据协议,安进将为5个初始项目向Arrakis支付7500万美元的预付款,并拥有选择权提名额外的项目;Arrakis将获得高达数十亿美元的临床前、临床、监管和销售里程碑潜在付款,以及产品的销售分成。
5.辉瑞拟建立AI实验室。辉瑞宣布扩大与PostEra的研发合作,并建立一个人工智能实验室(AI Lab)。AI Lab旨在将PostEra公司基于机器学习算法的药物设计和合成技术平台,与辉瑞的专业知识和数据结合起来,共同推进肿瘤学和抗新冠病毒治疗药物等多个药物发现项目。根据协议,PostEra将获得1300万美元的预付款,总额高达2.48亿美元的额外里程碑潜在付款,以及产品的销售分成。
6.Aligos终止乙肝新药的开发。Aligos公司宣布已停止进一步开发针对慢性乙型肝炎(CHB)的寡核苷酸聚合物(STOP)ALG-010133。在一项Ⅰ期研究ALG-010133-101中,在预期有效剂量400毫克(肝暴露水平为EC90的3倍)几乎没有降HBsAg(乙肝表面抗原)活性;据预测在最高可行剂量600毫克能降低90%(1 log)HBsAg的可能性也很低。试验中未报告剂量限制性毒性。研究审查委员会认为数据不足以支持ALG-010133的进一步开发。
7.美国CMS拒绝支付阿尔茨海默病疗法。美国医疗保险和医疗补助服务中心 (CMS) 日前宣布,表示只会在CMS认可的随机对照试验中对用于治疗阿尔茨海默病(AD)的Aduhelm以及其他FDA批准的抗淀粉样蛋白单克隆抗体进行支付。Aβ抗体Aduhelm(aducanumab)是FDA自2003年以来,批准的首款AD新药。2021年7月,FDA缩小Aduhelm适应症标签,新标签强调Aduhelm适用于轻度或早期AD患者。
医药热点
1.全球首例猪器官异种移植手术成功。2022年1月10日,马里兰大学医学院成功为美国1例57岁患者移植猪的心脏,目前患者的状况良好。马里兰大学医学中心的医生表示,目前说这项手术完全成功还为时过早,但这已经证实了基因编辑的动物心脏可以在人体内正常工作而不会立即被排斥。这标志着数十年来寻求使用动物器官移植挽救生命的重要一步。
2.阜阳师范大学半年挂牌3家附属医院。1月6日,阜阳师范大学第二附属医院在安徽阜阳市第五人民医院正式揭牌,成为阜阳师范大学又一家直属附属医院。阜阳师范大学创办于1956年,为一所多学科本科院校。该院校自2019年10月成立医学院后,已于2021年6月和2021年12月,挂牌2家附属医院,分别为阜阳市人民医院和阜阳市第六人民医院。
3.上海:所有执业医师可开展中医诊疗。上海市日前出台《非中医类别执业医师开展中医诊疗活动执业管理办法》,2022年2月7日起,所有非中医类别的执业医师均可通过4种途径参与培训并考核合格后,即可开展中医诊疗活动。4种途径分别为:经过中医药相关培训且考核合格的,通过相关程序登记或授权;参加市级及以上卫健部门批准的不少于2年的西医学习中医系统学习培训班并取得相应证书;参加市卫健部门批准的专项中医医疗技术培训并取得相应证书;经医疗机构培训并考核合格。
评审动态
1. CDE新药受理情况(01月12日)
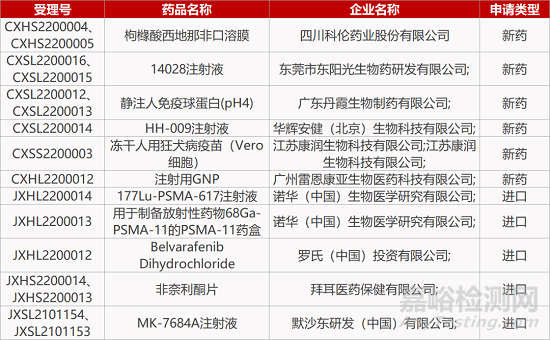
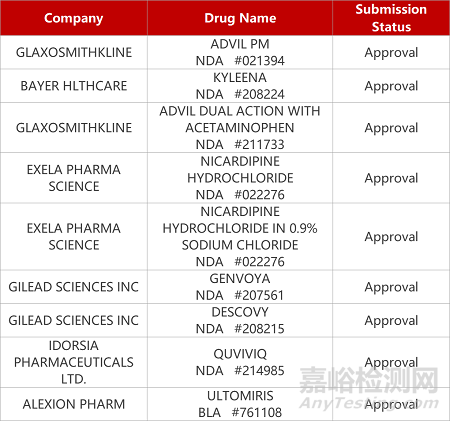

来源:药研发


