您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-08-12 19:33
冻干机广泛应用于制药、食品、生物等领域,主要分为实验室型、中试型和生产型。由于不同类型的结构原理存在的差异(主要体现在冷阱位置不同)会导致加热或制冷的方式、位置及测量要求不同,因此,为确保冻干过程的精确控制,提高产品的质量,本文针对其结构原理及现有的测量方法进行对比,并分析测量要求差异及存在问题。
真空冷冻干燥是冻干疫苗等生物制品和药品生产中的关键环节。冻干机作为其主体设备,性能是否满足要求并稳定可靠,关系着药品的质量和人们的生命健康。因此,需对温度、真空度进行精确控制。同时,不变性与速度进一步增加了两者的准确性和稳定性要求,生产厂家在冻干前需进行实验验证,确保其工作状态满足工艺要求[1-2]。
冻干机是将物料中的水分在低温、真空环境下直接升华成水蒸气,从而实现干燥目的,能在最大程度上保留物料的活性、营养成分和原有形态,延长物料的保存期限,广泛应用于制药、食品、生物等领域[3-5]。由于各类型的结构及原理存在显著差异,应用场景、生产规模及测量要求等方面也存在不同。因此,需进行深入研究测量要求及差异,从而提高产品质量,优化冻干工艺,确保产品符合相关质量标准,促进该技术在各个领域的广泛应用和持续发展。
Part.01冻干机种类
冻干机主要由制冷系统、真空系统、加热系统、控制系统、冻干腔和搁板等构成,可分为实验室型、中试型和生产型。
1.1实验室冻干机
实验室冻干机因具有小巧的体积和灵活的操作性,而在科研实验中发挥着不可或缺的作用,主要用于药品研发时小剂量药物样品的冻干实验,以及对细胞、蛋白质、核酸、酶等生物样品进行冻干保存或对一些新型材料的处理研究[6]。其通常采用钟罩式设计,即将冻干腔和冷阱设置为上下结构,并将用于放置物料的搁板位放置于整个仪器上方,使用透明有机玻璃罩罩住外部。其中,透明有机玻璃罩的设计便于实验人员观察物料的冻干情况,并实时掌握冻干过程中的变化。但部分钟罩式冻干机存在一定局限性,如冻干腔无预冻功能,需人工进行干预;使用过程中,物料预冻结束后,实验人员需人工操作将物料架提上来进行抽真空升华干燥,操作相对复杂。
1.2中试冻干机
中试冻干机满足从实验室研究到工业化生产的中间阶段需求。相较于实验室型,体积较大,在处理能力上具有显著提升,能处理相对较大体积的样品;但与生产型冻干机相比,规模相对较小,更侧重于中试规模的实验。其应用场景主要集中于将实验室研发成果进行放大验证和工艺优化。如在制药行业中,当新药研发进入中试阶段时,可用于模拟工业化生产条件,对冻干工艺进行进一步优化和验证,确定最佳的冻干参数(包括温度、压力、时间等),为大规模生产提供可靠的工艺依据;在食品行业中,对于一些新型食品的冻干工艺开发,能帮助企业在大规模生产前评估产品质量和生产可行性[7]。
1.3生产型冻干机
生产型冻干机容积和搁板面积较大,能同时处理大量的物料,满足大规模生产的需求,是大规模生产冻干产品的核心设备,被广泛应用于各个领域的大规模商业化生产。如抗生素、疫苗、生物制剂、中药注射剂等药品;冻干蔬菜、水果、肉类、海鲜、咖啡等冻干食品;酶、蛋白质、多肽、细胞因子等生物制品。此外,在化妆品、保健品、农业、电子等行业中也有一定的应用,如化妆品生产中,用于冻干面膜、精华液等产品;农业领域中用于冻干种子、生物菌剂等[8]。
目前,该冻干机大部分已采用先进的自动化控制系统,不仅能实现冻干过程的全程自动化控制,减少人工操作,而且能在较短的时间内完成冻干过程,提高生产效率。此外,部分设备还具备良好的清洗和消毒功能,能快速进行清洁和维护,为下一次生产做好准备。
Part.02测量要求差异分析
生产型与中试型的工作原理和控温方式基本相似,主要采用搁板控温式的冻干腔和冷阱为一体。其中,冻干腔中的搁板内部为冷阱盘管,该设计不仅自动化程度较高,操作简便,而且与钟罩式相比,控温精度更高,能实现物料的均匀加热和冷却,有效确保冻干产品质量的稳定性和一致性。由于两种方式主要差异为控温原理不同,因此主要测量要求差异为温度测量。
2.1测冷阱温度
钟罩式冻干机是由冷阱在下部控温,通过空气传热实现对搁板上物料的温度控制。目前,冷阱温度主要采用直接测量下方冷阱的方式。
以万能表的温度传感器为例。首先,将其连接至冻干机的冷阱里面壁上;然后,打开浓缩机和真空泵预平衡系统1h, 再将旋钮选到温度档,依次测定30min、60min、90min、120min冷阱温度。每个校准点重复测6次,并计算算术平均值,再按式(1)、式(2)分别计算示值误差及相对实验标准,并作为重复性的表征。


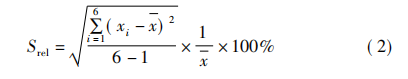

2.2测搁板温度
搁板控温冻干机是通过搁板直接进行控温。目前,主要根据JJF(蒙)074-2024校准规范[9]对搁板温度进行测量。
(1)将温度测量点(一般为5个)布置在除顶层搁板外各层表面的4个角和几何中心,并与其充分接触导热。其中,4角测量点位应靠近每层硅油的进、出口位置,与边缘的距离为各边长的1/10;真空测量点应除顶层搁板外,均匀分布于最接近上、中、下搁板的中部。
(2)冻干机稳定后,在30min内对各测量点进行测量,并将每次测量的最高与最低温度之差的最大值作为均匀度的校准结果。均匀度的计算公式为:
ΔTu=max (Timax-Timin) (3)
式中:ΔTu——温度均匀度,℃;Timax、Timin——第i次,各测量点的最高(上偏差)、最低(下偏差)温度,℃。ΔTmax=Tmax-Ts(4)
ΔTmin=Tmin-Ts(5)
式中:Tmax、Tmin——各测量点规定时间内的最高、最低温度,℃;Ts——设定温度,℃。
Part.03存在的问题
根据3种类型冻干机的结构原理分析可知,不同类型冻干机最大的差异在于冷阱位置不同会直接导致加热或制冷方式及位置的差异。现有的测量方法虽然在一定程度上能满足其温度测量的需求,但仍存在一些问题。其主要包括:
(1)目前,尚无通用于所有种类冻干机的测量方法。如现有的针对钟罩式冻干机和搁板控温冻干机的测量方法。
(2)现有的钟罩式冻干机测量法在实际操作中,难以将万用表的温度传感器连接至冷阱里面壁上,且连接方式无法进行溯源,导致无法确定测量结果的准确性是否符合标准要求,对其进行有效的质量控制和评估。
(3)目前,未有相应的国家校准规范,如JB/T 20032-2012行业标准[10]缺乏具体有效的校准方法,对真空冻干机的技术要求较低,无法满足当前形式下生物医药领域的需求;《药品GMP指南 无菌药品》[11]中第8章节及附录2、EU GMP Annex1 Manufacturing of Sterile Products[12]、Lyophilization of Parenteral (7/93) FDA检查指南等药品验证方法均为厂家自行验证方法,即不同实验室或企业可能采用不同的测量方法和标准,缺乏对设备性能的具体有效的校准方法,使性能评估缺乏一致性和可比性。
因此,为了推动冻干机技术的进一步发展,提高冻干产品质量,迫切需完善科学统一的校准方法,对真空冻干机设备进行在线全过程校准,以及对设备的各参数进行全面有效的定期校准,确保设备的性能可靠,从而保证产品质量的稳定性和一致性。此外,相关科研机构和行业组织应加强合作,共同制定统一的测量标准和校准规范,促进冻干行业的健康发展。
参考文献
[1]肖芃,陈玲玲,肖晓,等 . 药用真空冷冻干燥机搁板温度均匀性和压力性能检测方法[J]. 计量与测试技术,2023,50( 06) : 87 - 89.
[2]赵晶,张海锭,万正军,等 . 药用真空冷冻干燥机校准方法研究[J]. 计量与测试技术,2023,50( 10) : 80 - 83.
[3]张燕 . 制药企业真空冷冻干燥机的确认[J]. 设备管理与维修,2023,( 12) : 165 - 167.
[4]林洪,邓凯,宁钟灵,等 . 真空冷冻干燥机性能确认方法的研究[J]. 大众科技,2023,25( 01) : 74 - 77.
[5]吴兰,赵杨 . 真空冷冻干燥工艺优化及其品质预测[J/OL].食品与发酵工业,1 - 9[2025 - 04 - 22]. https: / /doi. org /10. 13995 /j. cnki. 11 - 1802 /ts. 041307.
[6]张晓敏,张力,贺雪英,等 . 冷冻干燥法制备聚合物基新型材料及其应用[J]. 化学进展,2014,26( 11) : 1832 - 1839.
[7]None. 伊马 Lyofast Mini 冷冻干燥机[J]. 流程工业,2019,( 08) : 88.
[8]王喆 . 探究真空冷冻干燥技术在生物制药方面的应用[J].世界最新医学信息文摘,2019,19( 88) : 247 - 248.
[9]JJF ( 蒙) 074 - 2024《真空冻干机校准规范》[S].
[10]JB/T 20032 - 2012《药用真空冷冻干燥机》[S].
[11]国家食品药品监督管理局药品认证管理中心编写 . 药品GMP 指南·无菌药品[M]. 北京: 中国医药科技出版社,2011.
[12]Sandle T. Draft Revision of EU GMP Annex 1 Manufacturing ofSterile Medicinal Products for Targeted Consultation: Implications for Cleanrooms[J]. Clean Air and Containment Review,2018,2018( 33) : 16 -21.

来源:Internet