刚刚,国家药监局发布《丹七片中异性有机物检查项补充检验方法》《脑立清丸(胶囊、片)中水麦冬酸检查项补充检验方法》《檀香清肺二十味丸中松香酸检查项补充检验方法》《小柴胡颗粒中黄芩提取物检查项补充检验方法》,内容如下:
丹七片中异性有机物检查项补充检验方法
(BJY 202301)
【检查】异性有机物 本品为部分浸膏片,除三七显微特征外,不得检出其他植物组织。
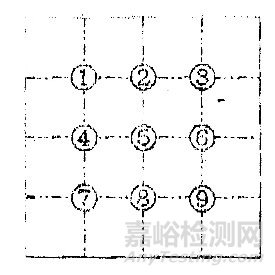
取本品2片,除去包衣,研细,称取细粉0.1g,加水10ml使溶解,离心,弃去上清液,沉淀加水2ml使混悬,吸取混悬液1滴,置于载玻片上,加水合氯醛1滴,加热透化,置显微镜100倍下,按下图选取9个检查点检视,视野中除三七的植物组织特征外,不得检出其它植物组织。
如仅有1个检查点视野中检出除三七显微特征外的其他植物组织,应依法制片复试,复试不得检出。
盖玻片上检查点示意图
起草单位:柳州市质量检验检测研究中心(柳州市食品药品检验检测中心)
复核单位:湖南省药品检验检测研究院
北京市药品检验研究院
脑立清丸(胶囊、片)中水麦冬酸检查项补充检验方法
(BJY 202302)
【检查】水麦冬酸 照高效液相色谱法(中国药典 2020 年版通则 0512)和质谱法(中国药典 2020 年版通则 0431)测定。
色谱、质谱条件与系统适用性实验 以十八烷基硅烷键合硅胶为填充剂(色谱柱内径2.1mm);以乙腈为流动相A,以0.1%甲酸溶液为流动相B,按下表中的规定进行梯度洗脱,流速为每分钟0.2ml;采用质谱检测器,电喷雾负离子模式(ESI-),进行多反应监测(MRM),选择质荷比m/z187.0→143.0和m/z187.0→99.0作为检测离子对。取对照品溶液,进样2µl,按上述离子对测定的MRM色谱峰的信噪比均应大于10:1。
|
时间(分钟)
|
流动相A(%)
|
流动相B(%)
|
|
0~10
|
1→5
|
99→95
|
对照品溶液的制备(临用新制) 取水麦冬酸对照品适量,精密称定,加乙腈-0.1%甲酸溶液(1:99)制成每1ml含0.25μg 的溶液,作为对照品溶液。
供试品溶液的制备 取脑立清丸、片、胶囊内容物,研细,取约8.0g(相当于清半夏1g),精密称定,置具塞锥形瓶中,精密加水50ml,称定重量,超声处理(功率500W,频率40kHz)45分钟,放冷,再称定重量,用水补足减失的重量,摇匀,离心(转速为每分钟8000转)5分钟,取上清液,滤过,精密量取续滤液25ml至离心管中,加甲酸0.2ml,摇匀,加入乙酸乙酯20ml,摇匀,离心(转速为每分钟5000转)5分钟,分取乙酸乙酯液,自“加入乙酸乙酯20ml”起,再同法操作3次,合并乙酸乙酯液,减压回收溶剂至干,残渣加乙腈-0.1%甲酸溶液(1:99)使溶解,并定容至2ml,用微孔滤膜(0.22μm)滤过,取续滤液,即得。
测定法 分别精密吸取对照品溶液与供试品溶液各2μl,注入液相色谱-质谱联用仪,测定,即得。
(1)供试品的提取离子流色谱中,未同时出现与对照品溶液色谱相应的色谱峰,视为未检出;(2)供试品的提取离子流色谱中,同时出现与对照品溶液色谱相应的色谱峰,且供试品色谱中 m/z 187.0→143.0 的色谱峰面积值不大于对照品溶液中相应的峰面积值,视为未检出;(3)供试品的提取离子流色谱中,同时出现与对照品色谱相应的色谱峰,且供试品色谱中 m/z 187.0→143.0的色谱峰面积值大于对照品溶液中相应的峰面积值,视为检出。
结果判定 供试品的提取离子流色谱中,应不得检出与对照品溶液色谱相应的色谱峰。
起草单位:山东省食品药品检验研究院
复核单位:河北省药品医疗器械检验研究院
四川省药品检验研究院(四川省医疗器械检测中心)
檀香清肺二十味丸中松香酸检查项补充检验方法
(BJY 202303)
【检查】松香酸 照高效液相色谱法(中国药典2020年版通则0512)测定。
色谱条件与系统适用性试验 以十八烷基硅烷键合硅胶为填充剂;以乙腈-0.1%甲酸(74:26)为流动相;检测波长为241 nm。理论板数按松香酸峰计算应不低于3000。
对照溶液的制备(临用新制) 取松香酸对照品适量,精密称定,加乙醇制成每1ml含2µg的溶液,作为对照品溶液。另取11-羰基-β-乙酰乳香酸对照品适量,精密称定,加乙醇制成每1ml含2µg的溶液,作为参照溶液。
供试品溶液的制备 取本品,研细,取0.2g,精密称定,精密加入乙醇20ml,称定重量,超声处理20分钟,放冷,再称定重量,用乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。
测定法 分别精密吸取供试品溶液、对照品溶液与参照溶液各10µl,注入液相色谱仪,记录色谱图。
结果判定 供试品色谱中,在与松香酸对照品溶液色谱峰保留时间相应的位置上不得出现相同的色谱峰。若出现保留时间相同的色谱峰,采用二极管阵列检测器比较相应色谱峰的紫外-可见吸收光谱,吸收光谱应不同(松香酸对照品色谱峰在241nm显示最大吸收);若吸收光谱相同,且该色谱峰的峰面积大于11-羰基-β-乙酰乳香酸参照溶液色谱峰的峰面积值,则视为阳性检出。
备注:必要时,可采用高效液相色谱-质谱联用方法验证。
起草单位:连云港市食品药品检验检测中心
复核单位:海南省药品检验所
云南省食品药品监督检验研究院
小柴胡颗粒中黄芩提取物检查项补充检验方法
(BJY 202304)
【检查】黄芩提取物 照高效液相色谱法(中国药典2020年版通则0512)测定。
色谱条件与系统适用性试验 以十八烷基硅烷键合硅胶为填充剂(建议色谱柱的内径为4.6mm,粒径为2.7μm);以甲醇为流动相A,0.5%甲酸为流动相B,按下表中的规定进行梯度洗脱;流速为每分钟0.6ml;检测波长为270nm。理论板数按黄芩苷峰计算应不低于5000。
|
时间(分钟)
|
流动相A(%)
|
流动相B(%)
|
|
0~10
|
5→25
|
95→75
|
|
10~40
|
25→55
|
75→45
|
|
40~55
|
55→80
|
45→20
|
参照物溶液的制备 取黄芩对照药材0.1g,加水煎煮1.5小时,滤过,滤液浓缩至近干,加入50%乙醇溶液25ml,密塞,超声处理(功率350W,频率37kHz)45分钟,取出,放冷,摇匀,滤过,滤液用0.22μm微孔滤膜滤过,作为对照药材参照物溶液。另取黄芩苷对照品和汉黄芩苷对照品适量,加甲醇制成每1ml各含60µg的混合对照品溶液,摇匀,用0.22μm微孔滤膜滤过,作为对照品参照物溶液。
供试品溶液的制备 取本品,混匀,研细,取约1g﹝规格(1)﹞、0.4g﹝规格(3)﹞、0.3g﹝规格(2)、规格(4)﹞或0.25g﹝规格(5)﹞(均相当于含黄芩生药量0.056g),精密称定,置具塞锥形瓶中,精密加入50%乙醇溶液25ml,密塞,称定重量,超声处理(功率350W,频率37kHz)45分钟,取出,放冷,再称定重量,用50%乙醇溶液补足减失的重量,摇匀,滤过,滤液用0.22μm微孔滤膜滤过,即得。
测定法 分别吸取参照物溶液与供试品溶液各5μl,注入超高效液相色谱仪,测定,即得。
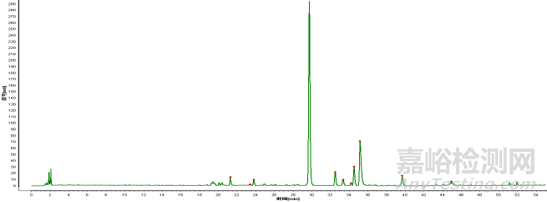
结果判定 供试品色谱中应呈现与对照药材参照物中5个主要特征峰保留时间相对应的色谱峰,其中峰1与峰4应与对照品参照物峰保留时间一致,且峰4与峰1的峰面积比值应不低于0.10。
对照特征图谱
5个特征峰中 峰1:黄芩苷;峰4:汉黄芩苷;峰5:黄芩素
注:规格(1)每袋装10g;(2)每袋装5g(无蔗糖);(3)每袋装4g(无蔗糖);(4)每袋装3g(无蔗糖);(5)每袋装2.5g(无蔗糖)。
起草单位:广东省药品检验所
复核单位:湖南省药品检验检测研究院