您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-01-10 11:01
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
FDA发布2021年新药年度报告。FDA药物评价和研究中心(CDER)发布2021年度的新药获批报告。2021年,FDA总计批准50款新药,这一数值雄踞近二十年的第三位。在50款创新药中,有27款属于“first-in-class”疗法,占获批新药总数的54%(27/50),其占比和绝对数值均为近十年来的最高值;有14款曾斩获“突破性疗法认定”,绝对数为2015年至今的第三高。
国内药讯
1.CDE再次五连发指导原则。2022年1月7日,CDE再次连布5个技术指导原则,均与临床有关:《中药新药毒理研究用样品研究技术指导原则(试行)》;《药物非临床依赖性研究技术指导原则》;《改良型新药调释制剂临床药代动力学研究技术指导原则》;《创新药人体生物利用度和生物等效性研究技术指导原则》和《药物临床试验随机分配指导原则(试行)》。自发布之日起施行。
2.再鼎HER2单抗报NDA。再鼎医药马吉妥昔单抗(margetuximab)的上市申请获CDE受理,拟联合化疗用于治疗既往已接受过两种或两种以上抗HER2治疗方案的HER2+转移性乳腺癌(其中至少一种治疗方案用于转移乳腺癌)。margetuximab是MacroGenics公司开发的一款HER2单抗,经Fc工程化优化,以增强其免疫系统的参与度,并利用抗体依赖性细胞介导的细胞毒性作用(ADCC)影响癌细胞的杀伤力。
3.恒瑞PD-1获批肝癌III期临床。恒瑞医药PD-1注射用卡瑞利珠单抗和VEGFR-2抑制剂甲磺酸阿帕替尼片获国家药监局临床试验默示许可,即将开展一项III期临床,评估卡瑞利珠单抗和甲磺酸阿帕替尼片联合经肝动脉化疗栓塞术对比单纯TACE用于不可切除肝细胞癌患者的疗效。PD-1/PD-L1抗体联合抗血管生成药物能够发挥协同增效作用,并在肝癌(如IMbrave150研究)获得积极结果。
4.南开大学新型肠动力促进剂报IND。南开大学研发团队开发的1类新药CP0119片的临床试验申请获CDE受理。CP0119是一款肠动力促进剂,通过与transgelin蛋白的结合,进而促进actin蛋白聚集,以增强肠肌细胞收缩和肠蠕动。该新药拟开发用于治疗结肠慢传输性疾病。此前,南开大学与天津国际生物医药联合研究院、华润医药中国医药研究开发中心签署了CP0119项目的产学研合作开发协议。
5.乐普PD-L1/TGFBRII融合蛋白报IND。乐普生物重组人源化抗PD-L1单克隆抗体/人TGF-β融合蛋白注射液(LP008)的临床试验申请获CDE受理,拟开发用于实体瘤的治疗。LP008可以阻断PD-1/PD-L1通路,并中和肿瘤微环境中的TGF-β,PD-1和TGF-β负信号的共同抑制可带来比任一单独途径抑制更加有效的抗肿瘤免疫应答,增强抗肿瘤疗效。目前,国内仅有恒瑞医药和默克的PD-L1/TGFBRII抗体融合蛋白处于临床阶段。
6.悦康药业拟开发抗新冠多肽药物。悦康药业日前发布公告,宣布与中国医学科学院病原生物学研究所签署《技术转让(专利权)合同》,合作开发针对新冠病毒肺炎的广谱冠状病毒膜融合抑制剂多肽药物。目前,该新药已完成早期筛选、细胞水平SARSCoV-2变异株及其它hCoV活性检测、体外活病毒活性检测、细胞毒性检测和初步成药性分析,尚处于临床前研究阶段。
7.科伦药业2021年净利润增长超30%。科伦药业发布2021年业绩快报。2021年全年实现营业总收入172.29亿元,同比增长4.64%;实现归属于上市公司股东的净利润10.96亿元,同比增长32.16%;实现归属于上市公司股东的扣除非经常性损益的净利润10.15亿元,同比增长61.54%。根据公告,净利润增长主要原因为该公司积极优化产品结构,销售收入增加,毛利及毛利率同比增长。
国际药讯
1.创新GnRH拮抗剂Ⅲ期临床积极。ObsEva公司口服GnRH拮抗剂linzagolix治疗中重度子宫内膜异位症相关疼痛(EAP)的Ⅲ期临床达主要终点。与安慰剂相比,200mg linzagolix联合反向添加疗法(ABT)治疗组在第3个月时有更多患者痛经和非经期盆腔疼痛症状显著减轻。75mg linzagolix单药治疗组第3个月时与安慰剂相比,患者表现出统计学显著性的痛经改善,但未达到非经期盆腔疼痛减轻的共同主要终点。两种剂量水平的linzagolix均显示出良好耐受性。
2.赛诺菲拟52亿美元合作开发多种新药。赛诺菲联合Exscientia公司将利用后者特有的AI个体化技术平台,共同开发多达15种用于肿瘤和免疫治疗的新型小分子疗法。根据协议条款,Exscientia将获得1亿美元的预付款,总金额高达52亿美元的里程碑潜在付款,与产品的销售分成。Exscientia将负责靶标发现、药物设计和先导化合物优化等活动,赛诺菲则将负责药物的临床前和临床开发、生产和商业化。
3.默沙东布局蛋白酶创新生物药。AI驱动并专注于开发复杂蛋白骨架的创新生物制品公司Absci与默沙东达成一项研究合作,将通过其集合大肠杆菌的合成生物学平台SoluPro、纯化平台SoluPure和AI驱动的药物发现平台,为默沙东开发多达3个靶点的蛋白酶候选疗法。根据协议,Absci将获得6.1亿美元的预付款和研发费用,还有资格获得里程碑潜在付款以及产品的销售分成。
4.安进布局创新蛋白疗法。安进与Generate Biomedicines达成一项研究合作协议,将利用后者开发的人工智能(AI)药物发现技术平台,合作开发5个靶标的新型蛋白候选疗法,用于多个治疗领域和治疗模式。根据协议,Generate将获得5000万美元的预付款,和每一个项目高达3.7亿美元的里程碑后期付款以及产品的销售分成,合作潜在总金额将超过19亿美元。
5.赛诺菲终止个性化细胞疗法合作。赛诺菲宣布将镰状细胞病候选药物SAR445136归还给Sangamo公司,并将研发重点转移到同种异体通用基因组医学方法上。一项最新试验数据显示,接受SAR445136治疗后26周,镰状细胞病患者的总血红蛋白保持相对稳定,没有1例患者需要额外输血;患者中胎儿血红蛋白水平也出现升高趋势;未发现与SAR445136治疗相关的不良事件。
医药热点
1.湖北:执业药师可多点执业。湖北省药监局日前印发的《关于深入优化营商环境助推生物医药产业高质量发展的若干措施》明确,要探索药品经营监管改革,畅通市场大循环。《措施》谈到了多项利好药店的改革,包括取消药店面积、间距限制,支持互联网药品销售和远程药学服务等。同时,对执业药师的在岗履职也提出了新的要求——有条件放宽执业药师多点执业。
2.血站服务体系建设五年规划发布。国家卫健委日前发布《全国血站服务体系建设发展规划(2021—2025年)》提出,在华北、东北、华东、中南、西南、西北六大区域,依托高水平省级血液中心建设区域血液安全中心;在湖北省武汉市设立国家新冠肺炎康复者恢复期血浆储备库,各省份设立省级储备库;力争到2025年,血站卫生技术人员占职工总数≥75%,本科以上专业技术人员占比≥60%。
3.国家将大力培养“公卫博士”。1月5日,国家教育部等五部门联合发布《关于开展高水平公共卫生学院建设的通知》和《高水平公共卫生学院建设指南》,提出到2030年,我国要建成若干所具有中国特色世界一流水平的公共卫生学院。指南明确,国务院学位委员会将加速公卫博士专业学位(DrPH)的正式设立,以培养公卫“实战型”领军人才。
评审动态
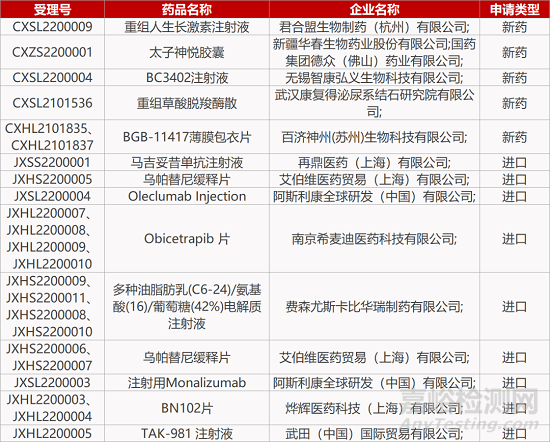


来源:药研发