您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-12-10 14:17
1 基本概念
晶习是指晶体生长趋向形成某一种特定形态的特性,也称为晶体习性、晶癖等。如六方晶体在特定方向生长较快或生长被抑制,棱柱状的晶习可能变为板状或薄片状晶习(b→a),也可能变为针状晶习(b→c)。晶习的改善,本质上是改变了晶体不同晶面的生长速度。
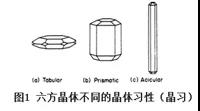
严格定义上讲,晶习≠外观形状≠晶体形貌。外观形状是晶体生长、晶体破碎、断裂、聚结后呈现的最终静态的形状结果。晶体形貌=晶体的外观形状+粒度大小,增加了对晶体大小尺寸描述。
在药物晶体实际研究应用中,技术人员大多将晶习和晶体外观两个概念等同使用。本文主要目的技术领域讨论,因此概念应用上,也将二者等同,表达意思均是强调外观形状对API理化性质、工艺后处理及制剂工艺的影响。
2 药物晶习粒度控制的原因
药物固体的粒度及晶习,制剂中已普遍较重视。制剂中是否需要制定粒度的标准,有相应的指导原则(ICHQ6A 决策树3#):粒度大小是否是影响溶出度、溶解度、生物利用度、制剂稳定性、制剂均匀度、制剂产品外观的关键因素,从以上角度决策制剂中药物粒度大小的研究。
晶体外观(晶习)对制剂的影响,虽暂无“官方的”指导原则,但固体口服制剂或者悬浮制剂研究项目中,常常会遇到需要关注改善晶习的情况:
(a)晶习影响制剂的处理,如细针状晶体,流动性差,容易在制剂工艺中堵塞聚结,造成无法下料等情况发生;
(b)晶习影响压片性能,如晶体形貌的对称性是片剂直压工艺的必要条件。
(c)晶习影响溶解速度及溶出,如肿瘤药甲磺酸索拉非尼,相同晶型和筛分粒度下,不同晶习在纯水、PH=1.2胃液模拟液以及小鼠体内吸收曲线均存在明显差异。
(d)晶习影响制剂产品的稳定性,影响制剂的储存;如甲氧苄氨嘧啶悬浮液,相同晶型和筛分粒度下,虽然不同晶习产品临床试验中人体内吸收曲线相似,但不同晶习对制剂悬浮沉降性能影响巨大,从而影响悬浮制剂的稳定性。
(e)晶习需要给予足够的重视,以保证制剂过程的可重现性。
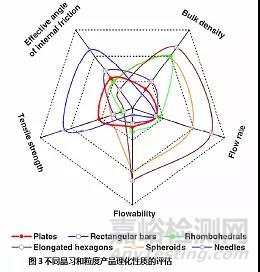
综上所述,药物晶体的晶习和粒度均会影响制剂的处理、储存、压片性能、溶解性、溶出、悬浮制剂的稳定性等,相辅相成,二者共同决定药物晶体的理化性质,适合制剂开发的晶习和粒度,均是各种考察指标的最优权衡的结果(如图3所示)。
3 晶习粒度改善的方法
晶习和粒度的调控的本质是调控晶面的生长速度和晶面的数量。结晶过程变量:溶剂种类、温度、过饱和度、添加剂或杂质、搅拌速度、降温速率等,通过影响晶体的成核(主要影响晶面数量)和生长(晶面生长速率)来调控晶习和粒度。结晶过程变量对晶习和粒度大小及分布的影响不能一概而论,其复杂之处在于,每个过程变量并非独立于另一个变量,而是相互作用。此处列出结晶过程变量对晶习和粒度的改善作用,仅仅是一个指导方针。
(1)过饱和度
高过饱和度:API-溶剂分子间作用力较强情况下,晶体沿特定某一方向的生长较快,容易生成针状晶体,生长越快的晶面,越先消失,生长慢的晶面决定产品理化性质。高过饱和度下容易爆发成核,成核的速度大于生长的速度,常常得到小粒度固体。
低过饱和度:API-溶剂分子间作用力较弱的情况下,片状晶体较多。粒度及分布较容易控制均匀。
(2)降温速率(蒸发速率)
快速降温:晶体生长较快,容易得到“非对称晶习”,如薄片状晶体,片状晶体不适合片剂直压工艺;
较慢降温速率:晶体生长速度减缓,容易得到“对称且致密的晶体”,后续工艺稳定且较好。
(3)搅拌速率
高搅拌速率:传质较快,各晶面表面的溶质分布较均匀,易得到粒度较小,粒度分布较优,短棒状晶习,产品流动性好,高搅拌速率易得到满足悬浮制剂沉降稳定性要求的晶习及粒度。
低搅拌速率:流体立场分布不均匀,溶质分子选择性的分布在特定的晶面上,容易产生大片状晶体(主要是薄片状晶体),晶体尺寸较大,但对制剂来说不利于后续制剂;
(4)溶剂的影响
溶质-溶剂间强相互作用力:成核会被延后,粒度细小,晶体对称生长得到流动性较好的棱柱状晶体,一般需要较高的溶液体积比,才能得到较好的晶体形貌。另外一方面,溶剂可能与API分子特定的基团相互作用力强,从而影响特定晶面的生长速度,从而改善晶习。一般来说,筛选溶剂体系,是改善晶习考察的第一步。
溶质-溶剂间弱的相互作用力:易成核,晶体生长较快,得到相对尺寸较大的晶体。
(5)温度的影响
低温:快速成核得到不规则的晶体、树杈分叉状晶习,不利于后续制剂的开发;
高温:成核被抑制,均匀对称的晶体容易产生;更容易得到较好形貌及粒度分布的产品用于口服制剂的开发;
(6)杂质的存在
杂质或添加剂的存在,吸附在特定晶面或特定官能团与高分子或溶质相互作用,抑制特定晶面的生长,从而会改善晶习。添加杂质去改善晶习,一般不会应用于工业化生产。对于悬浮制剂,考察悬浮制剂辅料与晶体相互作用避免晶体的聚集沉降。
(7)超声的作用
超声加温度控制:得到粒度分布较窄的药物晶体粉末,也是制备球形晶体的方法之一。
4 表征及量化:粒度+形状
某一物体的形貌通常以“尺寸”—长宽厚度来描述。而一堆药物晶体粉末的形貌描述,则以粒度大小、粒度分布外加外观形状如棱柱、棱锥、板状、针状、片状、块状、棒状等来描述。粒度分析仪通过参数D10/D50/D90及径距,可以实现较高精度的量化药物晶体粉末的粒度大小和粒度分布。但对于形状的量化,暂时没有公认的标准。某些缓控释注射剂,质量标准中,会严格限制粒度大小,粒度分布(径距)以及比表面积(通过比表面积对晶习定质量标准)。
结束语:药物晶体产品主要关注维度有两个:一个维度是晶型,另一个维度是晶体形貌。晶型反映的是药物晶体“内部结构”,即不同的晶型本质代表晶胞的排列方式的差异。晶体形貌则反映的是晶体“外部的形貌”的差异。本文主要集中探讨,晶型不变(晶体内部结构相同),晶习和粒度对制剂的影响以及改善晶习粒度的方法。药物晶型的研究,既需要研究晶型内部结构,也需要研究外部晶体形貌,做到“内外兼修”!
参考文献:
[1] Tiwary A K , Jindal M . Crystal Habit Changes and Dosage Form Performance[J]. 2012:1-19.
[2] Pudasaini N , Upadhyay P P , Parker C R , etal. Downstream Processability of Crystal Habit-Modified Active PharmaceuticalIngredient[J]. Organic Process Research & Development, 2017, 21(4):571-577.
[3] Phan C U , Shen J , Yu K , et al. Impact ofCrystal Habit on the Dissolution Rate and In Vivo Pharmacokinetics of SorafenibTosylate[J]. Molecules, 2021, 26(11):3469.

来源:药事纵横


